Teorie - Biologie - kompletní přehled (teorie + úkoly)
Chemické složení bioplazmy
Prvky
Stejné chemické složení je sice jednou z obecných vlastností všech typů buněk, ale chemické prvky jsou součástí i neživé přírody. Některé prvky se nacházejí v živých organizmech častěji než v jejich neživém okolí. Prvky, které se vyskytují v živých organizmech, se nazývají biogenní a dělí se na makrobiogenní (makroprvky, makroelementy) a mikrobiogenní.
MAKROBIOGENNÍ PRVKY zahrnují C, H, O, N, S, P, K, Na, Cl, Ca, Mg a Fe. Mezi nejdůležitější makrobiogenní prvky se řadí C, H, O, N, S a P. Tyto prvky jsou obsaženy v informačních makromolekulách (nukleových kyselinách a proteinech) a představují až 95 % celkové hmotnosti živých organizmů. Uhlík patří mezi nejtypičtější prvky živých organizmů. Primárním zdrojem veškerého uhlíku je pro živou přírodu oxid uhličitý. Vodík a kyslík jsou vázány v molekulách vody, která je podstatnou složkou každé buňky. Dusík je součástí všech nukleových kyselin a proteinů. Síra je součástí některých aminokyselin a fosfor je přítomen jak v nukleových kyselinách, tak ve sloučeninách, které se účastní energetických přeměn v buňce (adenosintrifosfát, ATP). Vápník a hořčík umožňují činnost mnoha enzymů. Vápník také funguje jako druhý posel v buněčné signalizaci a uplatňuje se při svalovém stahu.
MIKROBIOGENNÍ PRVKY (OLIGOBIOGENNÍ, MIKROELEMENTY, STOPOVÉ PRVKY) zahrnují především těžké kovy a dále některé další prvky (Cu, Mn, Co, Br, Se, I, F, B, Si, Li, Ba, Zn atd.), tvoří asi 0,1 % celkové hmotnosti živých organizmů. Větší množství těžkých kovů se může v živých organizmech hromadit (kumulovat) nebo může mít přímo toxický účinek.
PŘÍPRAVA MIKROSKOPU K MIKROSKOPOVÁNÍ znamená umístění mikroskopu tak, aby nosič tubusu byl od pozorovatele odvrácen a volná strana mikroskopického stolku směřovala k němu. Mikroskop musí být snadno v dosahu, aby pozorovatel mohl pohodlně sedět. Nejlépe je psát záznamy vpravo od mikroskopu a vlevo si umístit potřeby pro přípravu preparátů (leváci naopak). Mikroskop se spouští spínačem umístěným v podstavci mikroskopu. Pokud přerušujete mikroskopování pouze na čas, mikroskop nevypínejte (opakovaným zapínáním se zkracuje životnost žárovky). Preparát se vkládá do rohu upínacího zařízení stolku a poté se uchytí svorkou. Při mikroskopování se postupuje od nejméně zvětšujících objektivů po nejvíce zvětšující, tj. 4×, 10×, 40× a 100×.
Při zvětšení 40× a vyšším je vhodné korigovat optické vady očí, protože většina lidí nemá obě oční čočky stejně dioptricky silné. Nejdříve je třeba upravit rozestup okulárů (oční rozestup) a poté se snažit pozorovat obraz oběma očima. Pozorování jen jedním okem vyvolává jeho neúměrnou zátěž a při opakovaném zatěžování zhoršuje vady oka. Rozdíl vede opět k neúměrnému zatěžování jednoho oka. Vadu je možné kompenzovat úpravou dioptrické síly levého okuláru takto: zavřete levé oko a obraz dokonale zaostřete mikrošroubem při pozorování pravým okem v pravém okuláru, zakryjte si pravé oko a pozorujte obraz levým okem v levém okuláru. Pokud není obraz dokonale ostrý, zaostřete objekt pomocí točítka dioptrické korekce na levém okuláru. Poté byste měli oběma očima vidět stejně ostře. Vyhledáním optimální vzdáleností očí od okulárů docílíte při troše cviku splynutí obrazu z obou okulárů a obě oči tak budete zatěžovat rovnoměrně.
Látky
Látkové složení buňky tvoří voda (70 %), proteiny (15 %), nukleové kyseliny (7 %), polysacharidy (2 %), fosfolipidy (2 %), ionty a malé molekuly (4 %).
NUKLEOVÉ KYSELINY (NK) jsou tvořeny nukleotidy, jejichž pořadí (sekvence) určuje primární strukturu NK. Nukleové kyseliny tvoří genomy živých organismů.
Složení nukleotidu: kyselina fosforečná + pentóza (ribóza či deoxyribóza) + dusíkaté báze (purinové: adenin (A), guanin (G), pyrimidinové: cytozin (C), tymin (T) a uracil (U). Dusíkaté báze se spolu spojují na základě komplementarity: A-T (A-U), C-G.
Typy NK:
-
Deoxyribonukleová kyselina (DNA) je tvořena zpravidla 2 polynukleotidovými řetězci (dvouvláknová, dvouřetězcová). V ose řetězce se střídá kyselina fosforečná s cukrem (deoxyribóza), spojené esterickou vazbou. Na cukr se glykozidovou vazbou váže dusíkatá báze, která je spojena s dusíkatou bází druhého řetězce vodíkovými můstky (mezi A a T jsou 2 vodíkové můstky, mezi C a G jsou 3 vodíkové můstky). V roce 1953 popsali J. Watson a F. Crick sekundární strukturu DNA jako pravotočivou dvouřetězcovou šroubovici, jejíž řetězce probíhají antiparalelně, tzn. na jednom konci řetězce DNA je fosfátová skupina (5’ konec), zatímco na druhém je pentóza (3’ konec). Na druhém vláknu je to obráceně.
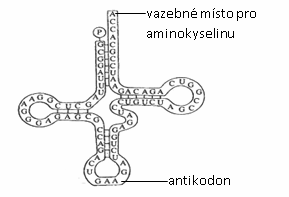
Obr.: tRNA "jetelový list"
- Ribonukleová kyselina (RNA) je tvořena zpravidla 1 polynukleotidovým řetězcem (jednovláknová). Skládá se z kys. fosforečné, cukru ribózy a dusíkatých bází A, U, G, C. Existuje několik typů RNA: transferová (tRNA), ribozómová (případně ribozomální, rRNA), mediátorová (mRNA), malá interferující (siRNA), ribozymová, virová (vRNA).
Nukleové kyseliny se množí replikací (u eukaryot probíhá v jádře, mitochondriích a chloroplastech, u prokaryot v cytoplazmě) – viz přednáška. Genetická informace obsažena v DNA se přepisuje do mRNA během transkripce (u eukaryot probíhá v jádře, mitochondriích a chloroplastech, u prokaryot v cytoplazmě), na ní navazuje translace (syntéza proteinů).
Funkce:
- Uchování genetické informace
- Ovlivnění činnosti buňky a celého organismu (prostřednictvím syntézy proteinů)
VODA tvoří u většiny živých organizmů 60 – 90 % jejich hmotnosti. Málo vody obsahují jen některé spory a semena jako adaptaci pro přetrvání v nepříznivých podmínkách. Voda byla nezbytným prostředím při vzniku života na Zemi a dodnes je podmínkou života. Životně důležité chemické reakce probíhají pouze ve vodných roztocích. Molekuly a ionty rozpuštěné ve vodě mohou prostupovat buněčnými povrchy. Voda má funkci rozpouštědla, pomáhá udržovat konstantní teplotu a udržuje stálost vnitřního prostředí – má význam pro osmotické děje v buňkách a udržování acidobazické rovnováhy.
PROTEINY jsou složeny z aminokyselin (AK).
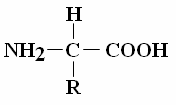
Obr.: Obecný vzorec aminokyseliny: (NH2 – aminová skupina, COOH – karboxylová skupina, R – postranní řetězec).
Dnes existuje 22 aminokyselin (ke 20 běžnějším patří ještě selenocystein a pyrolysin), které se značí třípísmenným nebo jednopísmenným kódem: např. alanin (Ala, A), glycin (Gly, G), valin (Val, V), leucin (Leu, L). Aminokyseliny (AK, případně AA – amino acids) se spojují kovalentní peptidovou vazbou (spojuje se aminová skupina jedné AK s karboxylovou skupinou druhé AK), čímž vzniká peptidový řetězec, který má N konec (aminový, zakončen NH2 skupinou) a C konec (karboxylový, zakončen COOH skupinou). Běžný proteiny (bílkovina) je tvořena až 300 AK. Proteiny vznikají během genové exprese při translaci (překlad genetické informace z mRNA do pořadí aminokyselin) na ribozomech, které jsou vázané na drsné endoplasmatické retikulum (eukaryota) nebo volně v cytoplazmě (prokaryota) – viz přednáška. U proteinů rozlišujeme tyto struktury (konformace): primární – je dána pořadím aminokyselin v polypeptidovém řetězci, zapisuje se od N-konce k C-konci proteinu (první určení primární struktury provedl v roce 1953 Frederick Sanger), sekundární - prostorové uspořádání polypeptidového řetězce, např. alfa šroubovice (alfa-helix), struktura skládaného listu (beta-sheet), terciární – trojrozměrné uspořádání celého peptidového řetězce, kvarterní – uspořádání podjednotek v proteinových aglomerátech, tvořících jednu funkční bílkovinu např. fibrily kolagenu.
Funkce:
- Stavební (strukturní): jsou součástí buněčných struktur, cytoskeletu, chromozomů a ribozomů (proteiny + NK), biomembrán (proteiny + fosfolipidy), buněčné stěny a extracelulární matrix (proteiny + polysacharidy).
- Enzymatická: urychlují chemické reakce (snižují aktivační energii chemických reakcí).
- Informační: podílí se na buněčné signalizaci (signály, receptory).
SACHARIDY jsou složeny z monosacharidů s obecným vzorcem (CH2O)n. Monosacharidy se spojují kovalentními glykozidovými vazbami za vzniku disacharidů, oligosacharidů (trisacharidy, tetrasacharidy atd.) až polysacharidů (tisíce jednotek).
Funkce:
- Energetický zdroj: glukóza, glykogen (živočichové), škrob (rostliny).
- Mechanická podpora: celulóza (rostliny), chitin (kostra hmyzu, buněčná stěna hub), glykolipidy, glykoproteiny (složka slizů, hlenu, chrupavek, buněčné membrány).
LIPIDY jsou tvořeny mastnými kyselinami a glycerolem.
Funkce:
- Stavební: fosfolipidy - součást buněčných membrán.
- Energetický zdroj: tukové kapénky.
- Signalizace: steroidní hormony.
- Metabolismus vitamínů: vitamíny (A, D, E, K) jsou rozpustné v tucích.
Kontrolní otázky – chemické složení bioplazmy
- Umíš zapsat obecný vzorec aminokyselin?
- Kolik existuje proteinogenních aminokyselin? Uveď příklady aminokyselin.
- Jak a kde vznikají proteiny?
- Umíš namalovat ribozom a tRNA?
- Jaké jsou konformace proteinů? Umíš je nakreslit?
- Jaká je funkce proteinů v buňce?
- Z čeho se skládají po chemické stránce nukleové kyseliny?
- Jak se párují dusíkaté báze v DNA a RNA? Kolik je vodíkových můstků ve vazbě?
- Jaký je rozdíl mezi DNA a RNA?
- Kdo popsal sekundární strukturu DNA?
- Umíš namalovat DNA?
- Jaký je monomer a funkce sacharidů v buňce?
- Jaké jsou stavební složky lipidů a jejich funkce v buňce?
- Co se používá k průkazu škrobu?
- K čemu slouží Lugolův roztok?
- Umíš namalovat škrobové zrno?
- Co se používá k průkazu tuků v buňkách?
- Mezi jaké inkluze patří tukové kapénky a škrobová zrna?
- Co se používá k průkazu proteinů?
- K čemu slouží Hellerova zkouška?
ÚKOLY - Chemické složení bioplazmy (viz úkoly)
Chemické složení bioplazmy
Úkol 1: Průkaz škrobu
brambor, Lugolův roztok
Rozkrojte bramborovou hlízu a skalpelem setřete tekutinu z řezné plochy a naneste na podložní sklo. Pozorujte tvar excentrických škrobových zrn a zakreslete. Poté přidejte k preparátu Lugolův roztok (2KI + I2 + H2O), přikryjte krycím sklíčkem a znovu pozorujte. Jak se změnila barva škrobových zrn?

Obr.: Škrobová zrna – zásobní rostlinné inkluze.
Úkol 2: Průkaz tuků v bioplazmě
TP: jaterní tkáň s tukovou infiltrací barvená na tuky (Sudan III, olejová červeň)
Zakreslete si jaterní buňku s oranžově zbarveným tukem, který se v buňce nachází v podobě tukových kapének nebo vyplňuje celý obsah buňky.
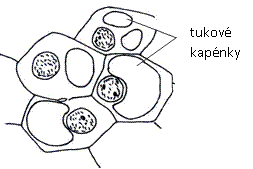
Obr.: Tukové kapénky v jaterních buňkách.
Úkol 3: Průkaz proteinů (Hellerova zkouška – srážecí reakce s koncentrovanou kyselinou dusičnou)
bílek, kys. dusičná
Do zkumavky nalijte asi 2 ml koncentrované kyseliny dusičné a po stěně zkumavky opatrně navrstvěte suspenzi vaječného bílku, tak aby nedošlo k promíchání tekutin. Na styčné ploše obou vrstev se vytvoří bílý prstenec vysrážených (denaturovaných) proteinů.
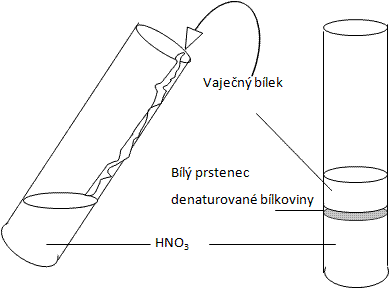
Obr.: Průkaz bílkovin (Hellerova zkouška)
Prokaryota, zastavení objektu pod imerzí
Prokaryota jsou tvořena buňkou prokaryotického typu, která je evolučně starší a jednodušší než buňka eukaryotického typu, průměrná velikost se pohybuje mezi 1-10 µm. Nukleoid (prokaryotické jádro neohraničené membránou) obsahuje jeden chromozom složený z kružnicové dvouřetězcové DNA. Buňka není rozdělena na kompartmenty, neobsahuje mitochondrie ani plastidy. Ribozomy se sedimentační konstantou 70S jsou uloženy v cytoplazmě. Množí se binárním dělením. Prokaryota se dělí na doménu bakterií a archeí.
Doména bakterií (Bacteria)
Bakterie jsou buňky prokaryotického typu. Většina (s výjimkou mykoplazmat) se vyznačuje přítomností buněčné stěny tvořené peptidoglykanem mureinem. Mezi glycerolem a karboxylovými kyselinami v plazmatické membráně je esterová vazba. Geny bakterií neobsahují introny, značná část genů je organizována do transkripčních jednotek typu operonů. Kromě nukleoidu obsahují plazmidy, malé kruhové dvouřetězcové molekuly DNA, které mohou obsahovat geny rezistence k antibiotikům. Tuto informaci si mohou bakterie mezi sebou předávat prostřednictvím konjugace. Při syntéze polypeptidového řetězce se v ribozomech jako první zařazuje aminokyselina N-formylmetionin. Rozmnožují se nepohlavně (binárním dělením nebo pučením), jsou autotrofní (fotoautotrofní nebo chemoautotrofní) nebo heterotrofní (fotoheterotrofní nebo chemoheterotrofní). Pohyb se uskutečňuje pomocí bičíků nebo klouzavým způsobem po povrchu substrátu. Některé bakterie jsou nepohyblivé.
Dělení bakterií:
-
Podle tvaru:
- kulovité (koky): dvojice (diplokoky), řetízky (streptokoky), čtveřice (tetrakoky), hroznovité seskupení (stafylokoky)
- tyčkovité (tyčky, tyčinky): dvojice tyček, řetízky tyček (streptobakterie), tyčky s endosporami mohou mít bacilární tvar (místo se sporou se nerozšíří) nebo klostridiální tvar (spora je uložena v rozšíření uprostřed buňky)
- zakřivené: vibrioidní (vibria), spirálovité (spirily) či helikální (spirochéty)
- větvící se: např. mykobakterie
-
Podle umístění bičíků:
- monotrichální nebo lofotrichální (bičíky na jednom konci buňky)
- amfitrichální (bičíky na obou koncích buňky)
- peritrichální (bičíky po celém povrchu buňky)
-
Podle buněčné stěny:
- Gram-negativní (G-) s buněčnou stěnou – mají tenkou buněčnou stěnu z peptidoglykanu, nad ní je vnější vrstva (membrána) z fosfolipidů a lipopolysacharidů. Při barvení dle Grama se krystalová violeť v komplexu s jodidem draselným neváže na buněčnou stěnu, vymývá se etanolem a po použití jiného barviva (safranin, karbolfuchsin) se buňka zbarví červeně. Patří sem např. Escherichia coli, Salmonella Typhi, Haemophilus influenzae, Klebsiella pneumoniae, Proteus mirabilis, Helicobacter pylori.
- Gram-pozitivní (G+) s buněčnou stěnou – mají silnou buněčnou stěnu složenou z několika vrstev peptidoglykanu. Při barvení dle Grama váže buněčná stěna komplex krystalové violeti s jodidem draselným, buňka se barví modře až fialově. Patří sem např. Staphylococcus, Streptococcus, Enterococcus, Bacillus, Listeria nebo Clostridium.
- bakterie bez buněčné stěny (např. mykoplazmata).
Někteří zástupci bakterií:
- Nitrifikační bakterie: žijí v půdě, oxidují amonné soli na dusitany a ty na dusičnany, tím obohacují půdu o dusík (př. Nitrosomonas, Nitrococcus, Nitrobacter); hlízkové bakterie: žijí v symbióze s bobovitými rostlinami, asimilují vzdušný dusík (např. Rhizobium)
-
Oxygenní fototrofní bakterie: gramnegativní bakterie obsahující bakteriochlorofyl, během fotosyntézy uvolňují O2 podobně jako zelené rostliny. Dělí se na:
- Prochlorofyta – bakterie obsahující bakteriochlorofyl a a bakteriochlorofyl b, nemají fykobiliny, jsou buď jednobuněčné, nebo tvoří vícebuněčná vlákna.
- Cyanobakterie (sinice) – bakterie obsahující bakteriochlorofyl a, fykobiliny (modrý fykocyanin a alofykocyanin, u některých je fykoerytrocyanin nebo červený fykoerytrin) a karotenoidy. Většina druhů žije v rozmezí teplot od 2 °C (antarktická jezera) do 74 °C (horké prameny). Žijí ve sladké i slané vodě, kde jsou součástí planktonu (Trichodesmium erythraeum podmiňuje zbarvení Rudého moře) nebo bentosu. V letních měsících se mohou ve sladkých vodách obsahujících fosfáty a nitráty rozmnožit a vytvořit na povrchu hladiny tzv. vodní květ. Mohou žít endosymbioticky s rozsivkami nebo houbami a exosymbioticky s lišejníky nebo játrovkami.
- Patogenní bakterie vyvolávající onemocnění: např. Salmonella (tyfus, paratyfus), Shigella dysenteriae (úplavice), Streptococcus (angína, spála), Mycobacterium (tuberkulóza), Yersinia pestis (mor člověka).
Doména archeí (Archaea)
Archea jsou také buňky prokaryotického typu. Mají tvar koků, spiril nebo tyček. S výjimkou rodu Thermoplasma mají buněčnou stěnu, která neobsahuje murein, ale může obsahovat pseudopeptidoglykan neboli pseudomurein. Vazba mezi glycerolem a vyššími karboxylovými kyselinami v plazmatické membráně je éterová. Geny přepisované do transferové RNA (tRNA) a ribozómové RNA (rRNA) (nikoli strukturní geny) obsahují introny, které jsou vystřihávány podobně jako u eukaryot, značná část genů je organizována do transkripčních jednotek typu operonů, při syntéze polypeptidového řetězce se v ribozomech jako první zařazuje aminokyselina metionin. Rozmnožují se nepohlavně binárním dělením nebo pučením. Jsou chemoautotrofní nebo chemoheterotrofní (obligátně nebo fakultativně), mezofilní nebo termofilní (rostou i při 100 °C).
Skupiny:
- Extrémně halofilní archea - žijí v prostředí s vysokou koncentrací solí (9 – 23 % NaCl), jako jsou solná jezera.
- Archea produkující metan - vyskytují se v horkých pramenech, v odpadních a stojatých vodách, na dně moří, v trávicím traktu přežvýkavců a termitů, kde přeměňují CO2 a CO na metan.
- Hypertermofilní archea - vyskytují se v horkých sirných pramenech nebo v podmořských vulkanických oblastech při teplotách 45-110 °C. Za anaerobních podmínek redukují síru na H2S, za aerobních podmínek oxidují H2S a síru na H2SO4.
Kontrolní otázky – prokaryota, zastavení objektu pod imerzí
- Jaký je rozdíl mezi eukaryotickou a prokaryotickou buňkou (velikost, stáří, organely, rozmnožování, pohyb atd.)?
- Jaká je velikost bakterií a jaký mikroskop se používá pro jejich pozorování?
- Jaký je rozdíl mezi bakteriemi a archei? Uveď příklady zástupců.
- Jaký je postup barvení dle Grama?
- Jaký je rozdíl mezi G+ a G- bakteriemi? Uveď příklady zástupců.
- Co znamená imerzní objektiv a k čemu slouží?
ÚKOLY - Prokaryota, zastavení objektu pod imerzí (viz úkoly)
Prokaryota, zastavení objektu pod imerzí
Úkol 1: Příprava trvalého preparátu suchou cestou – roztěr bakterií
bakterie G+ a G-, krystalová violeť, Lugolův roztok, etanol, karbolfuchsin
Nejdříve si vyžíhejte bakteriologickou kličku v plameni a poté proveďte kličkou stěr z povrchu agarové půdy porostlé koloniemi bakterií (zástupci Gram-pozitivních a Gram-negativních bakterií). Obsah kličky homogenizujte v co nejmenší kapce vody na podložním sklíčku, po usušení na vzduchu fixujte nad plamenem (stačí 3x protáhnout nad plamenem roztěrem nahoru) a proveďte barvení preparátu.
Postup barvení dle Grama:
- na sklíčko s roztěrem bakterií kápněte barvivo krystalová violeť (nechat barvit 3 min)
- slijte, opláchněte destilovanou vodou a převrstvěte preparát Lugolovým roztokem (KI + I + H2O) (2 min)
- slijte, opláchněte destilovanou vodou a přidávejte etanol tak dlouho dokud se bude barvivo vyplavovat
- opláchněte destilovanou vodou a převrstvěte karbolfuchsinem (1,5 min)
- opláchněte destilovanou vodou a osušte
Pomůcka pro zapamatování postupu barvení: VLAK (violeť, Lugol, alkohol, karbolfuchsin)
Preparát s obarvenými bakteriemi pozorujte pod imerzním objektivem. Do protokolu si zakreslete a zapište, jak se oba typy bakterií navzájem liší, a to tvarem a zbarvením.
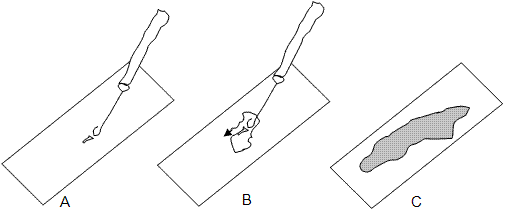
Obr.: Postup zhotovení roztěru bakterií: A – přenos bakterií do kapky vody bakteriologickou kličkou, B – homogenizace, C – hotový roztěr bakterií.
Úkol 2: Pozorování bakterií pod imerzí
TP, NP: zástupci G+ a G- bakterií
Imerzní objektiv slouží k pozorování větších detailů, které již nejsou patrné pod suchými objektivy. Nejdříve je potřeba najít vhodné místo v preparátu při menším zvětšení a umístit objekt do středu zorného pole mikroskopu. Následně je třeba pootočit revolverový měnič do poloviny (mezi objektivy), na krycí sklo nanést kapku imerzního oleje (dostatečně velkou) a dotočit objektiv do optické osy mikroskopu. Tím se spojí čelní čočka objektivu s kapkou imerzního oleje. Další postup: pomocí makroposuvu posunout stolek mikroskopu až do nejvyšší polohy (pozor, ať nepraskne preparát), kontrolovat pohledem ze strany, následně točit makrošroubem opačným směrem, tj. oddalovat stolek s preparátem až se v zorném poli mikroskopu objeví objekt, doostřit mikroposuvem a upravit osvětlení.
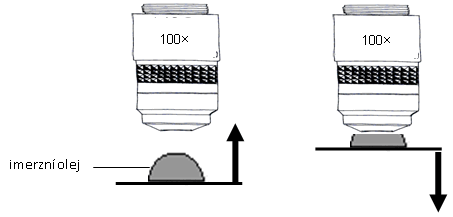
Obr.: Dva způsoby zastavení objektu pod imerzí.
Zásady:
- Mezi objektivem a preparátem musí být imerzní olej, proto je potřeba nanést dostatečně velkou kapku oleje.
- Po skončení práce s imerzním objektivem je nutné očistit čočku objektivu a sklíčko trvalého preparátu alkoholem.
- Nepodaří-li se zastavit pozorovaný objekt pod imerzním objektivem, je třeba olej odstranit a celý postup zopakovat.
Eukarya (eukaryota) – živočišná buňka, protozoa
Jejich základní stavební jednotkou je buňka eukaryotního typu, která je vývojově mladší a složitější než buňka prokaryotního typu. Průměrná velikost eukaryotní buňky se pohybuje mezi 10-100 µm. Eukaryotní buňky se množí mitózou, pohlavní buňky meiózou. Eukaryotní buňka může mít různý tvar a velikost, např. epiteliální buňky jsou kubické, buňky fibroblastů vřetenovité, nervové buňky mají dlouhé výběžky, bílé a červené krvinky u savců jsou obvykle kruhovité, u ptáků oválné. Od vnějšího prostředí je buňka ohraničena polopropustnou cytoplazmatickou membránou. Ribozomy mají sedimentační konstantu 80S. U eukaryotních buněk jsou hojně zastoupeny buněčné organely, které jsou specializovány na různé funkce.
JÁDRO – na jeho povrchu je dvojitá membrána, která odděluje jádro od cytoplazmy. V jaderné membráně se nachází jaderné póry, kterými se uskutečňuje transport molekul z jádra do cytoplazmy a naopak. V jádře jsou chromozomy, které jsou tvořeny lineární DNA a proteiny histony. Jádra různých buněk se liší velikostí, tvarem i počtem.
JADÉRKO je součástí jádra a nachází se jen u eukaryotních buněk v interfázi. Obsahuje geny pro rRNA a tRNA a jejich produkty. Na počátku mitózy jadérko mizí a v telofázi opět vzniká. Počet jadérek v jednom jádře není pevný a také jejich velikost je různá a závisí na metabolické aktivitě buňky.
ENDOPLAZMATICKÉ RETIKULUM (ER) vytváří systém plochých váčků a kanálků a naléhá těsně na jádro. Jsou-li na jejich vnější straně přilehlé ribozomy, jedná se o drsné ER, na kterém probíhá syntéza proteinů. Hladké ER je bez ribozomů a probíhá v něm syntéza lipidů. Endoplazmatické retikulum je rovněž zásobárnou vápníku.
GOLGIHO APARÁT (GA) je systém samostatných plochých cisteren, u rostlin se tradičně označuje jako diktyozom. Do GA jsou transportními váčky (vezikuly) přepravovány z ER proteiny, lipidy a sacharidy, které jsou dále chemicky modifikovány. Primárně se v GA syntetizují látky, které jsou transportovány a vyměšovány z buňky (sekrety, enzymy, hormony) prostřednictvím sekreční dráhy (viz obr.).
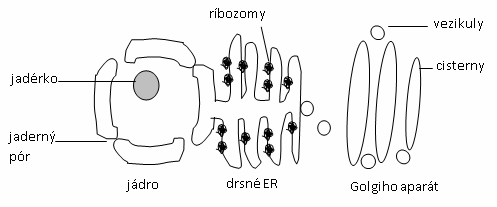
Obr.: Sekreční dráha v buňce.
MITOCHONDRIE jsou oválné organely se dvěma membránami, z nichž ta vnitřní je zprohýbaná v kristy, vnitřní prostor se nazývá matrix (viz obr.). Mají chromozomy, které jsou prokaryotního typu s cirkulární dvojřetězcovou DNA bez histonů. V buňce může být jedna až tisíce mitochondrií. Mitochondrie lze považovat za centra buněčného dýchání a energetická centra v buňce. Uvolňují chemickou energii vázanou v organických látkách (buněčné dýchání) a na vnitřní membráně se syntetizují molekuly ATP (oxidativní fosforylace), které jsou pro buňku okamžitým zdrojem energie.
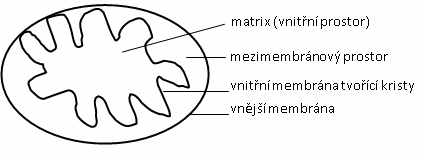
Obr.: Mitochondrie.
PEROXISOMY jsou kulovité útvary, obsahují oxidační enzymy. Podílejí se na katabolismu, detoxikaci látek a odbourání peroxidu vodíku.
LYZOSOMY (lysozomy, lysosomy) jsou malé měchýřkovité útvary obsahující hlavně trávicí enzymy. Dochází zde ke kyselé hydrolýze různých organických makromolekul na složky, které buňka následně využívá na stavbu vlastních makromolekul, nebo které vylučuje.
VAKUOLY se nachází u jednobuněčných eukaryot. Jedná se o potravní (trávicí) vakuoly, které jsou naplněné substrátem se živinami a pulzující vakuoly, které slouží k osmoregulaci (u sladkovodních eukaryot odstraňují přebytečnou vodu).
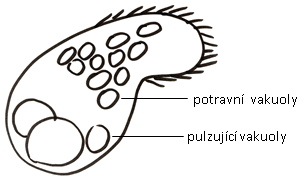
Obr.: Nálevník s vakuolami (pulzující a potravní).
PIGMENTOVÉ INKLUZE – vznikají ukládáním pigmentů. Buňky, které tento pigment obsahují, se označují jako chromatofory (např. melanofory obsahují tmavý pigment melanin).
Mezi eukaryota se řadí jednobuněčné eukaryotické organizmy (protozoa, dříve prvoci), chromista, houby, rostliny a živočichové. Eukaryota se aktuálně člení do šesti říší: OPISTHOKONTA (některá jednobuněčná eukaryota, houby, živočichové), AMOEBOZOA, RHIZARIA, EXCAVATA (v těchto třech říších jsou pouze jednobuněčná eukaryota), ARCHAEPLASTIDA (rostliny, řasy) a CHROMALVEOLATA (chromista a některá jednobuněčná eukaryota).
NÁLEVNÍCI jsou pojmenovaní podle toho, že se objevují v nálevech, např. v senném nálevu připraveném z vody, sena, rozkládajících se rostlin, listů a malého množství hlíny. Všude v přírodě a tedy i v seně jsou přítomné cysty nálevníků, ze kterých ve vodě vzniknou aktivní nálevníci.
Kontrolní otázky – živočišná buňka, protozoa
- Jaký je rozdíl mezi eukaryotickou a prokaryotickou buňkou (velikost, stáří, organely, rozmnožování, pohyb atd.)?
- Co patří mezi eukaryota?
- Jaká je velikost eukaryotní buňky?
- Co je to endosymbióza?
- Jaké organely se nachází v eukaryotické buňce a jakou mají funkci?
- Umíš nakreslit a popsat jádro, Golgiho aparát, endoplazmatické retikulum, mitochondrii?
- Umíš nakreslit nervovou buňku?
- Jaké tvary mohou mít jádra leukocytů?
- Jaké typy a počty jader se mohou vyskytovat u nálevníků?
- Jaké specifické barvení se používá k průkazu Golgiho aparátu a mitochondrií?
- Kde v buňce se nachází mitochondrie?
- Jaké inkluze se mohou nacházet v živočišné buňce?
ÚKOLY - Eukarya (eukaryota) – živočišná buňka, protozoa (viz úkoly)
Eukarya (eukaryota) – živočišná buňka, protozoa
Úkol 1: Tvar buněk – nervová buňka
TP: mícha
Ve ventrálních rozích šedé hmoty míšní vyhledejte neurony, pozorujte a zakreslete tvar nervové buňky (neuron).
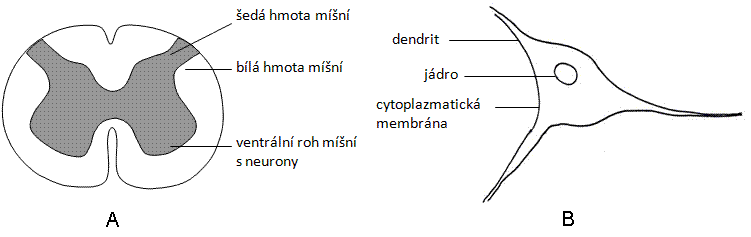
Obr.: A – průřez míchou, B – složení neuronu.
Úkol 2: Tvar a počet jader
TP: jaterní tkáň, leukocyty, nálevníci - trepka (Paramecium sp.), plazivenka (Spirostomum sp.), opalinka žabí (Opalina ranarum)
Pozorujte a zakreslete počet a tvar jader v jednotlivých buňkách. Jádra leukocytů (bílé krvinky) mohou mít tvar kulovitý, bobovitý (ledvinovitý), podkovovitý (tyčinkovitý), segmentovaný (esovitý nebo laločnatý); erytrocyt (červená krvinka) u savčích buněk je bez jádra, u ptáků má jádro oválný tvar. U trepky jsou v cytoplazmě dva typy morfologicky i funkčně odlišných jader: makronukleus (velké jádro vegetativní) a mikronukleus (malé jádro generativní); během procesu konjugace dvou trepek dochází k vzájemné výměně a vývoji těchto jader. Plazivenka má jádro růžencovité/korálkovité (připomíná růženec, korálky na šňůrce), v cytoplazmě opalinky můžeme pozorovat velký počet drobných stejných jader (mnohojaderná buňka).
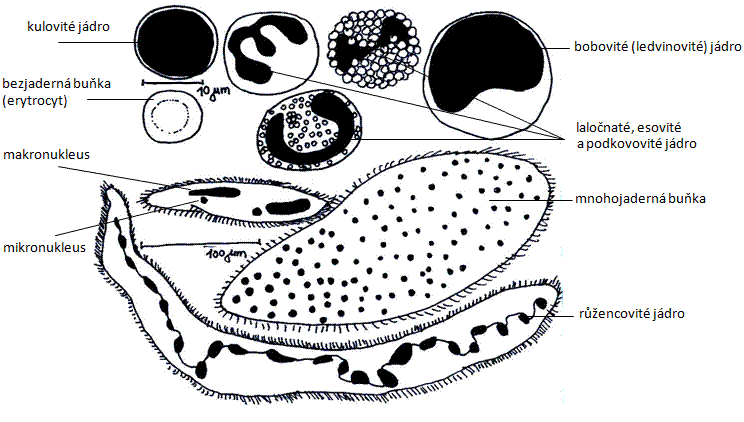
Obr.: Typy buněčných jader.
Úkol 3: Buněčné organely – Golgiho aparát, mitochondrie
TP: tenké střevo (stříbřené a dobarvené hematoxylin-eosinem), játra obarvená na mitochondrie (podle Heidenheina)
Do středu zorného pole zastavte klky střevní sliznice a při větším zvětšení prohlédněte jejich povrchové buňky (enterocyty). V apikální (horní) části buňky nad fialově zbarveným jádrem můžete nalézt Golgiho aparát v podobě hnědočerného klubkovitého útvaru nebo nepravidelné sítě. V jaterních buňkách jsou vidět mitochondrie (drobné tmavě zbarvené čárkovité až oválné útvary) a světlé šedé jádro (případně růžové) s tmavými jadérky. Nakreslete Golgiho aparát a mitochondrie.
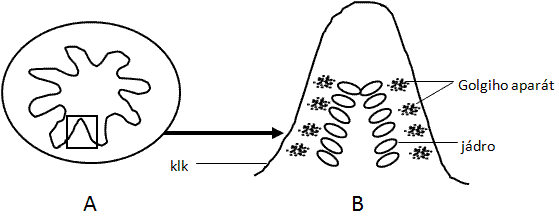
Obr.: A – průřez tenkým střevem, B – střevní klk s enterocyty s Golgiho aparátem a jádrem.
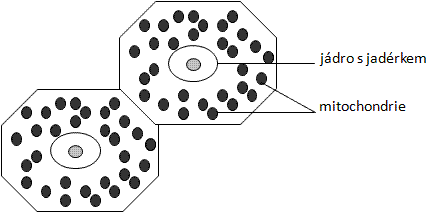
Obr.: Mitochondrie v jaterních buňkách.
Úkol 4: Pigmentové inkluze
TP: kůže žáby
Pod mikroskopem pozorujte buňky epidermis žáby (tzv. chromatofory resp. melanofory) obsahující inkluze pigmentu melaninu. Buněčné inkluze v podobě drobných hnědých zrnek se v cytoplazmě shlukují do hvězdicovitých útvarů s různě dlouhými výběžky, realizuje se tím barvoměna.
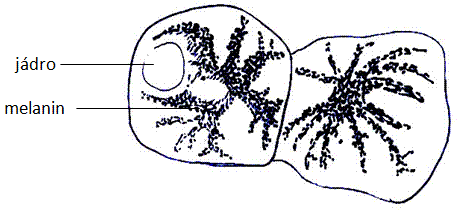
Obr.: Melanofory žáby obsahující melanin.
Eukarya (eukaryota) – rostlinná buňka
Rostlinná buňka je eukaryotického typu (složení eukaryotické buňky bylo popsáno v předchozí kapitole), ale na rozdíl od buňky živočišné má navíc buněčnou stěnu složenou z celulózy, dále obsahuje chloroplasty, zásobní a krystalické buněčné inkluze a velkou centrální vakuolu (ekvivalent lysozomů) s rostlinnými šťávami a barvivy (např. antokyany).
PLASTIDY se podle obsahu barviv rozlišují na bezbarvé leukoplasty, barevné chromoplasty, amyloplasty obsahující škrob, proteoplasty obsahující proteiny, oleoplasty obsahující tuky a chloroplasty obsahující zelené barvivo chlorofyl.
CHLOROPLASTY se nachází u rostlin a jejich funkční ekvivalenty se nacházejí i u některých bakterií. Mají chromozomy prokaryotního typu s cirkulární dvouřetězcovou DNA s histon-like proteiny (např. HC). Uvnitř chloroplastů na tylakoidních membránách probíhá nejdůležitější biochemický proces na Zemi – fotosyntéza spojená s tvorbou ATP (fotosyntetická fosforylace).
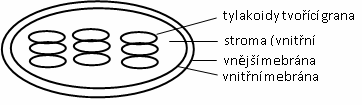
Obr.: Chloroplast – popis.
CENTRÁLNÍ VAKUOLA vyplňuje většinu objemu buňky. Centrální vakuola je ohraničena membránou (tonoplast), která se aktivně podílí na regulaci osmotického tlaku v buňce. Ve vakuolách se ukládají zásobní sacharidy, alkoholy, barviva, ale i odpadní látky a jsou zde i enzymy, které tyto nepotřebné látky rozkládají. Zhoustne-li obsah vakuol, dochází k vykrystalizování některých látek a ke vzniku buněčných inkluzí.
INKLUZE můžeme rozdělit na několik typů: zásobní (např. škrobová zrna, viz kapitola Chemické složení bioplazmy) a krystalické (krystaly šťavelanu vápenatého, které vznikly neutralizací přebytečné kyseliny šťavelové kationty vápníku jako např. rafidy, styloidy a drúzy).
ANTOKYANY jsou barviva, která se nachází např. ve vakuolách buněk oplodí bobulí ptačího zobu (Ligustrum vulgare). Antokyany chrání rostlinu proti nadměrnému ozáření, zvyšují odolnost proti mrazu a suchu a odpovídají za zbarvení, které může být v závislosti na pH červené (kyselé pH), fialové (neutrální pH 6,8-7,3) nebo modré (alkalické pH). Antokyany se vyskytují i v kořenech (červená řepa), stonku (begonie), listech (červené zelí), nebo květech (plicník lékařský).
OSMOTICKÉ JEVY – obecný princip viz kapitola Vyšetření krve
Rostlinná buňka:
- Hypotonické prostředí - voda proudí do buňky tak dlouho, dokud se nevyrovná vnitřní tlak plazmatické membrány protitlaku buněčné stěny, pak proudit přestane. Buněčná stěna je silná, napne se a dochází ke zvýšení turgoru (vnitřní tlak). Při poškození buněčné stěny může výjimečně dojít i k prasknutí buňky.
- Hypertonické prostředí - z rostlinné buňky uniká voda, ale tvar buňky se díky buněčné stěně, která drží tvar, nemění. Cytoplazma a vakuoly zmenšují svůj objem a plazmatická membrána se odděluje od buněčné stěny. Jev se označuje jako plazmolýza.
Kontrolní otázky – eukarya, rostlinná buňka
- Jaký je rozdíl mezi rostlinnou a živočišnou buňkou?
- Umíš nakreslit a popsat chloroplast?
- Co je to tonoplast?
- Co patří mezi krystalické inkluze?
- Co jsou to antokyany a k čemu slouží?
- Jak se mění zbarvení vakuol v bobulích ptačího zobu v závislosti na pH?
- Co je to turgor?
- Co je to plazmolýza (prostá a křečová)?
ÚKOLY - Eukarya (eukaryota) – rostlinná buňka (viz úkoly)
Eukarya (eukaryota) – rostlinná buňka
Úkol 1: Vakuoly, chloroplasty
NP: bobule ptačího zobu (Ligustrum vulgare), voda, NaOH, kys. octová
Rozřízněte bobuli ptačího zobu a obtiskněte na podložní sklíčko. Přidejte vodu, přikryjte krycím sklíčkem a pozorujte. Jaké je zbarvení vakuol (neutrální prostředí)? Pozorujte, jak se změní zbarvení vakuol po přidání kys. octové (kyselé prostředí) a NaOH (zásadité prostředí) a vaše pozorování zapište. Kromě vakuol lze uvnitř buněk pozorovat i drobné zelené chloroplasty.
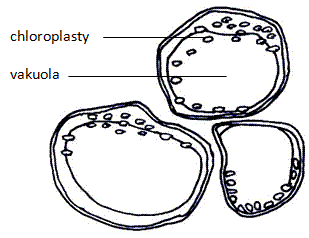
Obr.: Buňky bobule ptačího zobu s centrální vakuolou a chloroplasty.
Úkol 2: RZvýšení turgoru
pyl, voda
Na podložní sklíčko naneste špejlí pylová zrna, pozorujte a zakreslete jejich tvar. Pylová zrna se někdy v preparátu hůře hledají. Nejdříve se snažte zaostřit na vnitřní hranu krycího skla a poté prohledávejte okraje preparátu meandrovitým způsobem při zvětšení 10× (nezapomeňte clonit a proostřovat). Poté přikápněte k pylu kapku destilované vody, přikryjte krycím sklíčkem a znovu pozorujte a zakreslete. Pronikáním vody do pylových zrn, dojde ke změně jejich tvaru (zvětší se a zakulatí), u některých pylových zrn může docházet k praskání - výronům žlutě zbarvené cytoplazmy. Nezaměňujte ale se vzduchovými bublinami, které mají černé kontury.
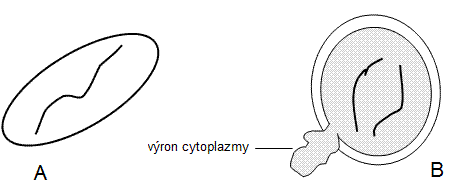
Obr.: Osmotické jevy: A – pylové zrno v izotonickém prostředí, B – pylové zrno v hypotonickém prostředí.
Úkol 3: Plazmolýza (prostá a křečová)
cibule, KNO3
Z cibule sloupněte vnitřní epidermis (protáhlé buňky) a dejte na podložní sklíčko (vyrovnejte epidermis preparační jehlou), přikápněte 1 % neutrální červeň a přikryjte krycím sklíčkem. Po obarvení vakuol do červena přikápněte k hraně krycího skla kapku 1M KNO3 (hypertonické prostředí) a z protilehlé hrany krycího skla odsajte filtračním papírem tekutinu pod krycím sklem. V mikroskopu pozorujte plazmolýzu - oddělování cytoplazmy od buněčné stěny z důvodu úniku vody z buňky do hypertonického prostředí. V jednom preparátu můžete pozorovat zároveň prostou plazmolýzu (oddělování cytoplazmatické membrány od buněčné stěny na protilehlých stranách buňky) a křečovou plazmolýzu (nestejnoměrné oddělování cytoplazmatické membrány od buněčné stěny, centrální vakuola je křečovitě stažená). Plazmolýza může být vratný proces. Nakreslete a napište závěr.
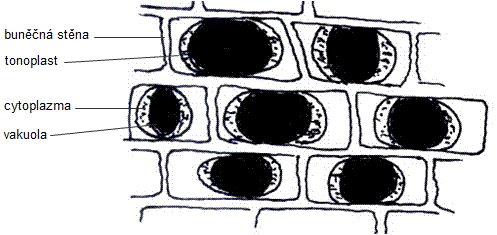
Obr.: Osmotické jevy v buňkách epidermis cibule - prostá plazmolýza
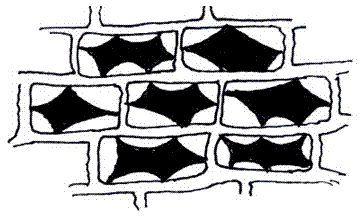
Obr.: Osmotické jevy v buňkách epidermis cibule - křečová plazmolýza
Pohyb a taxe, nativní preparáty
Pohyb a taxe
POHYB MOLEKUL - BROWNŮV MOLEKULÁRNÍ POHYB je náhodný pohyb mikroskopických částic v kapalném nebo plynném médiu. Tento pohyb poprvé zaznamenal v roce 1827 biolog Robert Brown, když pozoroval chování pylových zrn ve vodě. Podstatu tohoto jevu objasnil v roce 1905 Albert Einstein na základě kinetické teorie látek. Molekuly vody se v roztoku vlivem tepelného pohybu neustále srážejí, přičemž směr a síla těchto srážek jsou náhodné. Čím je částice menší, tím je pohyb výraznější.
POHYB BUNĚK/ORGANIZMŮ zahrnuje aktivní změnu tvaru jakékoliv součásti buňky, v užším pojetí se týká lokomoce (pohyb z místa na místo) buňky/organizmu. Na pohybu se podílí vlákna cytoskeletálního systému: mikrofilamenta (aktinová vlákna) a mikrotubuly. Jejich pohyb závisí na transformaci energie chemické v mechanickou, kterou realizují tzv. motorové proteiny (molekulové motory – dyneiny a kineziny asociované s mikrotubuly a myoziny I a II asociované s mikrofilamenty).
CYTOSKELET je součástí všech eukaryotních buněk. Jedná se o systém proteinových různě dlouhých vláken. Podle velikosti a funkce se vlákna cytoskeletu dělí na:
- intermediární (střední) filamenta – z fibrilárních proteinů různých typů (keratiny, vimentiny, neurofilamenta, laminy), dodávají buňkám mechanickou pevnost, vytváří jejich vnitřní kostru a určují umístění některých organel v buňce. Na pohybu buněk se nepodílí.
- mikrotubuly – z globulárních proteinů tubulinů, vytváří vlákna mitotického vřeténka, řasinky a bičíky. Bičíky a řasinky eukaryotních buněk mají v centru 2 samostatné mikrotubuly, na periferii 9 párů mikrotubulů (tj. struktura 9+2).
- mikrofilamenta (aktinová vlákna) – z globulárních proteinů aktinů, vytváří kontraktilní prstenec při dělení živočišných buněk (cytokineze), účastní se améboidního a svalového pohybu.
AMÉBOIDNÍ POHYB (měňavkovitý) je založen na vysílání výběžků (panožek) ve směru pohybu buňky. Růst panožek je zprostředkován klouzáním mikrofilament za pomocí molekulového motoru myozinu I. Po přichycení panožky k podkladu dojde ke kontrakci zadní části buňky a přelití cytoplazmy ve směru vytvořené panožky. Pohyb je charakteristický pro jednobuněčné měňavky (améby); u živočichů se takto pohybují např. makrofágy při fagocytóze.
POHYB BIČÍKŮ A ŘASINEK EUKARYOT (tzv. kinocilií) je podmíněn klouzáním mikrotubulů poháněných molekulovými motory dyneiny. Hlavní strukturou kinocilií je svazek 10 párů mikrotubulů (struktura 9+2, tj. 9 párů po obvodu a 2 mikrotubuly ve středu, viz obr.). Kinocilie jsou na povrchu kryty cytoplazmatickou membránou a v buňce jsou pevně zakotveny v tzv. bazálních tělískách. Bičíky jsou dlouhé a jejich počet bývá malý (1-8). Pozorovat je lze u jednobuněčných eukaryotních organizmů s bičíky, ale i u buněk živočichů (spermie, plaménkové buňky protonefridií), modifikací bičíku je tzv. undulující membrána trypanosom. Řasinky (brvy) jsou krátké a většinou pokrývají celý povrch buňky. Pozorovat je lze především u jednobuněčných nálevníků, u živočichů nalezneme řasinky na tzv. řasinkovém epitelu (např. na povrchu ploštěnek a v dýchacích cestách savců). Modifikacemi brv jsou např. cirri (vzniklé splynutím skupiny brv v silnější útvar a mající pohybovou a opornou funkci), nebo membranelly (vzniklé splynutím řad brv a sloužící k přihánění potravy).
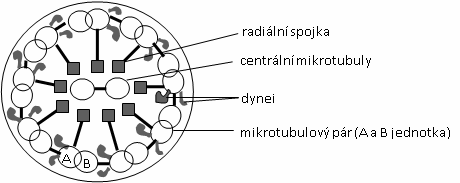
Obr.: Příčný řez kinocilií – struktura 9+2.
SVALOVÝ POHYB je založen na zkracování sarkomer (základní kontraktilní jednotka svalu) svalového vlákna v důsledku posunu aktinových vláken podél myozinových. Impulzem pro svalový stah je nervový vzruch, který vyvolá uvolnění Ca2+ iontů ze sarkoplazmatického retikula (speciální název pro endoplazmatické retikulum ve svalových buňkách). Vápenaté ionty se váží na protein troponin C a způsobí změnu jeho konformace a následně i změnu konformace tropomyozinu, který je navázán na aktinové vlákno. Aktinové vlákno se uvolní z vazby a může reagovat s myozinovým vláknem (tvořeno molekulovým motorem myozinem II) a dojde ke svalovému stahu. Stah se uvolní načerpáním Ca2+ iontů do sarkoplazmatického retikula vápenatými pumpami, aktinové vlákno je opět zablokováno tropomyozinem a svalový stah odezní.

Obr.: Sarkomera – základní kontraktilní jednotka svalu.
TAXE jsou usměrněné pohyby jednobuněčných eukaryot (prvoků) a živočichů na působení podnětu (podráždění).
- fototaxe - pohyb ke světlu
- oxygenotaxe - pohyb do prostředí se zvýšenou koncentrací kyslíku
- chemotaxe - pohyb vyvolaný přítomností chemické látky
Taxe mohou být pozitivní nebo negativní podle toho, jestli je vyvolaný pohyb orientován směrem k podnětu nebo opačně.
Nativní preparáty
NATIVNÍ PREPARÁTY jsou preparáty připravené ze živých objektů neovlivněných žádným fixačním roztokem. Nelze je dlouhodobě uchovávat a není možné pozorovat některé detaily, které nejsou obarveny. Jako médium pro pozorování slouží tekutina, ve které se studované objekty vyskytují za přirozených podmínek (voda, krevní sérum, plazma, kultivační média), nebo tzv. izotonické roztoky, např. fyziologický roztok, nebo PBS (phosphate buffered saline, fosfátem pufrovaný fyziologický roztok). Některé objekty je možné pozorovat pouze položené na podložním skle a přikryté krycím sklem bez použití tekutého média (např. různé kožní deriváty - chlupy a peří, chitinové části členovců - blanitá křídla, šupiny). Pozorování rychle se pohybujících organizmů se usnadní přidáním některých viskózních látek (glycerol, želatina, arabská guma), které zvyšují odpor tekutiny a brzdí tak pohyb organizmů, nebo přidáním některých narkotik (voda s několika kapkami éteru, chloroformu nebo CO2), které v malých dávkách vedou ke zpomalení pohybu. K omezení pohybu někdy stačí zvýšení tlaku na krycí sklo, odsátí přebytečné tekutiny apod. Preparát by neměl být příliš hustý, proto je dobré tekuté objekty ředit, části tkání je vhodné separovat na podložním skle preparační jehlou nebo rozdrtit druhým podložním sklem (kompresní preparát). Jinou metodou je příprava nativního otiskového preparátu, tj. přiložení řezné plochy objektu na podložní sklo, přikápnutí kapky tekutiny, přikrytí krycím sklem a pozorování částic, které ulpěly na skle. Pro dlouhodobé pozorování nativních preparátů slouží různé typy vlhkých komůrek. Ke zvýraznění některých struktur, které jsou pozorovatelné jen v živých organizmech, se používá vitální barvení.
Kontrolní otázky – pohyb a taxe, nativní preparáty
- Jaký je princip Brownova molekulárního pohybu?
- Jaké znáš typy pohybů u buněk/organizmů?
- Jaké cytoskeletální vlákno a molekulový motor se podílí na jednotlivých typech pohybů?
- Uveď příklad buněk s řasinkami a bičíky
- Umíš nakreslit příčný řez bičíkem (struktura 9+2)?
- Jak probíhá svalový pohyb?
- Umíš nakreslit sarkomeru?
- Co je to chemotaxe a oxygenotaxe u nálevníků?
- Jaké vakuoly se nachází u nálevníků?
ÚKOLY - Pohyb a taxe, nativní preparáty (viz úkoly)
Pohyb a taxe, nativní preparáty
Úkol 1: Brownův molekulární pohyb
NP: suspenze oxidu železitého
Kápněte na podložní sklo suspenzi oxidu železitého a přikryjte krycím sklem a pozorujte jednu malou částici a zakreslete trajektorii jejího pohybu.
Jaký je princip pohybu částice?
Úkol 2: Buňky s řasinkami
TP: buňky s řasinkovým epitelem obarvené hematoxylin-eosinem
Pozorujte a zakreslete buňky cylindrického nebo kónického tvaru s viditelným jádrem a řasinkami na širší základně.
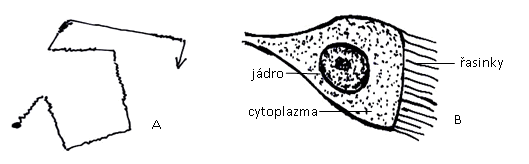
Obr.: A – Brownův molekulární pohyb, B – buňka s řasinkami
Úkol 3: Řasinkový pohyb
NP: senný nálev, detrit z akvária/ video
Z povrchové blanky senného nálevu (nebo detritu z akvária) naberte opatrně kapátkem kapku nálevu, přeneste na podložní sklíčko a pod úhlem 45o přikryjte krycím sklíčkem (rovnoběžně s podložním) tak, aby pod sklíčkem nevznikly vzduchové bubliny. Pozor na chyby: nadbytek vody (vibrace, unášení objektů proudem vody mimo zorné pole, únik ze zaostřené optické roviny, voda na stolku, kondenzoru), nedostatek vody (bubliny, rychlé vyschnutí preparátu). V preparátu pozorujte rychle se pohybující buňky jednobuněčných eukaryot, především nálevníky různých velikostí, drobné bičíkovce, a také velké množství prokaryot (bakterií).
Pohyb řasinek lze pozorovat na obrvených buňkách nálevníků, ale i na povrchu mikroskopických živočichů z akvária (ploštěnky, vířníci). U nálevníků pozorujte i potravní a pulzující vakuoly. Pro lepší pozorování lze použít fázový kontrast.
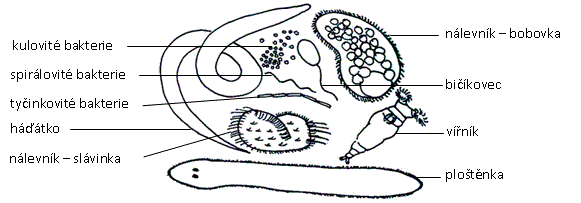
Obr.: Zástupci mikrofauny
Úkol 4: Améboidní pohyb
NP: senný nálev/video
Připravte NP z povrchové blanky senného nálevu a pozorujte améby. Zpočátku jsou améby podrážděné a zakulacené, po několika desítkách sekund se přemění v plošší formy a začnou vysílat panožky (pseudopodie) ve směru pohybu. Panožky jsou homogenní, cytoplazma je granulovaná. Pozorujte, nakreslete a popište princip améboidního pohybu.
Úkol 5: Bičíkový pohyb
NP: spermie, senný nálev/video
Kápněte spermie z inseminační dávky (v médiu androhep) na nahřáté podložní sklíčko a pozorujte pohyb spermií a to směrem dopředu a rotaci kolem osy (mění se šířka hlavičky, bičík je na zadním konci buňky, buňku tlačí před sebou). Obdobně lze pozorovat bičíkový pohyb u bičíkovců v NP zhotoveném ze senného nálevu (většina volně žijících bičíkovců má bičík na přední části buňky, bičík táhne buňku za sebou). Pro zpomalení nálevníků odsajte část vody pod sklíčkem pomocí filtračního papíru.
Úkol 6: Struktura příčně pruhovaného svalu
TP: příčně pruhovaný sval z končetiny hmyzu obarvený Heidenheinovým hematoxylinem a příčně pruhovaný sval potkana obarvený haematoxylin-eosinem
Pozorujte oba typy preparátů a zakreslete příčné pruhování svaloviny, které je způsobené rozdílnou barvitelností svalových vláken. Vysvětlete princip svalového pohybu.
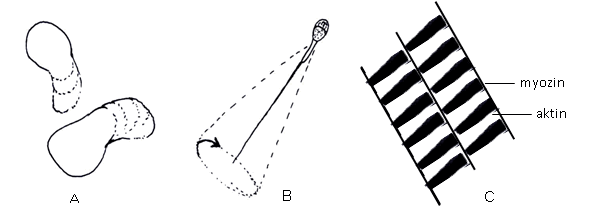
A – améboidní pohyb, B – bičíkový pohyb, C – příčně pruhovaný sval hmyzu.
Úkol 7: Oxygenotaxe u nálevníků
NP: senný nálev
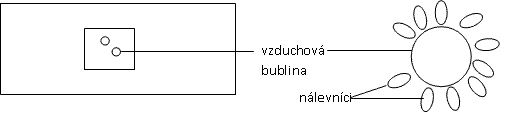
Připravte nativní preparát ze senného nálevu a přikryjte krycím sklíčkem tak, aby pod sklíčkem vznikly vzduchové bubliny. Nálevníci vyhledávají prostředí s optimální tenzí kyslíku a začnou se shromažďovat v okolí bublin. Stejný jev je možné pozorovat při okrajích krycího sklíčka. O jakou oxygenotaxi se jedná? (pozitivní nebo negativní)
Vyšetření krve
Metody vyšetření krve a jejich využítí
HEMATOLOGICKÉ VYŠETŘENÍ
Krevní obraz (KO) – poskytuje údaje o počtu krevních elementů (erytrocyty, leukocyty, trombocyty), množství krevního barviva (hemoglobin) a hematokritu (procentuální podíl erytrocytů na objemu krve). Diferenciální rozpočet slouží ke stanovení počtu jednotlivých druhů bílých krvinek (neutrofilní, eozinofilní, bazofilní, monofilní, lymfocyty, monocyty atd.). Používá se při screeningu, krevních chorobách a zánětlivých onemocněních.
Sedimentace erytrocytů (FW - podle Fahrea a Westergreena) – použití při screeningu, zánětlivých, infekčních a nádorových onemocněních.
Quick test – určuje protrombinový čas, použití při léčbě koagulancii.
APTT (aktivovaný parciální tromboplastinový čas) – slouží ke zjištění koagulačních faktorů IX, XI, XII pro vnitřní srážení, použití při heparinizaci, léčbě streptokinázou a u hemofilie.
Krvácivost (srážlivost) – použití při krvácivých chorobách a předoperačních vyšetřeních.
Určení krevní skupiny a Rh faktoru
Coombsův test – slouží k rozpoznání imunohemolytické reakce při inkompatibilitě Rh faktoru dítěte a matky.
BIOCHEMICKÉ VYŠETŘENÍ
Ionty (ionogram nebo mineralogram) – stanovení koncentrace elektrolytů v krvi (Na, K, Ca, P, Mg, Fe atd.). Použití: součást screeningu, rozvrat vnitřního prostředí, poruchy činnosti ledvin, šok, zvracení, průjmy, poruchy srdeční činnosti.
Metabolity – produkty metabolismu (např. urea, kreatinin, bilirubin).
Bílkoviny – stanovujeme celkovou bílkovinu, albuminy, imunoglobuliny. Použití: posouzení stavu výživy, imunity nebo sledování vývoje zánětu.
Enzymy – např. transaminázy (ALT, AST, ALP), GMT, LDH, CK a amylázy. Použití: onemocnění jater, žlučových cest, pankreatu, kosterních svalů apod.
Lipidy – např. cholesterol, triglyceridy.
Hormony – např. TSH, T3, T4, aldosteron, progesteron, apod.
Tumorové markery – např. alfafetoprotein, CA, CEA, PSA.
Léky – např. Digoxin, Phenobarbital, atd.
Speciální metabolity – např. vit. A, B6, B12, C, D apod.
Toxiny – např. alkohol.
stanovení glykémie
stanovení acidobazické rovnováhy
MIKROBIOLOGICKÉ VYŠETŘENÍ
bakteriologické – hemokultura
mykologické – plísně
virologické – viry
parazitologické – paraziti
SÉROLOGICKÉ VYŠETŘENÍ
Těmito vyšetřeními se stanoví hladiny některých protilátek, které vznikají jako odpověď na infekční agens (viry, bakterie a parazity). Příkladem je stanovení C-reaktivního proteinu (CRP), jehož koncentrace zejména při bakteriálních infekcích prudce stoupá.
Měření velikosti mikroskopických objektů
Měření velikosti objektu se provádí běžným mikroskopem, do jehož okuláru se vloží okulárový mikrometr. Je to kruhová, skleněná destička, na níž je vyryta 1 cm dlouhá úsečka rozdělená na 100 dílků po 0,1 mm. Okulárovým mikrometrem se provádí vlastní proměřování objektu. Jak velké dílky okulárového mikrometru se skutečně jeví v mikroskopu, lze zjistit porovnáním s jiným přesným měřidlem pozorovatelným celou optickou soustavou mikroskopu. K tomuto účelu slouží objektivový mikrometr, což je krycí sklo (přitmelené kanadským balzámem na podložní sklo), na kterém je vyryta 1 mm dlouhá úsečka rozdělená na 100 dílků, takže 1 dílek odpovídá 10 µm. Na začátku měření je nejdříve potřebné zjistit tzv. mikrometrický koeficient, tj. jaké hodnotě odpovídá jeden dílek okulárového mikrometru. K tomuto stanovení slouží okulárový mikrometr v jednom z okulárů a objektivový mikrometr, který se umístí na stolek mikroskopu a zastaví se jako běžný preparát. Otáčením okuláru s okulárovým mikrometrem se dají obě měřítka do takové polohy, aby byla vzájemně rovnoběžná. Potom se posouvá objektivovým mikrometrem tak, aby se jeho počáteční ryska kryla s počáteční ryskou okulárového mikrometru. Poté se hledá libovolný dílek objektivového měřítka, který se překrývá s dílkem okulárového měřítka (nejjednodušší je vzít pravý okraj kratšího měřítka a odečíst odpovídající hodnotu na okulárovém měřítku), hodnoty dílků se zaznamenají. Měření je potřebné provést pro všechna zvětšení objektivů. Při použití menších zvětšení je třeba hodně clonit a před přechodem na větší zvětšení (hlavně ze 40× na 100×) umístit objektivové měřítko do středu zorného pole, aby se neztratilo. Je třeba také počítat s tím, že objektivové měřítko se při větších zvětšeních také úměrně zvětšuje (pokud si nejste jisti, které měřítko je které, tak při otočení okulárem se otočí okulárový mikrometr).
Hodnota jednoho dílku okulárového mikrometru (mikrometrický koeficient) se vypočítá vydělením počtu dílků odečtených na objektivovém mikrometru počtem dílků odečtených na okulárovém mikrometru. Je nutné stanovit mikrometrický koeficient zvlášť pro jednotlivá zvětšení objektivů.
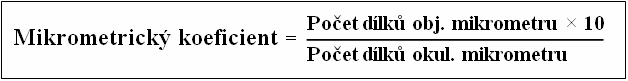
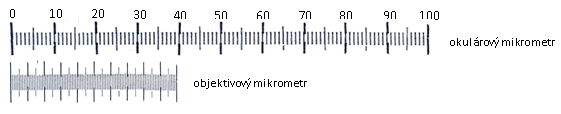
Obr.: Příklad stanovení mikrometrického koeficientu pro zvětšení objektivu 4× (100. dílek objektivového mikrometru odpovídá 40. dílku okulárového mikrometru – do vzorce pro mikrometrický koeficient dosadíme 100×10/40 = 25 µm).
Mikrometrické koeficienty pro různé objektivy: 25 (4×), 10 (10×), 2,5 (40×), 1 (100×)
Při vlastním měření mikroskopického objektu se umístí preparát na stolek mikroskopu a zjistí se, kolika dílkům okulárového mikrometru odpovídá měřený objekt. Tento počet dílků se vynásobí mikrometrickým koeficientem pro daný objektiv a výsledek se vyjádří v µm.
Transport látek, osmotické jevy (živočišná buňka)
Buňka, jako otevřená soustava, může žít jen za stálé výměny látek, energie a informací se svým okolím. Hlavní strukturou regulující buněčný příjem a výdej látek je cytoplazmatická membrána, která je polopropustná (semipermeabilní). Svou selektivní propustností zajišťuje, že koncentrace látek uvnitř buňky jsou udržovány na úrovni optimální pro život buňky. Mezi mechanizmy transportu látek přes membránu patří:
PŘÍMÁ (PROSTÁ) DIFUZE – závisí na fyzikálních vlastnostech membrány, která je propustná pro nízkomolekulární látky např. plyny, uhlovodíky, organické kyseliny, močovinu, etanol a vodu. Difuze závisí na rozdílu koncentrace daných látek uvnitř a vně buňky tj. na koncentračním spádu, teplotě a velikosti molekul. Difuze probíhá tak dlouho, až se koncentrace na obou stranách membrány vyrovnají. Zvláštním případem difuze je osmóza.
OSMÓZA – souvisí s polopropustností membrány, tzn. vodu propouští snadno, ale nepropouští látky ve vodě rozpuštěné. Je-li buňka obklopena izotonickým roztokem (roztokem o stejné koncentraci, jakou má cytoplazma), k průchodu vody membránou nedochází. Osmotické jevy nastanou tehdy, je-li buňka obklopena roztokem hypotonickým (o nižší koncentraci než má cytoplazma) nebo hypertonickým (o vyšší koncentraci než má cytoplazma).
Živočišná buňka:
- Hypotonické prostředí - do buňky začne proudit voda (endosmóza vody), buňka zvětšuje svůj objem, až praskne. Jev se obecně označuje jako plazmoptýza, u červených krvinek jako osmotická hemolýza.
- Hypertonické prostředí - z buňky začne proudit voda ven (exosmóza) a buňka se začne svrašťovat. Někdy se tento jev označuje jako plazmorhiza.
TRANSPORT POMOCÍ MEMBRÁNOVÝCH TRANSPORTNÍCH PROTEINŮ - specifický transport větších nenabitých polárních molekul (aminokyseliny, nukleotidy, cukry) a iontů (H+, Na+, K+, Ca2+, Mg2+, Cl-, HCO3-) pomocí kanálových proteinů, které vytváří póry (iontové kanály) pro difuzi rozpuštěných látek, nebo pomocí přenašečových proteinů na základě změny konformace (funkce turniketu).
ENDOCYTÓZA - příjem kapalin a různě velkých částic vchlípením plazmatické membrány a následnou tvorbou endocytotických váčků, které jsou přesouvány do lyzosomů, kde jsou stráveny. Příjem rozpuštěných látek se označuje jako PINOCYTÓZA, příjem pevných částeček je FAGOCYTÓZA.
EXOCYTÓZA – výdej kapalin a různě velkých částic buňkou.
Určování krevních skupin
KREVNÍ SKUPINY U LIDÍ
Krevními skupinami (KS) obecně rozumíme všechny
antigeny na membránách erytrocytů, které jsou schopné vyvolat tvorbu protilátek.
Jedná se o proteiny (receptory, enzymy či transportní proteiny), glykoproteiny
či oligosacharidy. Tyto antigeny se obvykle označují jako aglutinogeny.
Protilátky (aglutininy) se v krevním oběhu vyskytují buď přirozeně,
nebo je jejich tvorba vyvolána průnikem krvinek jiné KS do krevního oběhu.
Shlukování krvinek v přítomnosti příslušných protilátek proti daným
antigenům se označuje jako aglutinace a využívá se pro rychlé
orientační stanovení KS. U člověka je známo více než 30 systémů krevních skupin.
Mezi nejvýznamnější patří systémy AB0, Rh či MNS.
V systému AB0 rozeznáváme čtyři základní krevní skupiny: A,
B, AB a 0. Tento systém je nejstarší a nejvýznamnější. Jako první jej popsal
rakouský vědec a lékař Karl Landsteiner v roce 1901 (a za tento objev
dostal v roce 1930 Nobelovu cenu za medicínu). Landsteiner však popsal
pouze tři krevní skupiny, A, B a C (dnes 0). Nezávisle na něm dospěl v roce
1907 ke stejnému objevu rovněž český lékař Prof. MUDr. Jan Janský. Ten
ovšem správně identifikoval a klasifikoval všechny čtyři krevní skupiny, které
sám označoval I, II, III a IV. Jedinci krevní skupiny A nesou na svých krvinkách
aglutinogen A a tvoří protilátky anti-B, skupina B nese aglutinogen B a
protilátky anti A. Skupina AB má oba aglutinogeny a žádné protilátky, skupina 0
nemá aglutinogeny (je přítomen jen jejich prekurzor) a tvoří protilátky proti
oběma aglutinogenům.
Krevní skupina
Aglutinogen
Protilátky
A
A
anti-B
B
B
anti-A
AB
A, B
-
O
-
anti-A, anti-B
Při transfúzi krve odlišné krevní skupiny hrozí akutní hemolýza: rychlá destrukce darovaných krvinek protilátkami příjemce a jejich následné odbourání prostřednictvím makrofágů a retikuloendoteliálním systémem.
URČOVÁNÍ KREVNÍCH SKUPIN U LIDÍ
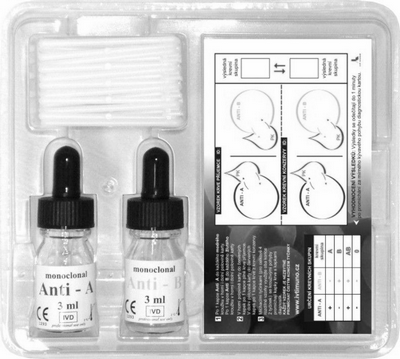 K určení krevních skupin u lidí se používá "diagnostická souprava pro určování krevních skupin systému ABO (monoklonální)". Tato souprava obsahuje monoklonální Anti-A, monoklonální Anti-B, diagnostické karty a tyčinky k promíchání diagnostik s krevními vzorky.
K určení krevních skupin u lidí se používá "diagnostická souprava pro určování krevních skupin systému ABO (monoklonální)". Tato souprava obsahuje monoklonální Anti-A, monoklonální Anti-B, diagnostické karty a tyčinky k promíchání diagnostik s krevními vzorky.
Princip testu: aglutinační reakce, která je založena na reakci mezi antigenem (na povrchu erytrocytů) a protilátkou (reagencie v testu).
Postup: Do každého modrého kroužku karty se kápne po 1 kapce monoklonálního diagnostika Anti-A. Do každého žlutého kroužku se kápne po 1 kapce monoklonálního diagnostika Anti-B. Do červeného kroužku se kápne po 1 kapce krve (po píchnutí do prstu tenkou jehlou stisknout prst a vymáčknout kapku krve). Přiloženými tyčinkami se promíchají kapky monoklonálních diagnostik s kapkami krve a to každý vzorek samostatným koncem tyčinky.
Hodnocení: Výsledky se odečítají do 1 minuty po promíchání za mírného kývavého pohybu diagnostickou kartou.
Reakce s diagnostikem
Krevní skupina
Anti-A
Anti-B
+
-
A
-
+
B
+
+
AB
-
-
O
- Pozitivní reakce (aglutinace) indikuje přítomnost odpovídajícího antigenu na erytrocytech.
- Negativní reakce (bez viditelné aglutinace) indikuje chybění odpovídajícího antigenu na erytrocytech
- Příslušná krevní skupina se určí podle následující tabulky
Krevní skupiny v populaci lidí v ČR:
- A (45%)
- 0 (30 – 35%)
- B (15 – 20%)
- AB (5 – 7%)
Kontrolní otázky – vyšetření krve
- Co se používá k panoptickému barvení (dle Pappenheima) krevního nátěru?
- Jaký je rozdíl mezi ptačím a savčím erytrocytem (velikost, tvar a přítomnost jádra)?
- Jak se provádí měření velikosti mikroskopického objektu?
- K čemu slouží mikrometrický koeficient?
- Umíš nakreslit a popsat membránu (model tekuté mozaiky)?
- Jaké jsou způsoby transportu látek přes membránu?
- Jaký je rozdíl mezi endocytózou, exocytózou, pinocytózou a fagocytózou?
- Co je to osmóza?
- Jaké typy prostředí v souvislosti s osmotickými jevy rozlišujeme?
- Co se stane s živočišnou buňkou v hypotonickém, hypertonickém a izotonickém prostředí?
- Co znamená plazmoptýza a plazmorhiza?
- Co je to hemolýza?
- Jak vypadá hemolýza makroskopicky a mikroskopicky?
- Jaký je princip určování krevních skupin u lidí?
- Jaké jsou krevní skupiny u lidí (která skupina je nejčastější a která je vzácná)?
ÚKOLY - Vyšetření krve (viz úkoly)
Vyšetření krve
Úkol 1: Příprava trvalého preparátu suchou cestou – krevní nátěr
krev
K jedné straně odmaštěného podložního skla kápněte malou kapku nesrážlivé krve. Před kapku krve přiložte pod úhlem 45o podložní sklo se zabroušenými rohy a nechejte krev roztéct podél hrany sklíčka a poté plynulým tahem rozetřete kapku po podložním skle (kapka krve se táhne za sklíčkem). Krevní nátěr musí být tenký, rovnoměrný, asi do 2/3 podložního sklíčka. Několikrát postup opakujte, až se vám podaří zhotovit kvalitní krevní nátěr, který nechte zaschnout a prohlédněte pod mikroskopem.
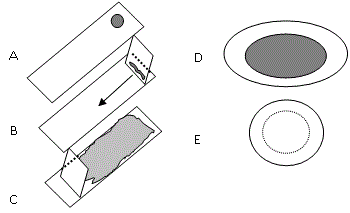
Obr.: Postup zhotovení krevního nátěru: A – kápnutí kapky krve na podložní sklo, B – přiložení krycího skla před kapku krve pod úhlem 45°, C – zhotovení krevního nátěru, D – ptačí erytrocyt (oválný, s jádrem, větší), E – savčí erytrocyt (kulatý, bikonkávní, bez jádra, menší)
Úkol 2: Barvení krevního nátěru (panoptické barvení dle Pappenheima)
krev, May-Grünwald, Giemsa-Romanowski
Zhotovte krevní nátěr (viz předchozí úkol). Po zaschnutí převrstvěte preparát barvivem May-Grünwald a nechejte působit 5 min., poté přidejte destilovanou vodu a opět nechejte 5 min. působit. Slijte a převrstvěte barvivem Giemsa-Romanowski. Po 10 min. slijte, opláchněte destilovanou vodou a k preparátu opatrně přiložte filtrační papír k odsátí zbytků vody. Po odstranění filtračního papíru nechte nátěr zaschnout. Prohlédněte si obarvený krevní nátěr, v kterém můžete kromě erytrocytů pozorovat i leukocyty s modře obarvenými jádry.
Úkol 3: Měření velikosti mikroskopických objektů
TP: ptačí erytrocyty, NP: savčí erytrocyty
Měření velikosti objektů se provádí pomocí okulárového mikrometru (měřítka), který je umístěn v jednom z okulárů. Při měření velikosti objektu je třeba zjistit, kolika dílkům okulárového mikrometru odpovídá měřený objekt. Tento počet dílků se vynásobí mikrometrickým koeficientem pro daný objektiv (každý objektiv má svůj koeficient) a výsledek se vyjádří v µm. Změřte velikost ptačích a savčích erytrocytů. Jaký je rozdíl mezi ptačím a savčím erytrocytem (velikost, tvar a přítomnost jádra)?
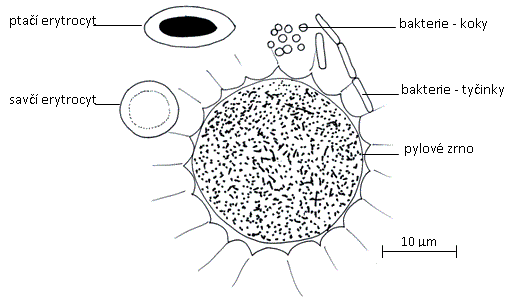
Obr.: Porovnání velikostí různých buněk.
Úkol 4: Hemolýza osmotická (makroskopicky)
krev, fyziol. roztok, voda
Do dvou zkumavek nalijte po 1 ml savčí krve. Do jedné ze zkumavek přidejte 3 ml fyziologického roztoku a do druhé stejné množství destilované vody. Mírně protřepejte a porovnejte obě zkumavky. Vysvětlete, k čemu v jednotlivých zkumavkách došlo a proč. Proveďte tzv. „čtecí zkoušku“ a výsledky zaznamenejte.
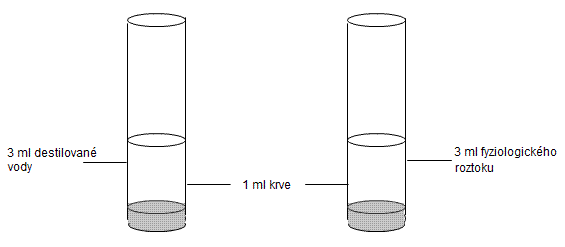
Úkol 5: Hemolýza osmotická (mikroskopicky)
krev, voda
Na podložní sklíčko naneste malou kapku krve a přikryjte krycím sklíčkem. K okraji sklíčka přikápněte kapku destilované vody. Pozorujte postupné ubývání erytrocytů způsobené jejich praskáním (prasklé erytrocyty jsou málo viditelné).
Úkol 6: Plazmorhiza
krev, 1M KNO3
Na podložní sklo naneste kapku krve a přikápněte k ní kapku 1M KNO3. Po přiložení krycího skla pozorujte a zakreslete krvinky svraštělé do hvězdicovitých útvarů, tzv. echinocyty (k této deformaci krvinek může dojít také např. v silných nátěrech, které pomalu vysychaly). Nakreslete a zapište závěr.
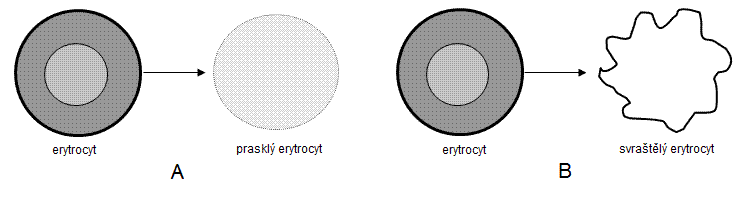
Obr.: Osmotické jevy u savčích erytrocytů: A – hemolýza, B – plazmorhiza.
Úkol 7: Fagocytóza
TP: fagocytující bílé krvinky, barvené Pappenheimovou metodou.
Prohlédněte si preparát, najděte a zakreslete bílé krvinky s fagocytovanými partikulemi. Spočítejte fagocytární aktivitu (FA): FA = počet fagocytujících buněk/počet počítaných buněk.
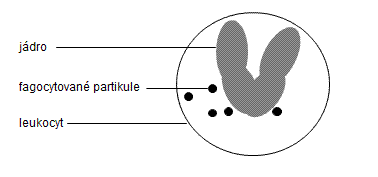
Obr.: Leukocyt s fagocytovanými partikulemi.
Úkol 8: Určování krevních skupin
Pomocí diagnostické soupravy pro určování krevních skupin systému ABO (monoklonální) si určete svoji krevní skupinu a zaznamenejte do protokolu.
Buněčný cyklus, mitóza
BUNĚČNÝ CYKLUS je sled pochodů probíhajících v buňce od skončení jedné mitózy do konce mitózy následující a má 4 fáze: G1 (z angl. "gap" - mezera), S (syntetická fáze), G2 a M (mitóza). První tři fáze se označují jako interfáze, která zaujímá 90 % času celého buněčného cyklu.
G1 buňka roste, probíhá v ní množení organel, syntéza proteinů, RNA a DNA polymerázy. Na začátku G1 fáze leží hlavní kontrolní bod. Diferencované nedělicí se buňky (nervové, svalové) přecházejí do klidové fáze označované jako G0.
S - jaderná DNA se replikuje (replikace mimojaderné DNA probíhá během celého cyklu s výjimkou mitózy), zdvojuje se počet chromozomů a centrozomů.
G2 - buňka opět roste a přibývá buněčných struktur.
M (MITÓZA) - slouží jak k budování mnohobuněčného organizmu, tak i k nepohlavnímu rozmnožování (u jednobuněčných a primitivnějších mnohobuněčných organizmů). Při mitóze dochází k rovnoměrnému rozdělení genetického materiálu, zdvojeného mechanizmem replikace DNA v predcházející S-fázi, do dvou dceřiných buněk, které jsou tak geneticky identické (klony).
Mitóza zahrnuje období vlastního dělení jádra (karyokineze) a dělení cytoplazmy buňky (cytokineze) a má 4-5 fází: profáze, (prometafáze - v mikroskopu těžko odlišitelná od jiných fází), metafáze, anafáze a telofáze.
Profáze - mizí jadérko, kondenzace (zviditelnění) chromozomů, centrozomy se rozchází k opačným pólům buňky a začíná se formovat dělicí (mitotické) vřeténko složené z pólů dělicího vřeténka (centrozomy) a mikrotubulů, vznik kinetochorů (komplex proteinů) v místě centromery na každé sesterské chromatidě chromozomu.
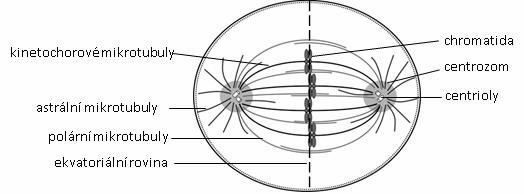
Obr.: Dělící vřeténko v živočišné buňce během metafáze.
Prometafáze - rozpad jaderného obalu, vazba mikrotubulů dělicího vřeténka na kinetochory.
Metafáze - seskupení chromozomů v ekvatoriální rovině buňky za pomoci mikrotubulů a molekulových motorů kinezinů.
Anafáze - přerušení spojení sesterských chromatid proteolytickými enzymy a jejich rozchod (segregace) k opačným pólům vřeténka pomocí molekulových motorů dyneinů a zkracováním mikrotubulů.
Telofáze - dekondenzace dceřiných chromozomů, vznik dvou jader s jaderným obalem a jadérky, zánik dělicího vřeténka.
Cytokineze - obvykle začíná již v anafázi, kdy se u živočišných buněk začíná v ekvatoriální rovině pod plazmatickou membránou formovat kontraktilní prstenec tvořený mikrofilamenty a molekulovým motorem myozinem II. Stahováním prstence dojde k rozdělení buňky a poté se kontraktilní prstenec rozpadne. U rostlin a hub se v cytokinezi uplatňuje přepážka fragmoplast, která je formována ze zbytků polárních mikrotubulů v ekvatoriální rovině buňky. K fragmoplastu jsou podél mikrotubulů transportovány váčky z Golgiho aparátu. Váčky se slévají a rostou směrem k buněčné stěně, až dojde k rozdělení buňky.
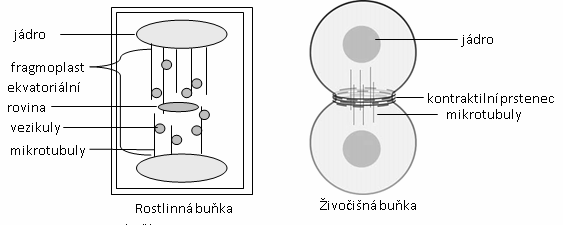
Obr.: Cytokineze u rostlinné a živočišné buňky.
PORUCHY MITÓZY vznikají vlivem mutagenů (např. hydrochinonu). Následkem těchto poruch může být:
- fragmentace chromozomů v profázi
- anafázový most - vzniká tak, že se sesterské chromatidy spojí v místě telomer (opakující se nukleotidová sekvence na konci chromatid) a při mitóze tak nedojde k jejich oddělení.
- anafáze u porušených chromozomů
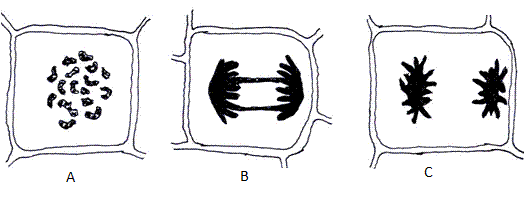
Obr.: Poruchy mitózy (A – fragmentace chromozomů v profázi, B – anafázový most, C – anafáze u porušených chromozomů).
Kontrolní otázky – buněčný cyklus, mitóza
- Jaké jsou fáze buněčného cyklu a co se děje v jednotlivých fázích?
- Jaké jsou fáze mitózy a co se děje v jednotlivých fázích?
- Co je to interfáze?
- Umíš nakreslit a popsat dělící vřeténko?
- Jak probíhá cytokineze u rostlinné a živočišné buňky?
- Jaké mohou být poruchy mitózy?
- Co je to anafázový most a jak vzniká?
- Co je to monaster?
ÚKOLY - Buněčný cyklus, mitóza (viz úkoly)
Buněčný cyklus, mitóza
Úkol 1: Mitóza v buňkách kořínku cibule
TP: kořínek cibule obarvený v acetorceinu
Mitóza u rostlinných buněk je mnohem výraznější než u buněk živočišných, jednotlivé chromozomy jsou po obarvení acetorceinem patrné a jsou vidět i mikrotubuly dělicího vřeténka. V preparátu najděte a zakreslete jednotlivé fáze mitózy a rovněž buňku v interfázi.

Obr.: Mitóza v buňkách kořínku cibule.
Úkol 2: Mitóza v tkáňové kultuře a mitotický index
TP: preparát z tkáňové kultury z ledvin králíka.
V preparátu najděte a zakreslete jednotlivé fáze mitózy, buňku v interfázi a tzv. monaster (buňka v metafázi při pohledu shora). V preparátu jsou patrné i poruchy mitózy jako je anafázový most.
V 5 zorných polích mikroskopu spočítejte buňky v mitóze a buňky v klidu a dosaďte do vzorce pro MI.
MITOTICKÝ INDEX udává frekvenci mitóz v živočišné tkáni nebo v rostlinném pletivu. Vyjadřuje podíl počtu buněk ve stádiu mitózy k celkovému počtu buněk.
MI (%) = M/N x 100 kde, M = počet buněk v mitóze, N = celkový počet buněk
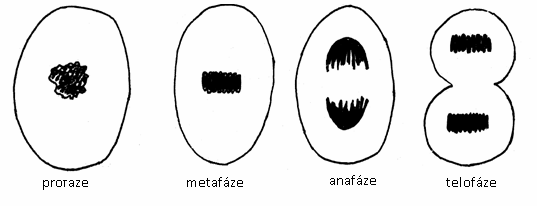
Obr.: Mitóza v živočišné buňce.
Úkol 3: Mitotické buňky v histologickém řezu tenkého střeva
TP: střevo laboratorního potkana barvené hematoxylin-eosinem
Preparát střeva prohlédněte nejdříve při malém zvětšení a zakreslete průřez střeva s vyznačením místa, kde budete hledat mitotické buňky. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy. Buňky v mitóze jsou větší se zaoblenými okraji, světlejší a místo jádra je možné pozorovat některou z mitotických figur.
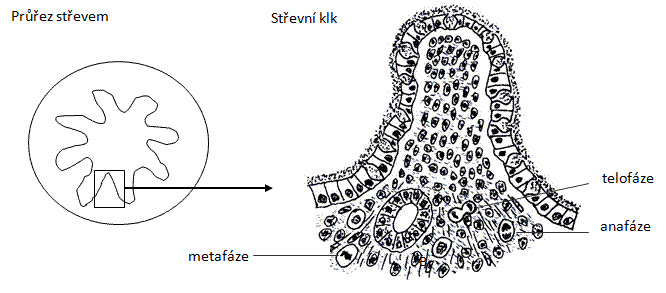
Obr.: Mitóza v epitelu tenkého střeva.
Úkol 4: Mitotické buňky v histologickém řezu dělohy
TP: děloha laboratorního potkana barvená hematoxylin-eosinem
Preparát prohlédněte nejdříve při malém zvětšení a zakreslete průřez dělohou s kubickým epitelem děložní sliznice, kde je možné najít buňky v mitóze. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy.
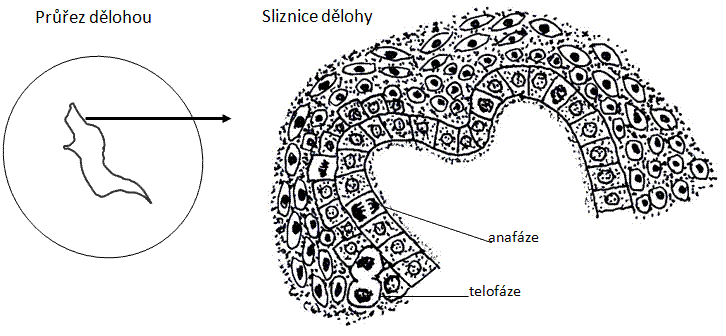
Obr.: Mitóza ve sliznici dělohy.
Úkol 5: Mitotické buňky v histologickém řezu varlat
TP: varle laboratorního potkana barvené hematoxylin-eosinem
Preparát prohlédněte a nakreslete nejdříve při malém zvětšení s vyznačením místa, kde budete hledat mitotické buňky, tj. na obvodu semenotvorných kanálků. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy.
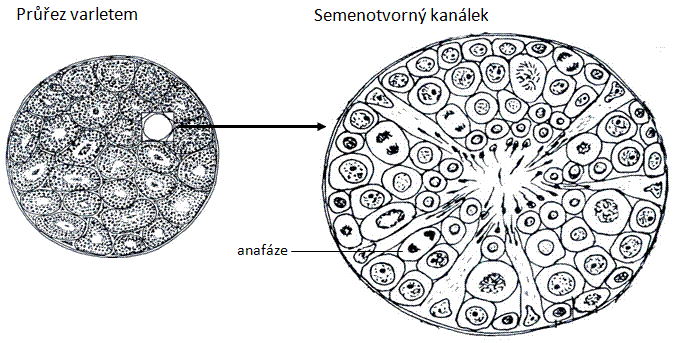
Obr.: Mitóza v semenotvorném kanálku varlete.
Rozmnožování a vývoj
NEPOHLAVNÍ (ASEXUÁLNÍ, VEGETATIVNÍ) ROZMNOŽOVÁNÍ je vznik nového jedince z jedné nebo většího počtu somatických buněk mateřského jedince. Genetická informace se přenáší nezměněná, všichni potomci jsou tedy stejní jako generace předchozí. Hlavními způsoby nepohlavního rozmnožování jsou dělení a pučení:
- Dělení (fisiparie) - dceřiní jedinci vznikají rozdělením mateřského jedince, který zaniká. Prvoci se dělí podélně (trypanosomy) nebo příčně (nálevníci). Známo je i mnohonásobné dělení, tzv. polytomie (např. při schizogonii, sporogonii, gamogonii u prvoků kmene Apicomplexa; nebo při schizogenezi (seriálním dělení) u živočichů, kdy se dceřiní jedinci začínají dělit dříve, než se sami oddělí od mateřského jedince a vzniká tak řetězec spojených jedinců (ploštěnky, mnohoštětinatci).
- Pučení (gemiparie) - na mateřském jedinci se vyvíjí pupen, který postupně dorůstá v dceřiného jedince (časté u přisedlých organizmů - houbovců, žahavců, mechovců).
POHLAVNÍ (SEXUÁLNÍ, GENERATIVNÍ) ROZMNOŽOVÁNÍ - nový jedinec se vyvíjí z jediné buňky (zygoty), která vzniká splynutím samčí a samičí pohlavní buňky (gamety). Gamety vznikají redukčním meiotickým dělením. U gonochoristů se tvoří samčí gamety v jiném jedinci než gamety samičí; u hermafroditů jsou gamety obojího typu tvořeny jedním jedincem.
MEIÓZA je proces (gametogeneze), který slouží ke vzniku pohlavních buněk. Meióza je jaderné dělení, při němž se jádro dvakrát dělí, ale dělení předchází pouze jedna syntetická fáze (syntéza jaderné DNA). V prvním dělení (též heterotypické, první zrací, redukční, meióza I) se rozcházejí homologní chromozomy (dvojchromatidové). Ve druhém dělení (též homeotypické, druhé zrací, ekvační, meióza II) se rozcházejí sesterské chromatidy (identické chromatidy se stejnou nukleotidovou sekvencí). Mezi dvěma děleními může být interkineze (obdoba interfáze u mitózy), ale bez S fáze.
Heterotypické dělení - počet chromozomů je redukován na polovinu (diploidní počet 2n se mění na haploidní počet chromozomů n). Má 4 fáze (profáze, metafáze, anafáze, telofáze):
-
PROFÁZE I - z celého meiotického dělení zaujímá až 90 %. Může trvat několik hodin, dní až roků. Při zahájení profáze I jsou již chromozomy zdvojeny (dvojchromatidové, obsahují 2 sesterské chromatidy, ke zdvojení došlo během S fáze). Během profáze I je možné rozlišit 5 fází:
Leptotene (časná profáze I, leptonema podle leptos = tenký) - chromozomy se začínají spiralizovat (začínají být viditelné), mají vzhled dlouhých jemných vláken. Začíná párování homologních chromozomů (nepohlavní chromozomy, obsahující stejné geny).
Zygotene (období mezi časnou a střední profází I, zygonema podle zygon = dvojitá nit) - homologní chromozomy (každý má 2 sesterské chromatidy) se přikládají těsně k sobě a vzniká tzv. bivalent složený ze 4 chromatid (= tetráda). Za vyhledání a navázání již maximálně kondenzovaných homologních chromozomů odpovídá tzv. synaptonemální komplex, tj. seskupení proteinů, které specificky rozezná příslušný chromozomový pár.
Pachytene (střední profáze I, pachytene podle pachynema = tlustý) - dochází k reciproké (vzájemné) výměně částí homologních chromozomů od otce a od matky (dochází k rekombinaci genetické informace). Tato výměna se označuje jako crossing-over a místa překřížení chromatid jako chiazmata (jednotné číslo chiazma). Synaptonemální komplex se rozpadá a chromozomy se více kondenzují (zkracují a ztlušťují).
Diplotene (střední až pozdní profáze I, diplonema podle diplos = dvojitý) - homologní chromozomy se od sebe oddělují (bez rekombinace nebo po rekombinaci vlivem crossing-overu).
Diakineze (pozdní profáze I, podle diakino = rozpojuji) - zaniká jaderná membrána a jadérko, vzniká dělicí vřeténko. - METAFÁZE I - homologní páry chromozomů se pomocí mikrotubulů dělícího vřeténka řadí v ekvatoriální rovině.
- ANAFÁZE I - dochází k segregaci chromozomů. Segregace je nezávislá, tj. náhodně se k pólům buňky rozchází homologní chromozomy (dvojchromatidové) původově od otce a od matky nebo rekombinované při crossing-overu. Tím dochází k druhé rekombinaci genetické informace, jejímž výsledkem je jádro vytvořené kombinací otcovských, mateřských a v crossing-overu rekombinovaných chromozomů.
- TELOFÁZE I - kolem dvou nových jader s haploidním počtem dvouchromatidových chromozomů se vytvoří nová jaderná membrána. Vzniknou 2 haploidní buňky (2 haploidní jádra) oddělené buněčnou přepážkou a telofáze heterotypického dělení přechází do profáze homeotypického dělení.
Homeotypické dělení - haploidní buňky se dělí jako při mitóze.
- PROFÁZE II - chromozomy se kondenzují, na konci profáze se diferencují 2 dělící vřeténka.
- METAFÁZE II - chromozomy zaujmou polohu v ekvatoriální rovině.
- ANAFÁZE II - dochází k podélnému rozštěpení centromer a k rozchodu sesterských chromatid dceřiných chromozomů k pólům dělicího vřeténka.
-
TELOFÁZE II - tvoří se jaderná membrána kolem každé sady chromozomů. Následuje cytokineze, chromozomy se despiralizují a přestávají být viditelné.
Produktem meiózy výchozí mateřské buňky s diploidním počtem dvouchromatidových chromozomů je čtveřice gamet s haploidním počtem jednochromatidových chromozomů. Studium a pochopení průběhu meiózy se uplatňuje v cytogenetice.
SPERMIOGENEZE (spermatogeneze) je vznik a vývoj spermií ve varleti. Spermatogonie se mitoticky dělí na spermatocyty I. řádu (primární spermatocyt), které vstupují do prvého meiotického dělení za vzniku spermatocytů II. řádu (sekundární spermatocyt). Po druhém meiotickém dělení vznikají čtyři spermatidy, které se následně diferencují ve spermie. Diferenciace spermií (ztráta většiny cytoplazmy a vytvoření bičíku) se děje až po ukončení meiózy, kdy jsou buněčná jádra haploidní a buňky ukončily cytokinezi. Spermiogeneze je zahájena v době pohlavní dospělosti a trvá asi 74 dnů.
OOGENEZE je vznik a vývoj vajíček ve vaječníku. Vajíčka vznikají z diploidních zárodečných prapohlavních buněk (primordiální gonocyty), které osídlily vaječník a staly se z nich oogonie. Ty se mitoticky dělí a vznikají primární oocyty (oocyty I. řádu), které vstupují do meiózy (u člověka v 7. měsíci nitroděložního vývoje) a zastaví se v profázi prvého meiotického dělení (u ženy to je do 12-45 let). Během této doby primární oocyt roste až na konečný průměr 100 µm, pomocí endocytózy a folikulárních buněk (pomocné buňky obalující vajíčko) se v nich hromadí žloutek jako materiálová a energetická rezerva. Gonadotropní hormon vylučovaný z hypofýzy (folikulostimulační hormon, FSH) navodí v buňkách folikulů tvorbu pohlavních hormonů (estrogenů), které indukují pokračování zrání primárního oocytu. V pohlavní dospělosti pokračuje oogeneze. Ve 28 denních cyklech vzniká z primárního oocytu sekundární oocyt (oocyt II. řádu) a první pólové tělísko. Sekundární oocyt se zastaví v metafázi druhého meiotického dělení, kde setrvá až do oplození. Po oplození dokončí sekundární oocyt druhé meiotické dělení a vznikne vajíčko a druhé pólové tělísko. Vajíčko se začne rýhovat, pólová tělíska zanikají.
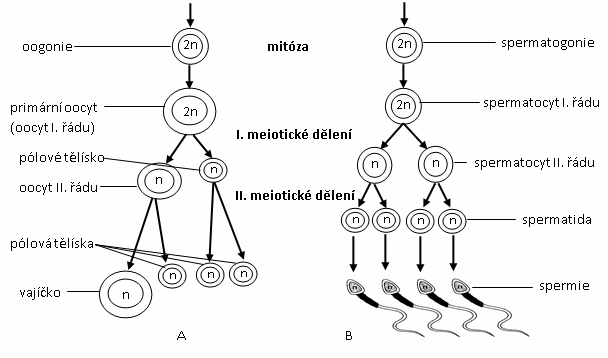
Obr.: A – schéma průběhu oogeneze, B – schéma průběhu spermiogeneze.
ESTRUS (říje) - dozrávání a uvolňování samičích gamet u savců probíhá opakovaně v tzv. estrálním cyklu. Rozlišujeme 4 fáze, pro něž je charakteristický mikroskopický nález ve stěru z poševní sliznice. Pro proestrus jsou typické epiteliální buňky s malým dobře barvitelným jádrem (v této době dozrává vajíčko ve vaječníku uvnitř folikulu, který je tvořen folikulárními buňkami, které produkují hormon estrogen); v estru převládají bezjaderné zrohovatělé epiteliální buňky (dochází k uvolnění zralého vajíčka z Graafova folikulu = ovulace); v metestru je možné najít buňky s velkými jádry a hlen (děložní sliznice se připravuje na případné zahnízdění oplozeného vajíčka, vzniká žluté tělísko "corpus luteum", které produkuje hormon progesteron); v diestru převládá hlen a leukocyty (dochází k vyloučení neoplozeného vajíčka).
Monoestrická zvířata - říje (estrus, ovulace) probíhá jednou ročně (např. vlk, jelen).
Deiestrická zvířata - říje probíhá dvakrát do roka (např. pes).
Polyestrická zvířata - říje probíhá několikrát do roka (např. hlodavci, zajíc, mnozí domestikovaní savci).
UTAJENÁ BŘEZOST je prodloužení doby mezi pářením a porodem pozastavením vývoje zárodku zpravidla na konci rýhování ve stadiu blastocysty (některé kunovité a medvědovité šelmy, pásovci, srna aj. savci).
UTAJENÉ OPLOZENÍ - páření proběhne určitou dobu před ovulací a spermie jsou po kopulaci uchovávány v pohlavních cestách samice až do ovulace (např. u netopýrů a některých ptáků).
INDUKOVANÁ OVULACE (provokovaná říje) - stimulem pro ovulaci je vlastní akt páření (např. králík, zajíc, myš, drobné šelmy), případně ztráta mláďat (lvi, hulmani - noví vůdčí samci záměrně zabíjejí "cizí", tedy ne svá mláďata = infanticida).
FYLOGENETICKÝ VÝVOJ je vývoj v historickém sledu, představující příbuzenské vztahy žijících i vymřelých organizmů.
ONTOGENETICKÝ VÝVOJ je individuální vývoj organizmu v průběhu jeho života od oplození vajíčka do dospělého stavu, případně až do jeho smrti. Probíhá ve dvou obdobích: embryonálním (prenatálním) a postembryonálním (postnatálním) (u savců bývá včleněno ještě tzv. období fetální).
NEPŘÍMÝ VÝVOJ ŽIVOČICHŮ je vývoj jedince přes stádium larvy. Larvy mají zpravidla jinou potravní základnu a žijí v jiném prostředí než dospělci. Primární larvy jsou upravená vývojová stádia (např. obrvená blastula), sekundární larvy jsou stavebně zcela odlišné (larvy hmyzu a pulci žab). U hmyzu má nepřímý vývoj 2 varianty:
- Proměna nedokonalá (hemimetabolie) - larvy se podobají dospělci, tj. imagu hmyzu (kobylky, ploštice, všenky aj.).
- Proměna dokonalá (holometabolie) - larvy se morfologicky i ekologicky liší od imaga, které vzniká metamorfózou (u hmyzu přes stádium kukly, např. motýli). Vyskytuje se také u obratlovců s vnějším oplozením, jako jsou ryby a obojživelníci.
PŘÍMÝ VÝVOJ ŽIVOČICHŮ - z oplozeného vajíčka se vyvíjí jedinec podobný dospělci až do vzniku pohlavně dospělého jedince. Podle odlišného vývoje rozlišujeme:
- Vejcorodost (oviparie) - mláďata se líhnou z vajíček uložených v prostředí mimo tělo matky (ptáci, hmyz, plazi, ryby, někteří savci).
- Vejcoživorodost (ovoviviparie) - vajíčka zůstávají v pohlavních vývodech matky a její tělo opouštějí larvy nebo juvenilní jedinci (některý hmyz, ryby, plazi, př. zmije obecná).
- Živorodost (viviparie) - vývoj zárodku uvnitř mateřského organizmu, kde je vyživován alespoň částečně z těla matky prostřednictvím placenty (savci).
APOMIXE je vývoj jedince z haploidní buňky - gamety. Příklady apomixe:
- Partenogeneze (řecky parthenos = panna) - vývoj jedince z neoplozeného vajíčka zcela bez účasti spermie (pavoukovci, hmyz, některé druhy ryb a ještěrů).
- Gynogeneze - vývoj vajíčka je aktivován spermií, jež poskytuje dělicí aparát, jádro spermie však zaniká a dalšího vývoje se neúčastní (hlístice, ploštěnky, vzácně ryby a ještěrky).
- Androgeneze (řecky andros = muž) - vývoj jedince ze samčí pohlavní buňky (pouze u rostlin).
Kontrolní otázky – rozmnožování a vývoj
- Jaký je rozdíl mezi nepohlavním a pohlavním rozmnožováním?
- Jak se liší mitóza od meiózy?
- K čemu slouží meióza a jaké jsou fáze meiózy?
- Jaké jsou fáze profáze prvního meiotického dělení?
- Co je to crossing-over a kdy k němu dochází?
- Co je to spermiogeneze?
- Umíš zakreslit schéma spermiogeneze?
- Co je to oogeneze?
- Umíš zakreslit schéma oogeneze?
- Jak dlouho trvá spermiogeneze a jak dlouho oogeneze?
- Co jsou to folikulární buňky a jaký hormon produkují?
- Co je to Graafův folikul?
- Co je to corpus luteum a jaký hormon produkuje?
- Jaké jsou fáze estrálního cyklu a co je pro ně typické?
- Jaký je rozdíl mezi ontogenezí a fylogenezí?
- Umíš nakreslit příklad fylogenetického stromu?
- Jaký je rozdíl mezi proměnou dokonalou a nedokonalou (uveď příklady)?
- Co je to apomixe?
ÚKOLY - Rozmnožování a vývoj (viz úkoly)
Rozmnožování a vývoj
Úkol 1: Spermiogeneze
TP: varle potkana barvené hematoxylin-eosinem.
Spermiogeneze probíhá v semenotvorných kanálcích varlat. Na příčném řezu semenotvorného kanálku jsou patrná jednotlivá vývojová stádia spermiogeneze. Prohlížejte kanálek směrem od periferie do středu kanálku a zakreslete jednotlivé typy buněk. Na periferii semenotvorného kanálku se nachází spermatogonie, menší buňky s jádrem bohatým na chromatin, směrem do středu kanálku se vyskytují spermatocyty I. řádu a spermatocyty II. řádu, které se liší velikostí buněk i typem jader. Blíže ke středu jsou spermatidy s malým množstvím chromatinu v jádrech, v centru kanálku jsou dozrávající spermie. V některých kanálcích převládá pouze určitý typ buněk, proto je důležité prohlédnout větší počet kanálků a zakreslit jednotlivá vývojová stádia buněk.
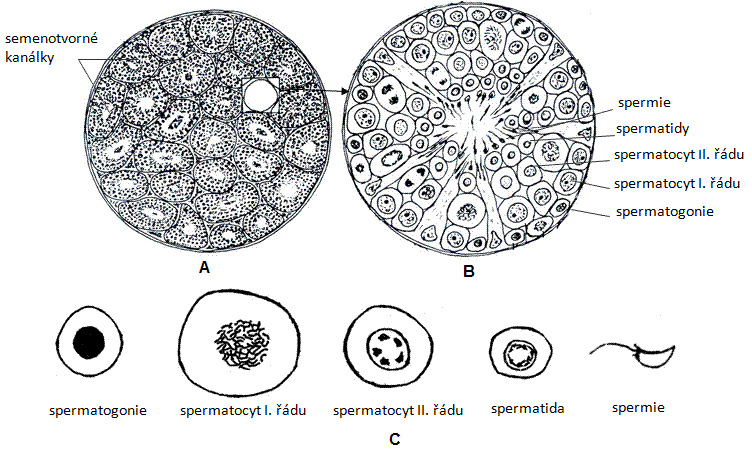
Obr.: Spermiogeneze ve varleti potkana: A – příčný řez varletem potkana, B – semenotvorný kanálek s jednotlivými buňkami spermiogeneze, C – vývojová řada spermiogeneze.
Úkol 2: Pozorování tvaru a velikosti spermií různých druhů zvířat
TP: spermie potkana, králíka, prasete a býka. Fotografie spermií dalších druhů živočichů.
Pozorujte a zakreslete v poměrných velikostech jednotlivé typy spermií lišících se počtem a délkou bičíků, tvarem hlavičky a velikostí akrozomu (struktura ve tvaru čepičky, která obklopuje přední polovinu hlavičky, obsahuje důležité enzymy, které umožňují pronikání hlavičky spermie do vajíčka).
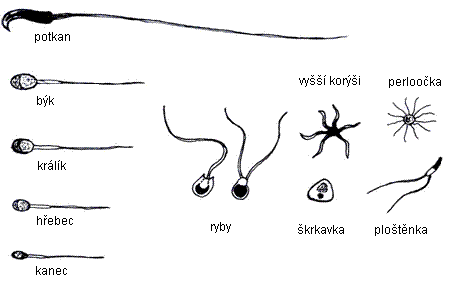
Obr.: Ukázky spermií různých živočichů v poměrných velikostech.
Úkol 3: Meióza
TP: obarvené podélné řezy varlat brouka smrtníka obecného (Blaps mortisaga).
Prohlédněte si v TP několik řezů varlat a hledejte jednotlivé fáze meiózy. Do protokolu zakreslete charakteristickou strukturu jader meiotické profáze I v chronologicky správném pořadí.
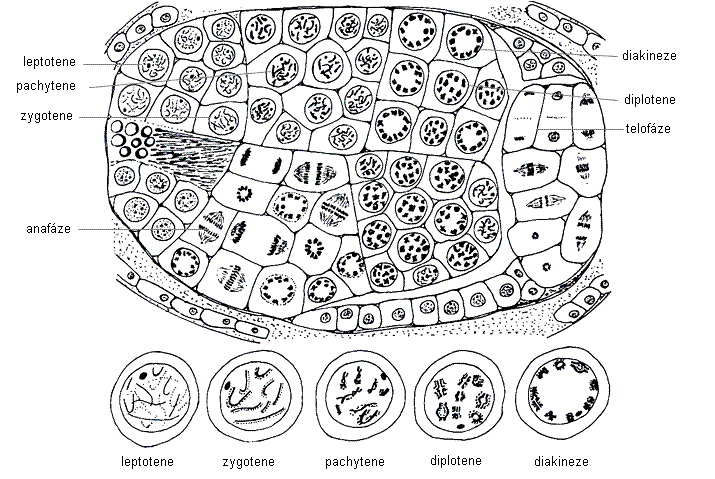
Obr.: Meióza v podélném řezu varlete brouka smrtníka obecného.
Úkol 4: Oogeneze
TP: ovarium potkana
Prohlédněte si preparát ovaria potkana. Najděte a zakreslete oocyt s několika folikulárními buňkami (tzv. primární folikul, tj. nezralý) a Graafův folikul, tj. zralý folikul obsahující zralý oocyt se zmnoženými folikulárními buňkami a dutinkami vyplněnými tekutinou.
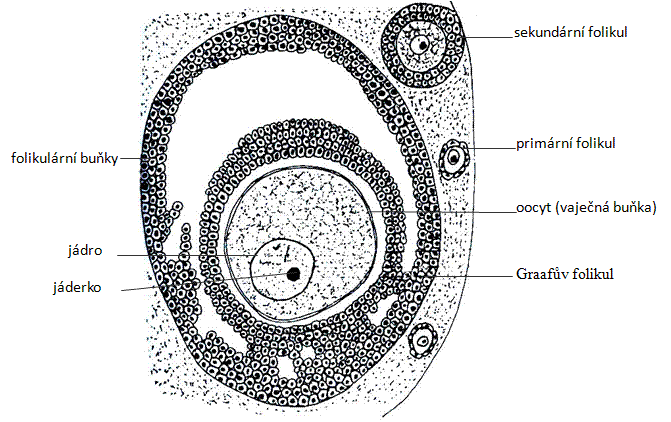
Obr.: Oogeneze ve vaječníku potkana.
Úkol 5: Cytologické změny vaginální sliznice v průběhu estrálního cyklu
TP: obarvené vaginální výtěry potkana v různých fázích estrálního cyklu
V každé fázi estrálního cyklu převládá charakteristický typ buněk. Pozorujte a zakreslete nálezy typické pro jednotlivé fáze estrálního cyklu.
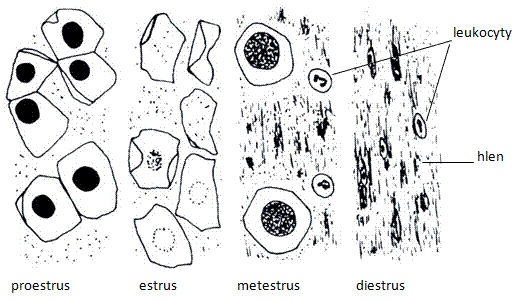
Obr.: Jednotlivé fáze estrálního cyklu s typickým nálezem ze stěru z poševní sliznice.
Úkol 6: Rýhování vajíčka králíka
TP: vajíčko obklopené folikulárními buňkami a vajíčko se 2 blastomerami. Fotografie vajíčka se 2 pólovými tělísky a vajíčka s 8 blastomerami.
Prohlédněte si trvalé preparáty a fotografie a zakreslete zralé vajíčko a jednotlivá stádia rýhování.
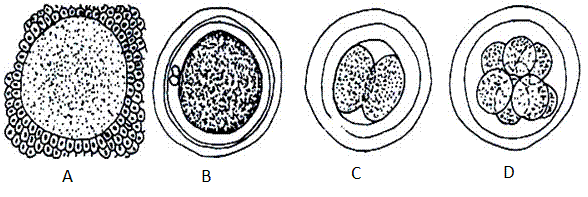
Obr.: Vajíčko králíka: A – neoplozené vajíčko, B – vajíčko po oplození, C – 2 blastomery, D – 8 blastomer.
Úkol 7: Pučení kvasinek
NP: suspenze kvasinek v kultuře
Zhotovte nativní preparát ze suspenze kvasinek. Pozorujte a zakreslete pučení, tj. vznik pupenu na pólu některých buněk, který se postupně zvětšuje a nakonec se odloučí od mateřské buňky.
Obr.: Pučení kvasinky.
Úkol 8: Vývoj jednotlivých druhů živočichů
TP: Hmyz s proměnou nedokonalou – (luptouš Menacanthus currucae nebo péřovka Degeeriela rufa). Kyvety s vývojovými stadii hmyzu s proměnou dokonalou (motýl bekyně velkohlavá Lymantria dispar), ryby (pstruh obecný Salmo trutta), obojživelníka (skokan hnědý Rana temporaria), ptáka (kur domácí Gallus gallus) a savců (potkan Rattus norvegicus, plod člověka Homo sapiens).
Prohlédněte si vývojová stádia hmyzu s proměnou nedokonalou (vajíčko, larva, nymfa II. a III. instaru, imago), hmyzu s proměnou dokonalou (vajíčko, larva, kukla, imago), ryby (jikra, zárodek, vykulený plůdek se žloutkovým vakem), obojživelníků (vajíčko, pulec, žába s pulčím ocáskem, žába), ptáků (vejce, embryo vyjmuté z vejce, kuře po vylíhnutí) a savců (děloha v raném a pozdním období gravidity, plod potkana).
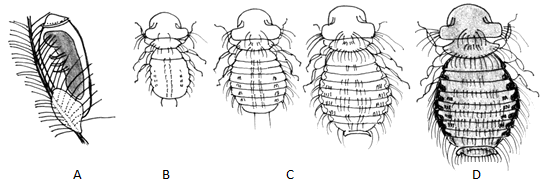
Obr.: Vývoj hmyzu s proměnou nedokonalou (všenka): A – vajíčko, B – larva, C – nymfa II. a III. instaru, D – imago (dospělec).
Modelový organizmus – Drosophila melanogaster
Drosophila melanogaster (octomilka obecná, drozofila, lidově banánová nebo vinná muška) patří do řádu Diptera (dvoukřídlí) a jejím původním domovem je Indo-malajská oblast. Kromě tohoto druhu se ve střední Evropě nachází přes 10 jiných druhů rodu Drosophila. Genetické studium u drozofil začalo r. 1909 v laboratoři T. H. Morgana v USA. Jedná se o genetický model, který byl použit z několika důvodů: snadný chov a křížení, krátká generační doba, početné potomstvo, existence mutantních kmenů a malý genom (bylo popsáno a analyzováno 13 600 genů, celý genom čítá asi 116 Mb, miliónů párů bází). Karyotyp 2n = 8, z toho 1. pár chromozomů jsou gonozomy (metacentrické, X je větší než Y), 2. – 4. pár chromozomů jsou autozomy (2. a 3. pár velké metacentrické, 4. pár velmi malé metacentrické).
Životní cyklus:
- vajíčko (1 den), bílé, velikost 0,5 mm
- první larvální stádium L1, 1. instar (1 den)
- druhé larvální stádium L2, 2. instar (1 den)
- třetí larvální stádium L3, 3. instar (2 dny)
- kukla (4 dny), zpočátku bílá, později hnědne.
- imago, dospělec (40-50 dnů), velikost 2-3 mm, samička se od samečka liší velikostí, tvarem a zbarvením hřbetní strany zadečku (na zašpičatělém zadečku má tmavé pruhování, zatímco sameček má na kulatém zadečku celistvou tmavou skvrnu). Pro křížení se vybírají neoplozené (virginelní) samičky, tj. asi 4-6 hod. po vylíhnutí. Tyto samičky jsou světlejší, mají protáhlý zadeček a někdy ne zcela rozvinutá křídla. Samičky jsou schopny se pářit za 12 hodin od vylíhnutí z kukly, samečci se mohou pářit již za několik málo hodin. Za 6-10 dnů od páření klade samička až 300 vajíček.
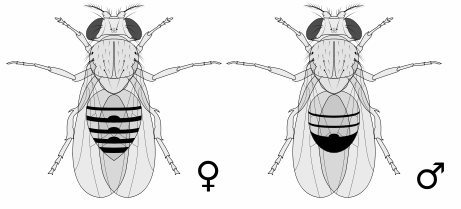
Obr.: Drosophila melanogaster – rozdíl mezi samečkem a samičkou
Laboratorní chov:
Mouchy se chovají v Erlenmeyerových baňkách při pokojové teplotě nebo v termostatu při 25 oC. Na dno baněk se nalije živné médium, které se připraví z kukuřičného šrotu, sušených kvasnic, cukru a agaru. Na živné médium se pokládá filtrační papír a po vpuštění drozofil do baněk se baňka uzavře vatovou zátkou.
Mutantní linie:
U drozofil je vyšlechtěna celá řada mutantních linií s rozdílnými geneticky založenými znaky (barva očí a těla, morfologie křídel). Mutantní alela se u drozofily značí symbolem s malým počátečním písmenem, je-li recesivní, což je většina (w "white" = bílé oči; y "yellow" = žluté tělo) a velkým písmenem, je-li dominantní (B "bar" = zúžené oči). Standardní alela se značí symbolem (+).
| Mutace | Symbol | Fenotyp |
|---|---|---|
| white | w | bílé oči |
| vestigial | vg | zakrnělá křídla |
| curly | cy | křídla zahnutá nahoru |
| yellow | y | žluté zbarvení těla |
| ebony | e | černé zbarvení těla |
| eyeless | ey | redukované oči |
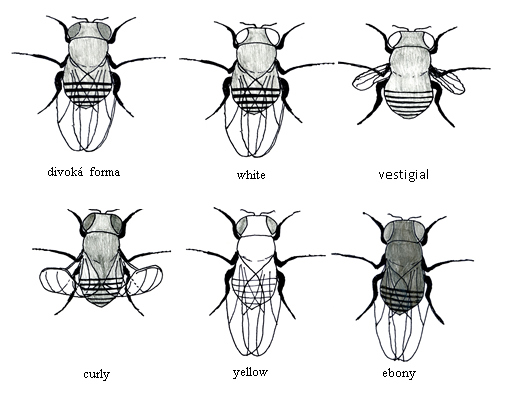
Obr.: Některé typy mutací u octomilky (Drosophila melanogaster) v porovnání s divokou formou.
modelový organismus Drosophila melanogaster
- Kdo používal octomilku ke svým experimentům?
- Proč se octomilky používají jako vhodný genetický model?
- Jaký je vývojový cyklus octomilky?
- Jaký je rozdíl mezi samcem a samicí octomilky?
- Kolik chromozomů má octomilka?
- Znáš příklady mutací u octomilek?
- Jak se dědí barva očí u octomilek?
ÚKOLY - Modelový organizmus – Drosophila melanogaster (viz úkoly)
Modelový organizmus
Úkol 1: Křížení drozofil s různě zbarvenýma očima
Drosophila melanogaster – samec a samice s různou barvou očí
Křížení původní (divoké) formy drozofily s červenýma očima a mutantní linie drozofily s bílýma očima. Jedná se o pokus, který bude probíhat během 3 cvičení:
1. cvičení - zahájení pokusu
Na cvičeních budete pracovat ve skupinách. Každá skupina dostane Erlenmeyerovu baňku s čerstvým živným médiem a 2 zkumavky s drozofilami vytříděnými podle pohlaví. Prohlédněte si obě zkumavky (někdo bude mít červenooké samečky a bělooké samičky, jiní zase červenooké samičky a bělooké samečky), všimněte si a zaznamenejte rozdíly mezi oběma pohlavími a různě zbarvených očí. Poté opatrně přesypte drozofily (samečky i samičky) do Erlenmeyerovy baňky, kterou si důkladně popište.
2. cvičení - odstranění dospělých drozofil z pokusu
Na vatu připevněnou zespodu uzávěru uspávací nádobky kápněte trochu éteru a nádobku uzavřete. Za chvíli nádobku otevřete a vytřepejte do ní mouchy z kultivační nádoby. Mouchy jsou během několika sekund znehybněny a můžete je přesypat do zkumavky.
3. cvičení - hodnocení výsledku pokusu
Pomocí éteru uspěte mouchy (potomky křížení) a roztřiďte je podle pohlaví a barvy očí a odvoďte, jak se tento znak dědí.
Úkol 2: Mutantní linie
Mutantní linie drozofil (white, yellow, ebony, curly, vestigial) - živé, v lihu a na obrázku.
Prohlédněte si jednotlivé mutantní linie drozofil a zakreslete.
Cytogenetika
CHROMOZOMY jsou pentlicovité útvary o velikosti 1-10 µm, které je možné pozorovat mikroskopem v dělicí se buňce. U eukaryot existuje více modelů struktury chromozomů (např. jednořetětězcové, víceřetězcové). Metafázický chromozom se skládá ze dvou chromatid, které jsou spojeny proteiny koheziny v místě primární konstrikce, tj. v místě centromery. Na základě polohy centromery se chromozomy dělí na metacentrické, submetacentrické, akrocentrické a telocentrické. Lidské chromozomy se rozdělují podle Denverské nomenklatury do sedmi skupin A až G podle jejich velikosti a uložení centromery. Chromozom je tvořen tzv. chromatinem tvořeným DNA, která je v trvalé vazbě s bazickými proteiny histony a dalšími kyselými proteiny. Podle intenzity barvení acetobarvivy, stupně kondenzace a intenzity transkripce se rozlišují dva druhy chromatinu: euchromatin (slabé barvení, malá kondenzace, transkripčně aktivní, přítomný v jádře inaktivní, pozorovatelný především při mitóze).
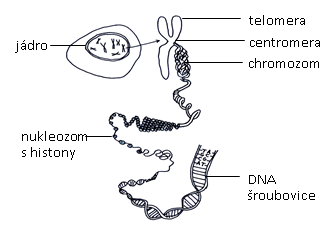
Obr.: Uložení DNA v buňce v podobě chromozomů
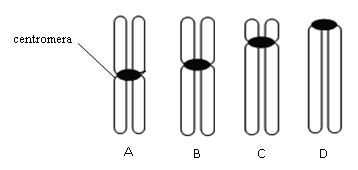
Obr.: Typy chromozomů podle polohy centromery (A – metacentrický, B – submetacentrický, C – akrocentrický, D – telocentrický).
Pohlaví jedinců většiny druhů s odděleným pohlavím (gonochoristů) je určeno pohlavními chromozomy (heterochromozomy, gonozomy). Ostatní chromozomy se označují jako somatické chromozomy (autochromozomy, autozomy). Diploidní buňky jedince homogametického pohlaví obsahují 2 stejné gonozomy, jedinec heterogametického pohlaví obsahuje dvojici rozdílných gonozomů, nebo jen jeden gonozom. V následující tabulce je uveden přehled počtu chromozomů, gonozomů a autozomů v tělních a pohlavních buňkách člověka.
| Buňka | Počet sad chromozomů | Celkem chromozomů | Gonozomy | Autozomy |
|---|---|---|---|---|
| Tělní (somatická) | 2 (2n) | 46 | 2 | 44 |
| Pohlavní (gameta) | 1 (2n) | 23 | 1 | 22 |
DETERMINACE POHLAVÍ U ŽIVOČICHŮ
-
Různý genetický základ u samce a samice (pohlavní chromozomy) – viz následující tabulka
Typ chromozomového určení pohlaví Samec Samice Zástupci Typ savčí (Drosophila) XY XX savci, většina řádů hmyzu, rostliny, některé ryby, někteří plazi, obojživelníci Typ ptakopysk X1Y1, X2Y2, X3Y3, X4Y4, X5Y5 X1X1, X2X2, X3X3, X4X4, X5X5 ptakopysk Typ ptačí
(Abraxas, systém ZW)ZZ ZW ptáci, motýli, některé ryby, někteří plazi, obojživelníci, ojediněle u rostlin Typ Protenor (systém XO) XO XX ploštice, rovnokřídlý hmyz Typ včela
(podle sad chromozomů)n 2n společenský hmyz - Stejný genetický základ u samce a samice (vliv prostředí, inkubační teplota) – u některých želv a krokodýlů má inkubační teplota vliv na pohlaví mláďat (při inkubační teplotě nižší než 28 °C se líhnou z vajec pouze samci, při teplotě 28 – 32 °C se líhnou samci i samice a při teplotě větší než 32 °C se líhnou pouze samice).
POLYTENNÍ CHROMOZOMY (mnohovláknové, mnohořetězcové, obrovské, gigantické) jsou chromozomy, které je možné najít v různých tkáních (slinné žlázy, buňky střevního epitelu a malpighických trubic) larev některého dvoukřídlého hmyzu, rovněž i u rostlin např. v endospermu kukuřice, v máku, oměji, pšenici a řeřiše. Polytenní chromozomy jsou zpravidla 50-200× delší než normální chromozomy, měří 200-600 µm a dosahují šířky až 25 µm. Každý polytenní chromozom se skládá z množství chromatinových vláken, která vznikla mnohonásobnou replikací a zůstávají spolu v paralelním uspořádání. Při barvení acetobarvivy vykazují lineární řadu střídajících se proužků (disků a meziproužků tmavší a světlejší barvy), což je způsobeno rozdílným barvením heterochromatinu a euchromatinu. Při aktivním fungování ztrácejí některé části polytenních chromozomů diskovité uspořádání, vznikají méně barvitelné vychlípeniny tzv. pufy (“puffs“, Balbianiho prstence), kde probíhá tvorba mRNA.
LYONIZACE, BARROVO TĚLÍSKO – u člověka a řady savců (např. kočka) u homogametického pohlaví (tedy samic), byla v nedělících se jádrech somatických buněk opakovaně prokázána přítomnost tzv. pohlavního chromatinu, který je podle svého objevitele označován jako Barrovo tělísko. Jedná se o 1 µm velký oválný útvar, který je ostře ohraničen a zpravidla bývá uložen při vnitřní straně jaderné membrány. Barrovo tělísko nelze obvykle prokázat ve všech buňkách (např. u žen se nachází ve 20 – 70% buněk ústní sliznice, u mužů se nachází v 0 – 3% buněk). Pohlavní chromatin je vlastně inaktivovaný chromozom X, který v interfázi zůstává spiralizován a je proto barvitelný. Většina genů inaktivovaného X chromozomu není geneticky aktivní, což počátkem 60. let zjistila M. F. Lyonová a tento jev (proces) byl nazván lyonizace. K irreverzibilní inaktivaci jednoho z chromozomů X dochází u savců již v rané fázi embryonálního vývoje. Trvání inaktivace nemusí být absolutní, kondenzovaný X chromozom může být reaktivován během tvorby vajíček. Vyšetření buněk na přítomnost pohlavního chromatinu se využívá k orientačnímu určování pohlaví u člověka.
CYTOGENETIKA je obor, který se zabývá studiem buněčných struktur nesoucích genetickou informaci. Pomocí cytogenetických metod se zjišťuje počet, tvar a struktura chromozomů a hledají se příčiny a následky jejich změn. Základní cytogenetickou metodou je chromozomová analýza, jejímž výsledkem je stanovení karyotypu. Materiálem pro vyšetřování chromozomů v somatických buňkách během mitózy jsou buňky kostní dřeně, choria, plodové vody, ale jako nejvhodnější se jeví lymfocyty z periferní krve. Mitotická aktivita lymfocytů se stimuluje fytohemaglutininem (extrakt z fazole), který se přidá do kultivačního média a buňky se kultivují v termostatu 72 hod. při 37 °C. Ke konci kultivace se do média přidává asi na 2 hod kolchicin, který poruší funkci dělicího vřeténka, zastaví dělení buněk v metafázi a tak vyvolá nahromadění metafázických buněk. Buňky jsou dále umístěny do hypotonického prostředí, fixovány, naneseny na podložní sklo a obarveny Giemsovým barvivem. Vhodné karyotypy se mohou vyfotografovat, jednotlivé chromozomy vystříhat a roztřídit podle velikosti, umístění centromery a uspořádání proužků a sestavit tak karyogram.
KARYOGRAM, IDIOGRAM je schématické grafické znázornění chromozomového souboru jednotlivých druhů organizmů.
KARYOTYP je sestava chromozomů zjištěná u konkrétního jedince. Každý chromozom v preparátech je tvořen sesterskými chromatidami.
EUPLOIDIE jsou změny počtu sad chromozomů př. triploidie (3n), oktoploidie (8n).
ANEUPLOIDIE jsou změny počtu jednotlivých chromozomů, např. monosomie (2n-1), trisomie (2n+1). Aneuploidie mohou u člověka způsobovat poruchy (syndromy) se specifickými příznaky. K nejčastějším syndromům patří:
Downův syndrom – trisomie chromozomu 21, u obou pohlaví (47,XX+21; 47,XY+21)
Edwardsův syndrom – trisomie chromozomu 18, u obou pohlaví (47,XX+18; 47,XY+18)
Pataův syndrom – trisomie chromozomu 13, u obou pohlaví (47,XX+13; 47,XY+13)
Turnerův syndrom – chybí chromozom X, jen u žen (45,XO; nebo 45,X)
Syndrom tří X (metafemale) – navíc chromozom X, u žen (47,XXX)
Klinefelterův syndrom – navíc chromozom X, u mužů (47,XXY)
Syndrom dvou Y (Jacobův syndrom, metamale) - navíc chromozom Y, u mužů (47,XYY)
BARVICÍ METODY (proužkovací, „banding“ metody) slouží k přesné identifikaci jednotlivých chromozomů a jejich aberací:
G pruhy – nejpoužívanější metoda, kdy se chromozomy vystaví účinku trypsinu, který denaturuje proteiny chromozomů, které se obarví Giemsovým barvivem. Na chromozomech vzniknou tmavé a světlé proužky (úsek chromozomu s převahou párů bází adenin-tymin se barví tmavě, úseky, kde převažují páry bází cytosin-guanin se barví světle).
FISH (fluorescence in situ hybridization) – využívá fluorescenční sondy ke specifickému barvení jednotlivých chromozomových párů. Je možné použít současně více sond (barev) k označení více párů chromozomů.
Kontrolní otázky – cytogenetika
- Čím se zabývá cytogenetika?
- Z čeho se skládá chromozom po chemické stránce?
- Jaké jsou typy chromozomů podle polohy centromery?
- Jaké jsou počty chromozomů (autozomů a gonozomů) v somatické a pohlavní buňce?
- Jak je determinováno pohlaví u různých skupin zvířat?
- Co je to polytenní chromozom?
- Co je to pohlavní chromatin (Barrovo tělísko) a jak vzniká?
- Jaký je rozdíl mezi trisomii a triploidii, jak se to dá zapsat?
- Z jakých buněk a jakým způsobem se dá zjistit karyotypy jedince?
- Umíš zapsat karyotyp člověka a domácích zvířat?
- Znáš příklady syndromů spojené s numerickou aberací? Umíš je zapsat?
- Jaká barvení se používají pro chromozomy?
ÚKOLY - cytogenetika (viz úkoly)
Cytogenetika
Úkol 1: Struktura polytenních chromozomů
TP: slinné žlázy larev pakomárů (Chironomus sp.) s obrovskými chromozomy.
Pozorujte buňky s polytenním chromozomem v buněčném jádru označovaném jako pentlicovité jádro. Pod větším zvětšením jsou na chromozomu patrné různě široké, odlišně se barvící okrsky, tzv. chromomery, které připomínají „čárový kód“. Dále jsou na chromozomu patrné zduřeniny, tzv. pufy. Zakreslete buňku slinných žláz s polytenním chromozomem.
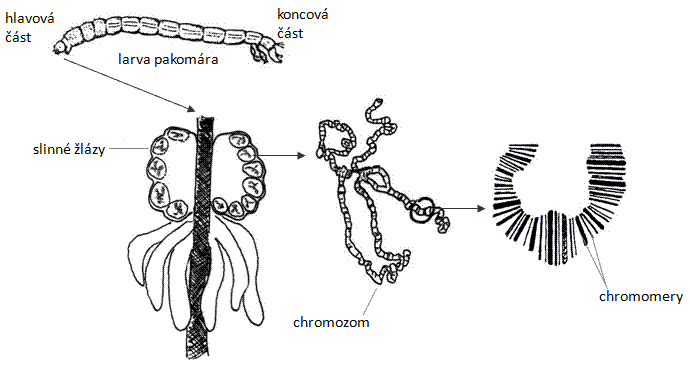
Obr.: Polytenní chromozom v buňkách slinných žláz z larev pakomára.
Úkol 2: Karyotypy savců
TP: karyotypy králíka (44), prasete (38), ovce (54), koně (64), skotu (60) a člověka (46) obarvené metodou podle Giemsy po předchozí kultivaci s kolchicinem.
V TP z krve jednotlivých zástupců savců hledejte chromozomy. Porovnejte počty a tvary chromozomů jednotlivých druhů savců na základě mikroskopického pozorování. Zakreslete alespoň jeden karyotyp. V čem je zvláštní karyotyp skotu?
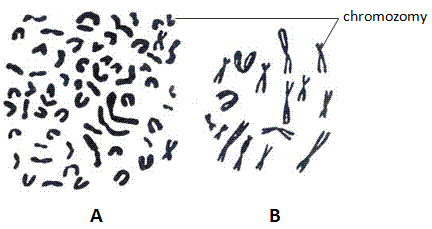
Obr.: Ukázka karyogramu: A – tur domácí (Bos taurus), B – cibule kuchyňská (Allium cepa).
Úkol 3: Zápis karyotypů
Pokuste se správně zapsat následující karyotypy:
- karyotyp zdravého muže a ženy
- karyotyp býka, klisny, berana
- karyotyp muže s Downovým syndromem a muže s Klinefelterovým syndromem
- karyotyp ženy s Edwardsovým syndromem a ženy s Turnerovým syndromem
Metody molekulární biologie
MOLEKULÁRNÍ BIOLOGIE je vědní disciplína zabývající se studiem buněčných biologických procesů na molekulární úrovni. Princip fungování některých biologických jevů je odhalitelný pouze studiem jejich molekulární podstaty. Molekulární biologie studuje strukturu biomakromolekul (DNA, RNA a proteinů), jejich vzájemné interakce a regulace jejich funkcí ve vztahu k funkcím a vlastnostem buňky. Molekulární biologie tak na jedné straně souvisí s biologií buňky, na straně druhé s biochemií a genetikou. Tento dynamicky se rozvíjející obor integruje ve svém přístupu hlediska biologická, chemická i fyzikální. Metody molekulární biologie zahrnují např. fyzikální a chemické separační a charakterizační metody, jako jsou chromatografie, elektroforéza, elektronová mikroskopie a spektroskopie. Molekulárně biologické metody jsou široce využívané nejen v základním a aplikovaném genetickém výzkumu nebo v genovém inženýrství, ale i v archeologii, zoologii, botanice, klinické medicínské diagnostice, kriminalistice nebo v soudním lékařství. K hlavním metodickým přístupům molekulární biologie patří purifikace a separace nukleových kyselin, amplifikace nukleových kyselin, různé způsoby manipulace s nukleovými kyselinami, sekvenování DNA a dále pak různé metody analýzy genové exprese (studium transkripce a translace). V následující části kapitoly jsou vysvětleny principy nejpoužívanějších molekulárně biologických metod spolu s příklady jejich možného využití.
IZOLACE DNA – je prvním krokem většiny molekulárně biologických technik. Materiálem pro izolaci DNA mohou být jednotlivé buňky (např. prokaryotických organizmů nebo kvasinek), tkáně a orgány eukaryot, které jsou nejdříve homogenizovány, nebo například virové částice. Izolace DNA zahrnuje 3 základní kroky:
- Rozrušení buněk nebo virových kapsidů působením enzymů (lysozym, celulázy) a/nebo detergentů (dodecylsulfát sodný).
- Odstranění kontaminant pomocí enzymů (proteináza, RNAáza).
- Vlastní extrakce DNA – nejčastěji je používaná fenol–chloroformová extrakce, kdy buněčný lyzát je promíchán se směsí fenolu a chloroformu. Fenol je organické rozpouštědlo používané k oddělení proteinů od NK. Proteiny jsou hydrofobní a zůstávají v organické fázi, zatímco NK jsou vysoce nabité a přecházejí do vodné fáze. Chloroform denaturuje proteiny, rozpouští tuky a napomáhá oddělení jednotlivých fází získaných v následujícím kroku. Centrifugací je oddělena spodní organická fáze, tvořená fenolem, mezifáze, tvořená denaturovanými proteiny a zbytky buněk, a horní vodná fáze, v níž je rozpuštěna DNA. DNA je následně vysrážena etanolem, precipitát je shromážděn centrifugací a získaný sediment je rozpuštěn ve vhodném roztoku (např. ve vodě). K izolaci DNA ze vzorku krve či tkáně je možné použít komerčně dodávané izolační soupravy (kity), které výrazně zjednodušují a urychlují postup získání DNA.
PCR (polymerase chain reaction, polymerázová řetězová reakce) je metoda sloužící k mnohonásobnému zmnožení (amplifikaci) specifického úseku DNA in vitro. PCR zavedl v roce 1983 Kary Mullis (za objev této metody dostal Nobelovu cenu). Princip syntézy DNA touto metodou je podobný replikaci: kopie úseku DNA jsou syntetizovány pomocí enzymu DNA-polymerázy podle templátu ve formě jednořetězcové DNA na principu komplementarity bází. K zahájení reakce je zapotřebí dvou primerů (čti prajmrů) – chemicky syntetizovaných krátkých oligonukleotidů, které se připojují ke komplementárním úsekům protilehlých řetězců DNA tak, že jejich 3'-OH-konce směřují proti sobě. Pomocí primerů je zároveň vymezen úsek DNA, který bude amplifikován. Jako templáty pro syntézu slouží oba řetězce dsDNA, po předchozí denaturaci.
Reakční směs pro PCR:
-
 templátová DNA – může být izolována z různých mikroorganizmů, bioptických vzorků, stěrů, z buněk z tkáňových kultur, z tělních tekutin
templátová DNA – může být izolována z různých mikroorganizmů, bioptických vzorků, stěrů, z buněk z tkáňových kultur, z tělních tekutin
- 2 primery (každý komplementární k jednomu řetězci DNA)
- dNTP (deoxyribonukleosidtrifosfáty)
- termostabilní DNA polymeráza (např. Taq polymeráza získaná z termofilní bakterie Thermus aquaticus žijící v horkých pramenech)
 (dNTP a DNA polymeráza bývají součástí tzv. master mixu)
(dNTP a DNA polymeráza bývají součástí tzv. master mixu)
Reakční směs pro PCR se napipetuje do malé PCR zkumavky, která se vloží do speciálního přístroje termocykleru (čti termosajkleru), kde probíhají cyklicky se opakující kroky za různých teplot.
Průběh PCR:
| 1. počáteční denaturace DNA (separace řetězců) (94 °C, 2-5 min) | |
|
Vlastní řetězová reakce:
2. denaturace (separace řetězců) (94 – 95 °C, 20 – 45 s) 3. připojení (nasedání) primerů (55 – 65 °C, 30 – 90 s) 4. polymerační reakce (72 °C, 45 – 90 s) (prodlužování řetězců pomocí DNA-polymerázy, která syntetizuje komplementární řetězce DNA z volných nukleotidů, nově syntetizované řetězce slouží jako templáty pro další cyklus) |
|
| 5. závěrečná extenze (72 °C, 5 min) (dosyntetizování případně nedosyntetizovaných řetězců) |
|
Výhodou PCR je, že vyžaduje minimální množství DNA (teoreticky stačí 1 molekula DNA). Touto metodou lze získat 2n-1 kopií, kdy n je počet cyklů. Z jedné molekuly DNA lze tedy například získat po proběhnutí 30 amplifikačních cyklů víc než 109 kopií.
*PCR (polymerázová – používá se enzym DNA polymeráza, řetězová reakce – počet kopií DNA roste během jednotlivých cyklů řetězovou řadou – 2, 4, 8, 16, 32...).
Výsledný produkt PCR (amplifikovaný úsek DNA) můžeme analyzovat např. stanovením velikosti produktu gelovou elektroforézou, štěpením restrikčními enzymy a posouzením vznikajících restrikčních fragmentů (RFLP), hybridizací se značenou sondou komplementární k části sekvence amplifikovaného úseku nebo stanovením sekvence DNA (sekvenování). Variantou PCR umožňující syntézu cDNA podle RNA templátu je reverzní PCR (RT-PCR) využívající enzymu reverzní transkriptázy.
Využití PCR:
PCR má mnohostranné využití nejen v základním výzkumu (k izolaci genů nebo jejich částí, k přípravě značených sond, při sekvenování DNA) a aplikovaném genetickém výzkumu (k detekci mutací v genech, ke studiu polymorfizmu genů nebo v populační genetice), ale uplatňuje se i v klinických disciplínách (v prenatální diagnostice např. dědičných chorob, při detekci patogenních mikroorganizmů, k identifikaci onkogenů, ke stanovení pohlaví), v archeologii, kriminalistice (k identifikaci jedinců), v soudním lékařství (např. k určení paternity), v potravinářském průmyslu (k identifikaci falšování potravinářských výrobků) a v dalších vědních oborech (zoologie, botanika, mikrobiologie, parazitologie).
 GELOVÁ ELEKTROFORÉZA patří k nejpoužívanějším separačním technikám sloužícím k izolaci a analýze nukleových kyselin a proteinů. Na tomto místě je vysvětleno použití gelové elektroforézy pro separaci různě dlouhých fragmentů DNA. Principem metody je pohyb záporně nabitých molekul DNA (hlavním nositelem náboje nukleových kyselin jsou záporně nabité fosfátové skupiny) v elektrickém poli směrem k anodě. Pomocí gelové elektroforézy můžeme separovat molekuly DNA na základě rozdílných rychlostí pohybu molekul DNA v gelu, které jsou nepřímo úměrné velikosti molekuly DNA. Elektroforéza se provádí na vhodném nosiči, nejčastěji v gelu tvořeném agarózou či polyakrylamidem (ve cvičení bude použita agaróza). Gel je tvořen složitou sítí polymerních molekul s póry, jimiž se různě velké molekuly DNA pohybují různou rychlostí (velké fragmenty pomaleji, malé fragmenty rychleji). Agarózový gel se připravuje v různé hustotě (udávané v % práškové agarózy). Agaróza se rozpouští v pufru, který je také obsažen v elektroforetické vaně jako elektrolyt (ve cvičení bude použit TBE pufr obsahující Tris, kyselinu boritou a EDTA). Vzorky se nanáší do jamek v gelu, které byly vytvořeny pomocí tzv. hřebínku.
GELOVÁ ELEKTROFORÉZA patří k nejpoužívanějším separačním technikám sloužícím k izolaci a analýze nukleových kyselin a proteinů. Na tomto místě je vysvětleno použití gelové elektroforézy pro separaci různě dlouhých fragmentů DNA. Principem metody je pohyb záporně nabitých molekul DNA (hlavním nositelem náboje nukleových kyselin jsou záporně nabité fosfátové skupiny) v elektrickém poli směrem k anodě. Pomocí gelové elektroforézy můžeme separovat molekuly DNA na základě rozdílných rychlostí pohybu molekul DNA v gelu, které jsou nepřímo úměrné velikosti molekuly DNA. Elektroforéza se provádí na vhodném nosiči, nejčastěji v gelu tvořeném agarózou či polyakrylamidem (ve cvičení bude použita agaróza). Gel je tvořen složitou sítí polymerních molekul s póry, jimiž se různě velké molekuly DNA pohybují různou rychlostí (velké fragmenty pomaleji, malé fragmenty rychleji). Agarózový gel se připravuje v různé hustotě (udávané v % práškové agarózy). Agaróza se rozpouští v pufru, který je také obsažen v elektroforetické vaně jako elektrolyt (ve cvičení bude použit TBE pufr obsahující Tris, kyselinu boritou a EDTA). Vzorky se nanáší do jamek v gelu, které byly vytvořeny pomocí tzv. hřebínku.
 Zatížení DNA (klesne do jamky v gelu) a migrace DNA v gelu jsou zajištěny přidáním tzv. nanášecího neboli vkládacího pufru, který je tmavě zbarvený a je tak umožněna kontrola vložení PCR produktu do příslušné jamky a také migrace v gelu. Pro odhad velikosti pozorovaných DNA fragmentů se do jedné jamky gelu nanáší tzv. velikostní marker (hmotnostní standard, DNA ladder = žebřík) o definované velikosti jednotlivých fragmentů. Po proběhnutí elektroforézy je třeba separované fragmenty DNA zviditelnit. Pro vizualizaci DNA se používá značení barvivem, které se váže na DNA, např. ethidiumbromid nebo Midori Green (na cvičení bude použit Midori Green) a v UV záření v přístroji zvaném UV transiluminátor zviditelní fragmenty DNA. Pro detekci fragmentů DNA lze použít radioaktivní značení, nebo hybridizaci se značenou sondou (krátkým oligonukleotidem, který se komplementárně váže k hledané sekvenci). Rozdělené molekuly DNA lze také ve funkční formě izolovat z gelu.
Zatížení DNA (klesne do jamky v gelu) a migrace DNA v gelu jsou zajištěny přidáním tzv. nanášecího neboli vkládacího pufru, který je tmavě zbarvený a je tak umožněna kontrola vložení PCR produktu do příslušné jamky a také migrace v gelu. Pro odhad velikosti pozorovaných DNA fragmentů se do jedné jamky gelu nanáší tzv. velikostní marker (hmotnostní standard, DNA ladder = žebřík) o definované velikosti jednotlivých fragmentů. Po proběhnutí elektroforézy je třeba separované fragmenty DNA zviditelnit. Pro vizualizaci DNA se používá značení barvivem, které se váže na DNA, např. ethidiumbromid nebo Midori Green (na cvičení bude použit Midori Green) a v UV záření v přístroji zvaném UV transiluminátor zviditelní fragmenty DNA. Pro detekci fragmentů DNA lze použít radioaktivní značení, nebo hybridizaci se značenou sondou (krátkým oligonukleotidem, který se komplementárně váže k hledané sekvenci). Rozdělené molekuly DNA lze také ve funkční formě izolovat z gelu.
RFLP (restriction fragment length polymorphism, polymorfismus délky restrikčních fragmentů) je metoda, jejíž podstatou je enzymatické štěpení molekul DNA ve specifickém restrikčním místě enzymem restrikční endonukleázou. Různé restrikční endonukleázy štěpí cílovou DNA v různých místech, v závislosti na sekvenci DNA. Po rozdělení vzniklých fragmentů pomocí gelové elektroforézy můžeme na základě velikosti a počtu fragmentů sledovat rozdíly ve studovaných sekvencích, tzv. polymorfizmy. Polymorfizmy v délkách restrikčních fragmentů jsou způsobeny přestavbami (např. inzercemi, delecemi a substitucemi bází) ve studované sekvenci, které způsobí změnu počtu restrikčních míst. Využití např. k určení pohlaví u ptáků nebo určení otcovství (test paternity).
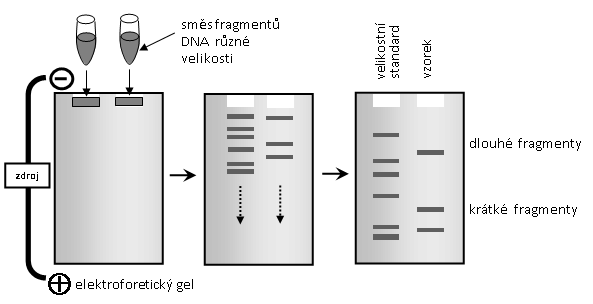
Obr.: Gelová elektroforéza.
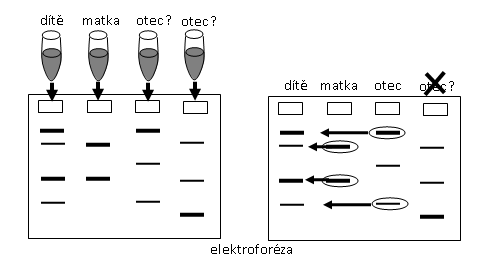
Obr.: Určení otcovství na základě metody RFLP – DNA je izolovaná např. z buněk bukální sliznice a využita k amplifikaci specifické sekvence. Amplikon je následně rozštěpen enzymem a výsledné fragmenty jsou separovány gelovou elektroforézou. Výsledné fragmenty lze využít k vyloučení nebo potvrzení otcovství.
HYBRIDIZACE NUKLEOVÝCH KYSELIN je založena na specifickém spojení (hybridizaci, renaturaci) komplementárních nukleotidových sekvencí pocházejících z různých molekul NK. Základem hybridizace je obvykle značená sonda – krátký úsek DNA o známé nukleotidové sekvenci, s jejíž pomocí můžeme detekovat sekvenci k ní komplementární. Sonda může být značena fluorescenčně nebo radioaktivně. Nejčastěji bývá hybridizace prováděna na nosičích (viz Southernův přenos), ale je například možno hybridizovat NK i v intaktních buňkách (hybridizace "in situ").
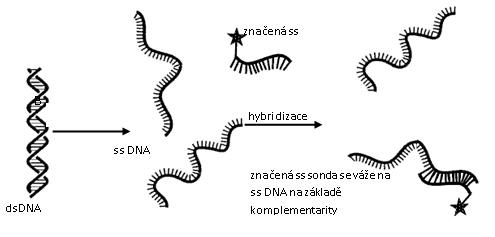
Obr.: Princip hybridizace DNA (ss – jednořetězcová, ds – dvouřetězcová).
Postup Southern blottingu (Southernův přenos) + hybridizace:
- Příprava a značení sondy.
- Rozdělení restrikčních fragmentů DNA daného vzorku gelovou elektroforézou.
- Denaturace DNA a přenos jednořetězcových fragmentů DNA na nylonovou membránu = Southern blotting.
- Inkubace membrány se značenou jednořetězcovou sondou
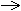 hybridizace (navázání) sondy s komplementární sekvencí DNA na membráně.
hybridizace (navázání) sondy s komplementární sekvencí DNA na membráně. - Odmytí nenavázané sondy.
- Detekce navázané sondy = vizualizace (autoradiografie nebo stanovení fluorescence).
SEKVENOVÁNÍ DNA slouží ke stanovení pořadí (sekvence) nukleotidů v molekule DNA (primární struktury). Sekvenování DNA je založeno na přípravě, separaci a detekci fragmentů DNA, jejichž velikost se liší o 1 nukleotid. Enzymová (Sangerova, po Fredericku Sangerovi) metoda využívá modifikovanou PCR k syntéze kopií DNA, do nichž jsou začleňovány kromě deoxyribonukleosidtrifosfátů (dNTP) i dideoxynukleosidtrifosfáty (ddNTP), které postrádají hydroxylovou skupinu na 3’-konci, na kterou by se mohl navázat další nukleotid v nově vznikajícím řetězci. Tyto ddNTP tedy slouží jako terminátory syntézy (viz obr. 62). Samotná syntéza DNA pomocí PCR se provádí odděleně ve čtyřech vzorcích, přičemž každý z nich obsahuje jiný dideoxynukleosidtrifosfát (A, T, G, nebo C).
Polymerázová řetězová reakce využívaná při sekvenování DNA má další specifika. Amplifikace produktu probíhá pomocí tzv. asymetrické PCR, která na rozdíl od „klasické“ PCR využívá pouze jednoho primeru. Amplifikace PCR produktu tedy probíhá pouze na jednom řetězci DNA, na který se tento primer specificky váže, a kopie molekul DNA nepřibývají exponenciální řadou.
Reakční směs:
- templátová DNA
- 1 primer připojující se k místu na molekule DNA, od něhož chceme stanovovat sekvenci
- 4 typy normálních nukleotidů v nadbytku (dATP, dCTP, dGTP, dTTP)
- jeden typ ddNTP v malém množství (v každém ze 4 vzorků je jiný)
- DNA polymeráza
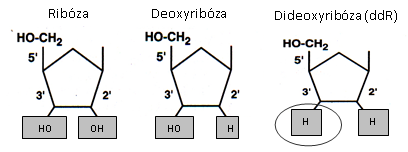
Obr.: Chemická struktura dideoxynukleosidtrifosfátu (ddNTP) a princip terminace syntézy nově vznikajícího řetězce DNA po začlenění dideoxynukleosidtrifosfátu do nově vznikajícího řetězce DNA.
Postup enzymového (Sangerova) sekvenování:
- Příprava ssDNA jejíž sekvence má být stanovena.
- Rozdělení do 4 vzorků, z nichž každý obsahuje jiný ddNTP
- Reakce s DNA polymerázou, při níž se začlení do různých míst syntetizované DNA příslušný ddNTP obsažený ve směsi. V každém ze 4 vzorků vzniknou fragmenty, které jsou zakončeny jedním typem ddNTP (ddCTP, ddGTP, ddATP, nebo ddTTP).
- Denaturace produktů
- Elektroforetická separace umožňující oddělení fragmentů lišících se délkou o jednu bázi
- Detekce fragmentů
 Automatické sekvenování DNA je variantou enzymatického sekvenování DNA. Syntéza DNA probíhá v jedné PCR reakci (každý ddNTP je značen jinou fluorescenční značkou) a vzniklé produkty (různě dlouhé úseky jednořetězcové DNA) jsou tak označeny jinou fluorescenční značkou. K následnému stanovení sekvence DNA vzniklých PCR produktů se využívá genetický analyzátor – "sekvenátor". Detekce těchto produktů probíhá během kapilární elektroforézy (=elektroforéza probíhá v tenké kapiláře naplněné gelem) pomocí laserového detektoru napojeného na počítač, který vyhodnocuje sekvenci.
Automatické sekvenování DNA je variantou enzymatického sekvenování DNA. Syntéza DNA probíhá v jedné PCR reakci (každý ddNTP je značen jinou fluorescenční značkou) a vzniklé produkty (různě dlouhé úseky jednořetězcové DNA) jsou tak označeny jinou fluorescenční značkou. K následnému stanovení sekvence DNA vzniklých PCR produktů se využívá genetický analyzátor – "sekvenátor". Detekce těchto produktů probíhá během kapilární elektroforézy (=elektroforéza probíhá v tenké kapiláře naplněné gelem) pomocí laserového detektoru napojeného na počítač, který vyhodnocuje sekvenci.
Využití sekvenování DNA - sekvenování DNA má řadu aplikací ve vědě, medicíně a dalších oblastech. Sekvenují se celé genomy, případně jenom některé části, které mají pro daný obor význam. Ve fylogenetice představuje DNA sekvenování možnost studovat fylogenezi organizmů, kde se zpravidla sekvenuje DNA, která kóduje ribozomální RNA. Antropologie využívá srovnávání DNA ke zjišťování migrací lidských ras (zejména podle mitochondriální DNA a Y-chromozomální DNA). Má využití rovněž ve forenzních vědách a v kriminalistice k testování paternity nebo například umožňuje stanovení viny či neviny v případě podezření z trestné činnosti. V zemědělství má možnost využití například při tvorbě geneticky modifikovaných plodin V lékařství slibuje sekvenování DNA například revoluci v diagnostice chorob a časnému zjištění náchylnosti jedince k určitým nemocem (rakovina, kardiovaskulární onemocnění) a v neposlední řadě také možnost využití v genové terapii.
Sekvenování příští generace (NGS, next-generation sequencing) je dalším stupněm vývoje sekvenačních metod. Tyto nejnovější metody jsou založeny na paralelizaci procesu sekvenování a produkci tisíců až milionů sekvencí současně a umožňují tak velmi rychlé a relativně levné sekvenování ve velkých objemech. Díky rychle klesajícím cenám a zvyšující se dostupnosti se tyto metody rychle prosazují nejen při studiu celých genomů (tzv. celogenomové sekvenování) či jejich částí, ale také v rutinní DNA diagnostice v humánní medicíně, v cytogenetice aj.
GENOMIKA, BIOINFORMATIKA, BIOLOGICKÉ DATABÁZE A POČÍTAČOVÉ ZPRACOVÁNÍ BIOLOGICKÝCH DAT
Výše zmíněnými metodami automatického sekvenování DNA a sekvenování příští generace je dnes možno stanovit nukleotidové sekvence celých genomů. Komplexní analýzou genomů založenou na znalosti pořadí nukleotidů v DNA se zabývá obor genomika. V současné době je známa kompletní sekvence desítek genomů, a to nejen bakteriálních, ale i genomů vyšších organismů, např. kvasinky Saccharomyces cerevisiae (12 Mbp), drozofily (137 Mbp) a od roku 2000 je známá i nukleotidová sekvence lidského genomu (3 Gbp).
Genomové sekvence představují obrovský objem biologických dat, který nelze zpracovávat bez odpovídajícího počítačového vybavení. Pro účely přehledného uchovávání biologických dat, vyhledávání potřebných informací a jejich následné analýzy jsou využívány přístupy bioinformatiky. Termín bioinformatika se objevil poprvé v roce 1991, představuje spojení dvou technologií (oblast molekulární biologie a biotechnologií a oblast informačních technologií), u nichž došlo v posledních letech k explozivnímu růstu nových poznatků. Hlavní oblastí zájmu bioinformatiky je vyhledávání informací v databázích, srovnávání sekvencí nukleových kyselin a proteinů, vyhledávání genů, funkční genomika, klasifikace proteinů a proteomika, fylogenetické studie a srovnávací genomika.
Shromažďováním a správou dat, vývojem nástrojů pro jejich analýzu a poskytováním informací se ve světě zabývá několik institucí. Na internetových stránkách těchto institucí jsou veřejně přístupné biologické databáze, které obsahují rozsáhlé soubory dat (nukleotidových nebo aminokyselinových sekvencí), které jsou obvykle spojeny s počítačovým softwarem pro aktualizaci a vyhledávání dat.
Nejdůležitější databáze sekvencí nukleových kyselin a proteinů:
- Databáze EMBL byla zřízená v roce 1980 jako první databanka nukleotidových sekvencí Evropskou molekulárně biologickou laboratoří (EMBL - European Molecular Biology Laboratory) ve Velké Británii. Je veřejně přístupná na stránkách Evropského institutu pro bioinformatiku (EBI - European Bioinformatic Institute) http://www.ebi.ac.uk.
- Databáze DDBJ zahájila svojí činnost v roce 1984, shromažďuje data především z japonských výzkumů. Databáze je spravována Centrem informační biologie (CIB - Center for Information Biology, založen v roce 1995 jako oddělení Národního genetického institutu) v Japonsku a je veřejně přístupná na adrese http://www.ddbj.nig.ac.jp.
- GenBank byla založena v roce 1992. Databázi nukleotidových sekvencí spravuje Národní centrum biotechnologických informací (NCBI - National Center for Biotechnology Information). Je přístupná na adrese http://www.ncbi.nlm.nih.gov.
- Swiss-Prot a TrEMBL je databáze zřízená v roce 1986 Švýcarským institutem pro bioinformatiku (SIB - Swiss Institute of Bioinformatics). Databáze obsahuje aminokyselinové sekvence proteinů a je přístupná na adrese http://www.expasy.org/sprot.
Množství molekulárně-biologických dat se zvyšuje tak rychle, že je nezbytné mít k dispozici prostředky, pomocí kterých můžeme k těmto datům snadno přistupovat. Existují tři prostředky na získávání informací, které jsou vstupním bodem do několika (až 80) integrovaných databází: Entrez (vyvinut v NCBI, http://www.ncbi.nlm.nih.gov/Entrez/), SRS (Sequence Retrieval System, vyvinut v EBI, http://srs.ebi.ac.uk/) a DBGET/Link DB (Integrated Database Retrieval System, vyvinut v Institutu pro chemický výzkum v Japonsku, http://www.genome.ad.jp/dbget/).
Nukleotidové sekvence můžeme pomocí počítačových analýz dále zpracovávat. Pomocí vhodného softwaru je možné identifikovat geny, jejich strukturu (exony a introny), nebo regulační oblasti (např. promotory, terminátory transkripce atd.). Na základě nalezených genů můžeme, opět s použitím vhodného softwaru, stanovit aminokyselinovou sekvenci proteinů kódovaných těmito geny a stanovit jejich základní charakteristiky (např. sekundární strukturu). Software vhodný k podobným analýzám je volně přístupný na Internetu např. na adresách http://www.ensembl.org nebo http://www.expasy.org.
Kromě výše zmíněné základní charakterizace lze také srovnávat nukleotidové sekvence různých buněk (organizmů, druhů atd.) mezi sebou, což je náplní komparativní (srovnávací) genomiky. Můžeme např. identifikovat rozdíly mezi genomy příbuzných druhů a určit tak jejich evoluční příbuznost (viz následující kapitola).
Podrobně popsané téma lze najít na tématických stránkách Molekulární biologie.
Kontrolní otázky – metody molekulární biologie
- Jaké znáš metody molekulární biologie?
- Jaký je princip izolace DNA?
- O co se zasloužili Kary Mullis a Frederick Sanger?
- Co je to PCR a jaký je její princip?
- Jaké jsou fáze PCR?
- Co vše je třeba pro PCR a v jakém přístroji probíhá?
- K čemu se PCR využívá?
- Co je to gelová elektroforéza a jaký je její princip?
- Co je to RFLP a jaký je její princip?
- K čemu se RFLP využívá?
- Jak funguje hybridizace a k čemu ji lze využít?
- Co je to sekvenování a jaký je jeho princip?
- Co vše je třeba pro sekvenování a v jakém přístroji probíhá?
- K čemu se sekvenování využívá?
- Jak se dá určit pohlaví ptáků pomocí metod molekulární biologie?
- Jak se dá určit otcovství pomocí metod molekulární biologie?
ÚKOLY - Metody molekulární biologie (viz úkoly)
Metody molekulární biologie
Cvičení z molekulární biologie jsou sestavena tak, aby se studenti prakticky seznámili se základními metodami, které se využívají k analýze DNA. Studenti si sami vyzkouší izolaci DNA, amplifikaci DNA pomocí PCR, restrikční štěpení PCR produktu, elektroforézu, vizualizaci DNA a hodnocení výsledku. Tyto metody budou využity při řešení jednoho komplexního úkolu. Bude se jednat o určení pohlaví ptačího jedince z biologického materiálu pomocí restrikční analýzy PCR produktu specifického genu. Každý student bude pracovat samostatně. Materiál k vyšetření bude zajištěn, ale lze si zajistit svůj vlastní materiál.
Instrukce k zajištění vlastního materiálu: K vyšetření lze použít jakékoliv ptačí buňky obsahující DNA. Lze odebrat krev od ptačího jedince zaživa, krev nebo orgány během porážky (kur, husa, kachna....), případně odebrat tkáň z drůbežího masa koupeného v tržní síti.
Ptačí krev:
- odběr do zkumavky s anti-koagulans EDTA (zkumavky budou k vyzvednutí u laborantky)
- požadovaný objem je minimálně 200 µl
- po odběru je třeba vzorek uložit do mrazáku při teplotě pod -15 °C
Ptačí tkáň (svalovina či vnitřní orgán):
- odběr do igelitového sáčku nebo mikrozkumavky
- o velikosti minimálně dvou špendlíkových hlaviček
- po odběru je třeba vzorek uložit do mrazáku při teplotě pod -15 °C
Vzorek je třeba označit (jméno studenta, číslo skupiny) a předat laborantce k evidenci a uložení do mrazáku ve cvičebně. Vzorky je potřeba přinést nejpozději do cvičení, kdy bude probíhat příprava tkáně k izolaci DNA.
Úkol 1 a 2: Příprava tkáně k izolaci DNA a vlastní izolace DNA
Izolace DNA se provádí pomocí izolační soupravy založené na principu adsorpce DNA na silikát. Vyšetřovaný materiál (ptačí krev či tkáň) je nejdříve lyzován pomocí lyzačního pufru (obsahuje detergenty, které rozpouští membrány a denaturuje proteiny) a enzymu proteinázy K (štěpí proteiny včetně histonů vázajících se na DNA). Buněčný lyzát se přenese na izolační kolonku, jejíž součásti je silikátový povrch (SiO2 – sklo). V přítomnosti chaotropních solí (součást lyzačního pufru) adheruje DNA na silikát. Kolonka s DNA vázanou na silikát je promyta promývacími roztoky a následně uvolněna pomocí elučního pufru. Vzhledem k tomu, že různé izolační soupravy od jednotlivých výrobců se poněkud liší, pokud jde o jednotlivé komponenty (zejména použité roztoky a jejich pipetované objemy), není možné uvést vždy platný konkrétní sled kroků a je třeba se vždy řídit předepsaným postupem od příslušného výrobce, který vám bude k dispozici na cvičení.
Zásady práce:
- Každý student zpracovává vlastní vzorek a pracuje v pracovní skupině, která má k dispozici sadu automatických pipet.
- U pipet lze nastavit požadovaný objem - pozor na přetočení pipety mimo dané rozmezí.
- K zabránění kontaminace vzorku a chemikálií se pro jednotlivé kroky používá vždy nová špička.
- K zabránění kontaminace pipet se pro práci s DNA používá špička s filtrem.
- K zajištění přesného objemu je třeba důkladně nasadit špičku na pipetu.
- Požadovaný objem se získá stlačením pipety do první polohy a ponořením špičky pipety do nasávané tekutiny, povolením stlačení, přenesením požadovaného objemu a stlačením pipety do druhé polohy.
- Homogenizace vzorku se provádí ve zkumavce tzv. propipetováním tj. po přidání určité chemikálie do zkumavky třikrát opakovaně nasát směs do špičky a vytlačit.
- Mikrozkumavky je třeba označit číslem skupiny a pořadovým číslem studenta ve skupině.
Úkol 3: PCR
Příprava PCR:
-
Každá pracovní skupina si do mikrozkumavky (1,5 ml) připraví společnou PCR směs dle počtu vzorků (n) s rezervou (n+1):
Směs pro jeden vzorek:
- 10 µl - PCR master mix (směs nukleotidů dNTP, DNA polymerázy a Mg2+ iontů)
- 0,2 µl - primer PP (pořadí nukleotidů: TCTGGATCGCTAAATCCTTT)
- 0,2 µl - primer P8 (CTCCCAAGGATGAGRAAYTG) (R a Y - degenerované nukleotidy)
- 7,6 µl - voda pro PCR
- Napipetujte (novou špičkou) 18 µl PCR směsi do PCR mikrozkumavky (0,2 ml) označené fixem.
- Napipetujte (špičkou s filtrem) 2 µl izolované DNA.
- Uzavřete důkladně PCR mikrozkumavku, vložte ji do termocykleru a spusťte program.
-
Po dokončení programu bude PCR produkt uchován v lednici.
Program PCR amplifikace (trvá asi 1 hod 55 min):

Úkol 4: Restrikční reakce s PCR produktem, elektroforéza, vizualizace a hodnocení
K určení pohlaví u ptáků se využívá gen CHD (Chromo-Helicase-DNA binding gene), který kóduje protein, jež reguluje aktivaci transkripce na úrovni chromatinu. Tento gen je u ptáků lokalizován na pohlavních chromozomech.
- Samčí pohlaví je u ptáků homogametické s pohlavními chromozomy ZZ.
- Samičí pohlaví je heterogametické s pohlavními chromozomy ZW.
Pomocí PCR je namnožena DNA odpovídající části genu na chromozomu W (CHD-W) a na chromozomu Z (CHD-Z). PCR produkt je štěpen pomocí restrikční endonukleázy (restriktázy) Hae III (izolované z bakterie Haemophilus aegyptius) v restrikčním místě:
PCR produkt genu CHD-Z toto místo obsahuje, proto dojde působením enzymu k odštěpení fragmentu DNA, zatímco PCR produkt genu CHD-W se enzymem neštěpí. Fragmenty jsou separovány pomocí gelové elektroforézy, vizualizovány pod UV zářením a vyhodnoceny.
Restrikční reakce:
- Napipetujte 1,2 µl směsi restriktázy Hae III a aktivačního pufru do nové označené PCR zkumavky (0,5 ml).
- Napipetujte (novou špičkou s filtrem) 10 µl PCR produktu.
- Vložte do termocykleru při teplotě 37 °C na 45 min.
Příprava 1,2 % agarózového gelu:
Připraví se jeden gel pro všechny studenty ve cvičebně.
- Do baňky typu Erlen dejte 1,2 g agarózy.
- Skleněným válcem odměřte 100 ml TBE pufru, přidejte do baňky a kroužením promíchejte.
- Dejte baňku do mikrovlnné trouby a vařte při teplotě nastavené na maximální ohřev po dobu 2 minut (jakmile začne obsah kádinky bublat, přerušte ohřev a promíchejte obsah kádinky v ruce s nasazenou rukavicí).
- Po 2 minutách ohřevu vyjměte baňku z mikrovlnné trouby a opatrně ji ochlaďte pod tekoucí vodou na teplotu přibližně 60 °C (teplota, kdy několik sekund udržíme kádinku přiloženou ke hřbetu ruky).
- Do rozehřátého roztoku agarózy napipetujte (novou špičkou) 3 µl Midori Green (10 tis. krát koncentrovaný roztok) a v ruce promíchejte.
- Připravte si nalévací vanu a přelijte do ní rozehřátý roztok agarózy z baňky do výšky minimálně 8 mm.
- Do vany vložte hřebínek a pipetovací špičkou odstraňte případné bubliny v gelu.
- Gel ztuhne asi po 30 minutách.
Horizontální agarová gelová elektroforéza a vizualizace DNA
- Po ztuhnutí gelu vyjměte hřebínek, otočte gel v elektroforetické vaně a zalijte TBE pufrem, tak aby byl celý gel ponořený.
- Do jedné z jamek v gelu (nejlépe do prostřední) naneste 3 µl velikostního markeru.
- Do sousední jamky naneste 10 µl směsného vzorku PCR produktu (směsný vzorek PCR produktu připravíte smícháním všech vzorků ve cvičebně).
- Do dalších jamek nanáší (novou špičkou) každý student svůj vzorek, tj. 10 µl PCR produktu po restrikční analýze. S pipetou je třeba manipulovat opatrně, ať neprotrhnete gel.
- Zapojte elektroforetickou vanu do zdroje a pusťte elektrický proud při konstantním napětí 160 V po dobu 15-20 minut.
- Po ukončení elektroforézy přemístěte gel na UV-transiluminátor a pod UV zářením odečtěte výsledek. V rámci bezpečnosti je třeba pozorovat gel přes plastový kryt.
U samičího pohlaví: (ZW) se na gelu objeví 2 pruhy (bandy). Jeden větší, který odpovídá neštěpenému CHD-W (o stejné velikosti jako neštěpený PCR produkt) a druhý menší asi o 50 bp (párů bází).
U samčího pohlaví: dojde ke štěpení CHD-Z a na gelu se objeví jeden pruh o menší velikosti.
Obr.: Výsledek gelové elektroforézy: 1 – velikostní standard, 2 – neštěpený PCR produkt, 3 – samec, 4 – samice.
Úkol 5: Sekvenátor a sekvenování DNA
Než proběhne restrikční reakce nebo gelová elektroforéza navštivte Laboratoř sekvenční analýzy na Ústavu biologie a chorob volně žijících zvířat, kde se seznámíte s osmikapilárovým automatickým sekvenátorem (Beckman Coulter CEQ 8000), který slouží ke stanovení sekvence DNA na principu separace fragmentů DNA syntetizovaných terminační enzymovou Sangerovou metodou.
Buněčné a tkáňové kultury
Buňky, tkáně a dokonce i celé orgány (nebo části orgánů) mohou být udržovány (pěstovány) naživu mimo tělo v pufrovaném roztoku s živinami, tzn. za podmínek, jež věrně napodobují jejich fyziologickou situaci. V medicíně, biologii a příbuzných oborech se v souvislosti s pěstováním organizmů v umělých podmínkách ve zkumavkách či jiném laboratorním skle používá termín in vitro (z latiny "ve skle"). Naproti tomu termín in vivo (z latiny "v živém") znamená výskyt organizmů (popř. jejich orgánů nebo jejich jednodušších složek a látek) v přirozených podmínkách (u složek či orgánů to znamená na/v živém organizmu). Prvotní tkáně používané pro založení kultur v laboratořích jsou často získávány ze zvířat, ale mohou být použity i lidské tkáně (např. krevní buňky, buňky z pupeční šňůry, placenty a chrupavek).
Využití: Metody buněčných a tkáňových kultur mají v dnešní době význam např. při vývoji a ověřování nových léků, při výrobě vakcín, v testech toxicity, v diagnostice, jsou používány ke kultivaci a dlouhodobým pasážím nitrobuněčných parazitů nebo virů nebo při genových manipulacích. Využití buněčných a tkáňových kultur tak velkou měrou přispívá i k omezování pokusů na zvířatech.
HISTORIE
- Roux E. (1885) jako první kultivoval embryonální kuřecí buňky v solném roztoku mimo tělo. Problémem byla dlouhodobá kultivace, aniž by došlo k bakteriální kontaminaci. Tento problém později vyřešila antibiotika.
- Rous P. a Jones F.S. (1916) používali proteolytický enzym trypsin k natrávení kousku tkáně. Takto dispergované buňky bylo možno opakovaně pasážovat - počátek studií moderních tkáňových kultur.
- Eagle H. (1955) definoval složení média potřebné ke kultivaci buněk (tzv. Eaglovo médium). Do té doby se používala nepřesně definovaná média složená např. z krevní plazmy a extraktů hovězích embryí.
- Hayflick L. a Moorhead P. (1961) prokázali, že lidské fibroblasty ve tkáňové kultuře po určitém počtu generací podléhají krizi a umírají (viz fázová křivka růstu buněk v tkáňových kulturách).
- Wigler M. a Axel R. (1977) vyvinuli metodu pro vnášení savčích genů do buněk v kultuře.
TKÁŇOVÉ KULTURY jsou tvořeny buňkami, které nejsou od sebe odděleny, a proto mohou na sebe navzájem působit, tak jako v organizmu. Tkáňové kultury tak nacházejí využití např. při kontrole účinků teratogenů a při testování kožní dráždivosti.
BUNĚČNÉ KULTURY jsou tvořeny izolovanými buňkami, které jsou pěstovány v kultivačních nádobách, kde rostou v jedné vrstvě (tzv. monolayer). Modifikace metod tkáňových kultur umožňují pěstovat v kultuře celou řadu specializovaných buněk, nejpoužívanější jsou fibroblasty a epiteliální buňky. Buňky získané přímo z organizmu, jež jsou pěstovány v kultuře, jsou známy pod názvem primární buněčné kultury. Příležitostně se mohou tyto buňky spontánně přetransformovat do souvislých buněčných linií, jež jsou schopny přežít v podmínkách in vitro po mnoho let. Např. název buněčné linie HeLa je odvozen ze jména 31 leté Američanky Henrietty Lacksové, které byly odebrány buňky z nádoru děložního čípku v roce 1951. Ačkoliv buňky buněčné linie jsou si velmi podobné, často nejsou identické. Genetickou uniformitu buněčné linie lze zajistit klonováním buněk, kdy se z jedné izolované buňky vytvoří kolonie identických buněk, tzv. klony.
Příklady buněčných kultur:
| Buněčná linie | Typ buněk | Původ | Způsob kultivace |
|---|---|---|---|
| Kc167 | embryonální buňky | octomilka | adherentní |
| MDBK | epiteliální buňky | tur domácí | adherentní |
| MDCK | epiteliální buňky | pes | adherentní |
| Vero | epiteliální buňky | kočkodan | adherentní |
| HeLa | epiteliální buňky | člověk | suspenzní |
| BHK21 | fibroblasty | křeček zlatý | suspenzní |
| SP2 | plazmatické buňky | myš | suspenzní |
KULTIVAČNÍ NÁDOBY - buňky se kultivují ve skleněných či plastových lahvích označovaných jako "Roux (čti 'ru') láhve" v termostatu při optimální teplotě (37 °C).
KULTIVAČNÍ MÉDIUM poskytuje buňkám optimální prostředí a slouží jako zdroj živin pro jejich růst. Přidává se do kultivačních nádob a pravidelně se musí vyměňovat za nové. Média (MEM = minimální esenciální médium) obsahují definované množství solí, glukózy, aminokyselin, vitaminů, inzulínu, transferinu, specifických růstových faktorů a bovinního fetálního séra. K prevenci bakteriální kontaminace se do média přidávají antibiotika (penicilin, streptomycin). Většina buněčných linií roste dobře při pH 7,4, při poklesu pH na 6,5 přestanou růst a při pH pod 6,5 ztrácí životaschopnost. Jako indikátor pH v médiu se používá fenolová červeň. Při pH 7,4 je zbarvení média červené, při poklesu pH (spotřebování živin, nahromadění metabolitů) se barva mění do žluta a to je signál pro výměnu média za čerstvé.
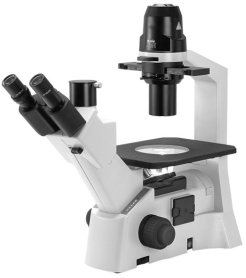
Inverzní mikroskop
KULTIVACE BUNĚK A PASÁŽOVÁNÍ - při práci s buněčnými kulturami (výměna média, pasážování buněk atd.) je potřebné dodržovat pravidla sterilní manipulace (používání boxů a germicidních lamp). Růst buněk v kultivační nádobě je možné průběžně pozorovat prostřednictvím speciálního inverzního mikroskopu. Buňky rostou v určitých fázích, které znázorňuje tzv. fázová křivka růstu. Většina buněk roste v kultivačních nádobách až do doby, kdy dosáhne vysokého procenta konfluence, tj. stavu, kdy buňky zaplní povrch dna nádoby a dostanou se do vzájemného kontaktu, čímž dochází k tzv. kontaktní inhibici. V té době je potřebné přenést (pasážovat) buňky do nové kultivační nádoby. Necháme-li buněčnou kulturu růst do vysoké hustoty, selektují se buňky, které ztrácejí normální kontrolu růstu a nepodléhají kontaktní inhibici. Takovéto buněčné linie nazýváme liniemi transformovanými. Podle způsobu růstu v kultuře a odlišnému způsobu pasážování lze buňky dělit na adherentní a suspenzní:
- Adherentní buňky adherují (přichycují se) na dno kultivační lahve v důsledku sekrece proteinů extracelulární matrix, jako např. lamininu, fibronektinu, kolagenu. Při výměně média se slije staré médium a nahradí se čerstvým, při pasážování se k uvolnění buněk ze dna lahve používá proteolytický enzym trypsin nebo jiná proteáza.
- Suspenzní buňky jsou volně dispergované v médiu. Při výměně média nebo pasážování je potřebné oddělit médium od buněk odstředěním.
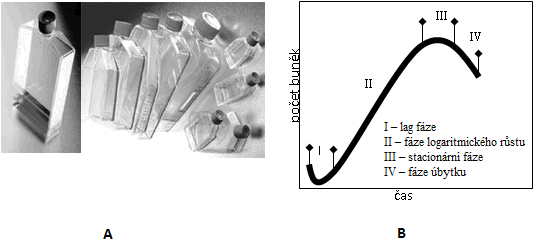
Obr.: A – plastové láhve pro kultivaci buněk, B – fázová křivka růstu buněk.
Kontrolní otázky – buněčné a tkáňové kultury
- V čem a za jakých podmínek se kultivují buňky in vitro?
- Jaký je rozdíl mezi pěstováním adherentních a suspenzních buněk?
- Jak se provádí pasážování buněk?
- Jaký průběh má růstová křivka buněk kultivovaných in vitro?
- Jaký mikroskop se používá k prohlížení buněčných kultur?
ÚKOLY - Buněčné a tkáňové kultury (viz úkoly)
Buněčné a tkáňové kultury
Úkol 1: Pozorování buněk v buněčné kultuře
TP: ledvinné buňky králíka z buněčné kultury
Pozorujte a zakreslete si ledvinné buňky králíka z buněčné kultury.
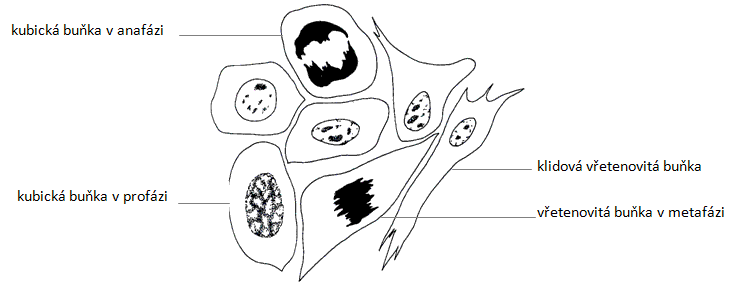
Obr.: Buňky rozdílné morfologie z buněčné kultury v klidové fázi a v mitóze.
Úkol 2: Práce s inverzním mikroskopem a buněčnou kulturou
NP: adherentní buňky z buněčné kultury
V inverzním mikroskopu si prohlédněte kultivační láhev s buněčnou kulturou (všímejte si tvaru buněk pokrývajících celé dno láhve). Slijte médium z láhve, propláchněte roztokem PBS (phosphate buffered saline, fosfátem pufrovaný fyziologický roztok) a do láhve přidejte 2 ml trypsinu. Účinkem trypsinu dojde k uvolnění buněk ze dna láhve, což se projeví zakalením obsahu láhve (uvolňování buněk lze urychlit umístěním láhví do termostatu na 37 oC nebo mechanicky klepáním láhve o dlaň ruky). Pod inverzním mikroskopem pozorujte uvolněné buňky, které jsou zakulacené a volně plavou. Do kultivační láhve přidejte médium obsahující sérum, které inhibuje účinek trypsinu, tak aby se zabránilo natrávení buněk. Poté slijte obsah láhve do kádinky, připravte si nativní preparát a pozorujte pod svým mikroskopem. Zakreslete si tvar buněk a porovnejte s tvarem, který měly buňky přisedlé.
Nebuněčné formy života, elektronové mikroskopy
Nebuněčné formy života
Mezi nebuněčné formy života patří viry (nukleové kyselina a proteiny), viroidy, virusoidy (nukleové kyseliny) a priony (proteiny).
VIRY jsou submikroskopické částice, jejichž velikost se pohybuje v desítkách až stovkách nanometrů. Genom u nejmenších virů je tvořen 3 500 nukleotidy (RNA-bakteriofág R17) a 3 strukturními geny kódující protein kapsidy, protein pro absorpci viru na hostitelskou buňku a specifickou RNA-polymerázu. Největším nově objeveným virem je Mimivirus z čeledi Mimiviridae (virus "napodobuje" bakterie), který byl zjištěn uvnitř buněk měňavky, měří 400 nm, jeho genetický kód se skládá z 800 000 nukleotidů a obsahuje až 900 genů.
Virion je jednotlivá částice (partikule), schopná infikovat hostitelskou buňku a množit se v ní. Je složen z nukleokapsidu, tj. nukleové kyseliny (NK), a to buď deoxyribonukleové (DNA), nebo ribonukleové (RNA) a z kapsidy, což je proteinový obal složený z proteinových molekul (kapsomer).
Obalené viry při zrání (maturaci) získávají membránový obal, který je odvozen z plazmatické nebo jaderné membrány (nebo z obou) hostitelské buňky, která je virem modifikována. Na povrchu obalu mohou být z glykoproteinů vytvořeny ostré výčnělky, tzv. hroty (peplomery), které udílí viru antigenní vlastnosti a jsou pro určité viry specifické.
Bakteriofág (zkráceně fág, "požírač bakterií") je virus infikující bakterie. Proteinová kapsida je složená z hlavičky obsahující nukleovou kyselinu (DNA, RNA) a z bičíku, ze kterého vyrůstají bičíková vlákna, která slouží k přichycení. Tyto viry mohou lyzovat napadené bakterie a lze je tak využít k antibakteriální léčbě. Po infekci bakterie může bakteriofág přejít do latentního (lyzogenního) stavu, kdy se začlení do genetické informace buňky ve formě tzv. profága. Teprve při „stresu“ bakteriální buňky se virus aktivuje, začne se replikovat a buňku zlyzuje. Byly popsány i případy, kdy se kmeny bakterií se začleněnou virovou DNA stanou vysoce patogenními původci onemocnění.
Pro taxonomii a systematiku virů jsou důležité tyto znaky:
- rozměry a morfologie virionu
- přítomnost (nepřítomnost) povrchového obalu: obalené a neobalené viry
-
typ a molekulární stavba genomové NK:
- typ NK: RNA-viry, DNA-viry
- počet a tvar řetězců NK: ssRNA - jednořetězcová (z angl. single stranded), dsRNA -dvouřetězcová (z angl. double stranded), ssDNA, dsDNA, lineární (většinou) nebo kružnicová NK
- polarita řetězce NK: (+)RNA (plus RNA, pozitivní RNA, stejná polarita jako mRNA), (-)RNA (minus RNA, negativní RNA), (+)DNA, (-)DNA.
- znaky proteinů kapsidu: symetrie helikální (šroubovicová), ikozahedrální (dvacetistěnová), komplexní, binární (u bakteriofágů; hlavička obsahující NK má ikozahedrální symetrií, dutý bičík sloužící ke vstřikování NK do hostitelské buňky má symetrii helikální)
-
okruh hostitelů a afinita k jejich tkáním:
- okruh hostitelů: živočišné viry - viry obratlovců (včetně člověka) a viry bezobratlých (nejčastěji hmyzu), rostlinné viry, viry hub, řas a prvoků, viry bakterií (bakteriofágy, fágy) a viry fototrofních bakterií (cyanofágy)
- afinita k tkáním: viry respirační, enterální, sexuálně přenosné, hepatické
- Viry jsou zařazeny do řádů s koncovkou virales, čeledí s koncovkou viridae, podčeledí s koncovkou virinae a dále rozlišujeme rody, druhy a varianty.
Některá virová onemocnění:
Rostliny: mozaiková choroba tabáku, brambor, rajčat.
Zvířata: slintavka a kulhavka sudokopytníků, vzteklina, myxomatóza králíků, mor drůbeže.
Člověk: dětská obrna, lidská hepatitida A (Picornaviridae), neštovice (Poxviridae), opary, infekční mononukleóza (Herpesviridae), spalničky, příušnice (Paramyxoviridae), chřipka (Orthomyxoviridae), klíšťová encefalitida, lidská hepatitida C, žlutá zimnice (Flaviviridae, lat. flavus = žlutý), zarděnky (Togaviridae), AIDS (Retroviridae).
Reprodukce virů v hostitelských buňkách:
LYTICKÝ CYKLUS probíhá v 7 krocích:- vazba virionu na povrch buňky: pomocí specifického receptoru
- proniknutí (penetrace) do buňky: celý virion proniká do buňky pinocytózou (živočišné a rostlinné viry), nebo je do buňky vstříknuta pouze NK (u bakteriofágů), u obalených virů splývá jejich vnější obal s plazmatickou membránou buňky a do cytoplazmy se dostává nukleokapsid
- uvolnění NK z kapsidy: enzymatickým rozložením
-
replikace virové NK a genová exprese: liší se v závislosti na typu NK:
- ds(+/-)DNA (u bakteriofágů a živočišných virů) - DNA se replikuje a přepisuje do virové mRNA, podle které jsou syntetizovány proteiny
- ss(+)DNA - nejdříve se nasyntetizuje komplementární řetězec DNA, další průběh jako u dsDNA
- ds(+/-)RNA - k syntéze proteinů slouží jen jedno ze dvou vláken
- ss(+)RNA (u bakteriofágů, živočišných a rostlinných virů) - může přímo sloužit jako mRNA pro syntézu proteinů, jinak dochází k nasyntetizování komplementární (-)RNA, která je matricí pro replikaci (+)RNA, která slouží jako mRNA pro syntézu proteinů nových virionů
- ss(+)RNA se zpětnou transkripci (u živočišných virů - retrovirů), (+)RNA se přepisuje v komplementární ss(-)DNA, podle níž je dosyntetizována komplementární (+)DNA za vzniku ds(+/-)DNA. Oba procesy katalyzuje virová polymeráza reverzní transkriptáza. Dvouřetězcová DNA se začlení do genomu buňky jako provirus, odkud je přepisována do (+)RNA, která slouží k syntéze proteinů nových virionů.
- ss(-)RNA (u bakteriofágů) - nejdříve probíhá syntéza komplementární (+)RNA s následnou tvorbou proteinů, podle (+)RNA se nasyntetizuje (-)RNA, která je součástí nových virionů.
- syntéza virových proteinů: probíhá v cytoplazmě (na ribozomech) hostitelské buňky
- zrání (maturace) virionů: spojování NK s kapsidem
- uvolnění virionů z buňky: exocytózou nebo rozpadem (lýzou) buňky
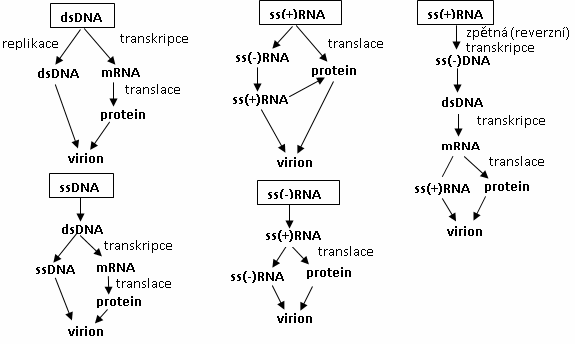
Obr.: Schéma rozdílů genové exprese u různých virů v závislosti na typu jejich nukleové kyseliny.
VIROGENNÍ CYKLUS u živočišných virů (zejména virů čeledi Retroviridae – např. virus HIV) spočívá v začlenění virové NK (DNA) do genomu hostitelské buňky jako tzv. provirus. Provirus může být přenášen z rodičů na potomky, aniž by se infekce projevila. Spontánně nebo účinkem indukčních činitelů (UV paprsky, peroxidy atd.) se provirus vyčlení z chromozomu, a tím je spuštěn lytický cyklus. Virogenní cyklus onkogenních virů může vést i k nádorové transformaci hostitelské buňky.
LYZOGENNÍ CYKLUS (např. u bakteriofágů) je obdobou virogenního cyklu. Do genomu bakterií je začleňována virová NK jako tzv. profág.
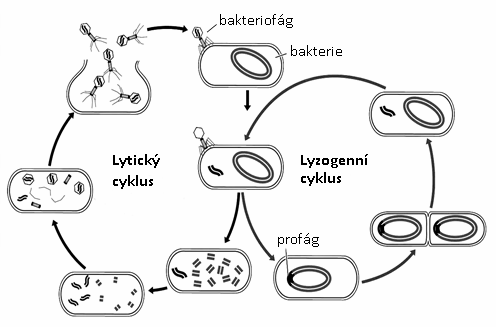
Obr.: Lytický a lyzogenní cyklus u bakteriofágů.
VIROIDY jsou malé infekční cirkulární molekuly RNA bez proteinového obalu. Předpokládá se, že vznikají cirkularizací intronů genů svých eukaryotických hostitelů uvolněných posttranskripčním sestřihem. Nekódují žádný protein, replikují se v jádře buňky pomocí jaderných RNA polymeráz. Vyvolávají onemocnění kulturních rostlin (např. vřetenovitost brambor, onemocnění kokosových palem), která jsou obvykle vázána na určitou lokalitu (první viroidová onemocnění byla objevena až ve 20. století).
SATELITY (VIRUSOIDY) jsou samostatné krátké molekuly nukleových kyselin (DNA či RNA), které vyvolávají onemocnění u rostlin. Byly objeveny teprve roku 1981. Nemohou se replikovat nezávisle, ale vyžadují pomocný virus, v jehož kapsomeře jsou uzavřeny (jsou tedy jakýmisi „parazity jiných virů“). Nekódují žádný protein, replikují se v cytoplazmě.
PRIONY jsou infekční proteiny (bez NK) kódované strukturními geny hostitelského organizmu. Vznikají konformační změnou prionového proteinu PrPC s prostorovou strukturou ?-helix (šroubovice) na PrPSc s ß-strukturou (složeného listu). Priony jsou původci přenosných spongiformních (houbovitý vzhled degenerované tkáně centrální nervové soustavy) encefalopatií. U lidí je to např. Creutzfeldtova-Jakobova choroba a kuru, u zvířat klusavka ovcí a koz (scrapie), bovinní spongiformní encefalopatie (BSE, "nemoc šílených krav") a felinní spongiformní encefalopatie (FSE).
Elektronové mikroskopy
Některé objekty jako např. viry jsou tak malé, že je nelze pozorovat ani nejvýkonnějším optickým mikroskopem s nejlepšími skleněnými čočkami, což zjistil již v 19. století německý fyzik Ernst Abbe. Rozlišovací schopnost optického mikroskopu je totiž omezena vlnovou délkou viditelného světla (400-700 nm). A protože vlnovou délku pro nás viditelného světla neumíme zkrátit, bylo třeba pro posunutí hranice rozlišovací schopnosti mikroskopu najít jiné "světlo" s výrazně kratší vlnovou délkou. A tady začíná příběh elektronového mikroskopu, který byl zkonstruován ve 20. století a umožnil odhalit do té doby skrytá tajemství hmoty. Cesta k jeho sestrojení byla podmíněna technologickým pokrokem a sestávala z postupného propojování objevů mnoha badatelů. Důležitý byl objev elektronu anglickým fyzikem J. J. Thompsonem v roce 1897. Dalším krokem vedoucím k použití elektronů k zobrazení mikrosvěta byl poznatek, který v roce 1925 publikoval Louis de Broglie, že rychle letící elektrony se chovají nejen jako částice, ale mají i vlnový charakter podobně jako viditelné světlo. Protože elektron jako záporně nabitá částice ochotně přispěchá k čemukoliv kladně nabitému, je možné mu tímto způsobem udělit určitou rychlost, které odpovídá konkrétní vlnová délka. Navíc je možné dráhu letícího elektronu ovlivnit silným magnetickým polem podobným způsobem, jako je tomu při průchodu světla optickými čočkami. Tím byla nalezena cesta k novému "světlu" vhodnému pro zkoumání mikrosvěta. Postupně byly sestrojeny dva typy elektronových mikroskopů (transmisní a rastrovací), které využívají urychlené elektrony, a které posunuly hranici rozlišovací schopnosti do rozměru desetin nanometru, tj. na úroveň velikosti atomů. První transmisní elektronový mikroskop sestrojili v roce 1931 němečtí vědci Max Knoll a Ernst Ruska. Teprve v roce 1986 dostal Ernst Ruska za konstrukci transmisního elektronového mikroskopu Nobelovu cenu. Rastrovací elektronový mikroskop se na trhu objevil až v roce 1965.
O rozvoj elektronové mikroskopie se zasloužil i český vědec Armin Delong (brněnský profesor, rodák z Bartovic u Ostravy), který uvedl první elektronový mikroskop do výroby už v roce 1949. V roce 2005 mu byla udělena Národní cena vlády České republiky Česká hlava.
Elektronové mikroskopy mohou dosahovat až 1 000 000× násobného zvětšení a jejich rozlišovací schopnost se pohybuje na hranici 2 – 20 nm, čímž umožňují pozorovat např. viry, které mají průměrnou velikost kolem 50 nm (do tečky za touto větou by se vešly stovky tisíc virů). V elektronovém mikroskopu se místo světelných paprsků pohybují elektrony (od toho název elektronový mikroskop), jejichž průchod mikroskopem je ovlivňován ne skleněnými, ale ektromagnetickými čočkami.
TRANSMISNÍ (PROZAŘOVACÍ) ELEKTRONOVÝ MIKROSKOP (TEM) je zařízení, které se vejde do menší místnosti. Jeho nejnápadnější částí je tubus (asi metr dlouhá svislá dutá trubice), kterým procházejí elektrony. Ty jsou v horní části tubusu uvolňovány elektronovým dělem (nejčastěji rozžhavené wolframové vlákno - katoda), jehož pracovní teplota je okolo 2500 °C. Aby vlákno neshořelo, musí být prostor elektronového děla zbaven vzduchu. Stejně tak musí být vzduch vyčerpán i z ostatních prostorů, kterými elektrony na své pouti tubusem procházejí. Uvolněné elektrony jsou urychleny působením kladně nabité anody a získají rychlost (až polovinu rychlosti světla), která je nezbytná k prolétnutí celým tubusem. Zhruba v jeho polovině jim stojí v cestě vzorek, jímž musí proniknout. Elektrony, které jsou vzorkem zachyceny, nedopadnou a nerozzáří stínítko na dně tubusu, čímž vzniknou stíny vytvářející mnohonásobně zvětšený obraz vzorku. Průchod elektronového paprsku tubusem je ovlivňován elektromagnetickými čočkami. V horní části tubusu se nachází kondenzorové čočky, řídící sílu a průměr elektronového svazku. Pod vzorkem je umístěn objektiv (nejvýkonnější čočka), který zaostřuje svazek elektronů na vzorek a zvětšuje obraz asi 50×. O zvětšování obrazu na požadovanou hodnotu se postarají další čočky (projektor resp. projektiv) umístěné pod objektivem. Ke zviditelnění obrazu neseného elektrony slouží stínítko na dně tubusu. Je tvořeno fluorescenční látkou, která se po dopadu elektronů rozzáří v závislosti na množství a energii dopadajících elektronů. Obraz, který na něm elektrony vytvoří, je možné pozorovat mikroskopem, zaznamenat na fotografický materiál uložený pod stínítkem nebo pomocí speciální CCD kamery (Charge Coupled Device – nábojově vázaný prvek) jej přenést do počítače v digitalizované podobě.
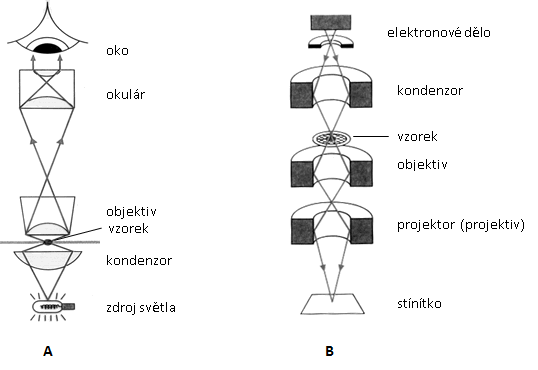
Obr.: A - Směr pohybu světelných paprsků ve světelném mikroskopu; B - Směr pohybu elektronů v elektronovém mikroskopu (TEM).
Velké požadavky jsou kladeny na vzorek, který nesmí obsahovat vodu, protože by se v prostoru zbaveném vzduchu vypařovala. Tloušťka vzorku by se měla pohybovat do 100 nanometrů, tak aby jím mohly elektrony procházet. Vzorek o velikosti 1 × 1 mm se zaleje do speciální pryskyřice a po vytvrzení se ze vzniklého bločku na ultramikrotonu odkrajují ultratenké řezy, které se pak pokrývají tenkou vrstvou těžkého kovu nebo jeho oxidu. Obraz pořízený v elektronovém mikroskopu je černobílý, ale pomocí počítačového programu je možné získat i barevný obraz dle vlastního výběru.
RASTROVACÍ (SKENOVACÍ) ELEKTRONOVÝ MIKROSKOP (SEM) získal své jméno na základě skutečnosti, že elektronový svazek jako velmi jemný hrot přejíždí po povrchu vzorku a skenuje ho. Svazek se pohybuje v řádcích podobně jako při zapisování signálu na televizní obrazovce. Při dopadu elektronů jsou z povrchu vzorku vyraženy sekundární elektrony, které jsou zachyceny detektorem. Povrch vzorku je nutné upravit podobně jako u transmisního mikroskopu. Tento typ mikroskopu je oblíbeným nástrojem pro pozorování mikrosvěta díky schopnosti poskytnout velmi plastický obraz s vysokou hloubkou ostrosti (trojrozměrný obraz) i z tak členitých objektů, jakými je např. hmyz.
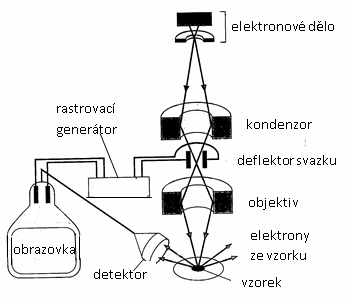
Obr.: Směr pohybu elektronů v elektronovém mikroskopu (SEM).
Mezi světelnými a elektronovými mikroskopy jsou určité analogie a určité rozdíly:
Světelné mikroskopy – využívají jako zdroj zobrazení světlo, světelný paprsek se pohybuje optickou soustavou mikroskopu, kterou tvoří skleněné čočky, rozlišovací schopnost je 0,2 µm, zvětšení max. 1000×, výhodou je, že lze pozorovat i nativní preparáty bez složité úpravy nebo fixace, pozorovaný obraz může být barevný.
Elektronové mikroskopy – využívají jako zdroj zobrazení elektrony, jejichž proud je usměrňován elektromagnety, rozlišovací schopnost je 2 – 20 nm, zvětšení max. 1 000 000×, nevýhodou je vysoká cena elektronových mikroskopů, složitá úprava vzorků, nutnost fixace a nemožnost pozorovat živé objekty, obraz pořízený z mikroskopu je černobílý, výhodou je možnost pořízení trojrozměrného obrazu (pomoci SEM).
Kontrolní otázky – metody molekulární biologie
- Co patří mezi nebuněčné formy života?
- Jaké je chemické složení virů, prionů, viroidů a virusoidů?
- Znáš příklady virového a prionového onemocnění?
- Jaká je velikost virů?
- Jak probíhá reprodukce virů v buňce?
- Jaký je rozdíl mezi lytickým a lyzogenním cyklem?
- Jak probíhá genová exprese u virů v závislosti na typu nukleové kyseliny?
- Jaké jsou dva typy elektronových mikroskopů?
- Jaký je rozdíl mezi světelným a elektronovým mikroskopem?
- Jaký je rozdíl mezi transmisním a rastrovacím elektronovým mikroskopem?
- Jaké je zvětšení a rozlišovací schopnost elektronových mikroskopů?
- Jak je třeba upravit vzorek před pozorováním v el. mikroskopu?
ÚKOLY - Nebuněčné formy života (viz úkoly)
Nebuněčné formy života
Úkol 1: Viry
Nakreslete si do sešitu alespoň 3 zástupce různých druhů virů. Můžete si vybrat virus známého onemocnění nebo virus, kde je patrný vztah mezi vzhledem a názvem - např. filovirus (filum = vlákno), kalicivirus (calyx = kalich), coronavirus (corona = koruna, věnec), parvovirus (parvus = malý), toga (toga = plášť, obal).
Obr.: Někteří zástupci virů.
Fyzikální a chemické vlivy vnějšího prostředí
FYZIKÁLNÍ VLIVY
Teplota - vysoké teploty způsobují denaturaci proteinů, naopak teploty pod bodem mrazu způsobují krystalizaci vody v buňce spojenou s jejím mechanickým poškozením.
Fotodynamie je jev, který vyvolávají některé látky, tzv. fotodynamická barviva (fagopyrin, hypericin obsažen v třezalce, eosin, akridin, fluorescein, porfyriny, chlorofyl), která způsobí zcitlivění organizmu na světlo. Vzniklá nemoc ze světla (např. fagopyrizmus skotu po zkrmení pohanky), může mít i letální následky. Princip fotodynamie spočívá v tom, že látky s fotodynamickým účinkem jsou barevné, nebo jsou v organizmu metabolizovány za vzniku barevných derivátů nebo metabolitů. Světlo je v povrchových tkáních organizmu absorbováno v relativně silné vrstvě a při běžných intenzitách záření je teplo produkované při absorpci fotonů v oblasti viditelného nebo ultrafialového spektra odváděno bez významnějšího patologického vlivu na tkáně. Je-li ovšem podkožní tkáň prostoupena barvivem, dochází k pohlcení tohoto záření v relativně slabé vrstvě, která se silně přehřívá. Tkáň reaguje uvolněním látek charakteristických pro zánět (histamin, bradykinin aj.), což se projeví lokálním zánětem. Při ozáření celého těla dochází k ataku na centrální nervový systém, což se projeví vznikem křečí, narušením celkového zdravotního stavu a následnou smrtí.
UV záření usmrcuje buňky velmi rychle (využití při sterilizaci). Největší účinek má záření o vlnové délce 260 nm, které je specificky absorbováno nukleovými kyselinami a způsobuje vznik tyminových dimerů a následné znemožnění replikace a transkripce.
Ionizující záření - účinek záření závisí na množství ionizací, vyvolaných podél stopy paprsku. Čím větší je rychlost částice, tím menší je množství vzniklých iontů. Částice α, které mají malou rychlost, vyvolávají velké množství ionizace podél krátké dráhy a mají tedy na buňku velký efekt. Paprsky γ, které pronikají organizmem větší rychlostí, poškozují menší počet buněk, ale zasahují i hluboko uložené tkáně. Hlavním mechanizmem účinku ionizujícího záření je tvorba velmi reaktivních volných radikálů (především H+ a OH-).
CHEMICKÉ VLIVY
Jedy (toxiny) jsou chemické látky, které způsobují porušení funkcí buňky nebo její smrt. Toxiny mohou působit na několika úrovních: syntéza biopolymerů (narušení syntézy buněčné stěny bakterií účinkem antibiotik - penicilinu, toxický účinek pro bakterie ne pro eukaryota), transportní funkce buněčných membrán (porušení soudržnosti membrán účinkem fosfolipáz včelího a hadího jedu nebo účinkem povrchově aktivních látek jako jsou saponiny, detergenty), energetický metabolizmus (poruchy syntézy ATP účinkem kyanidů a barbiturátů), buněčný cyklus (zastavení mitózy účinkem mitotického jedu kolchicinu).
Oligodynamie je schopnost některých poměrně stálých kovů (Au, Ag, Zn, Hg, Cu) emitovat ve vodním prostředí ionty, přestože tyto látky mohou být ve vodě nerozpustné. Tyto ionty nepříznivě ovlivňují jednobuněčné organizmy (např. nálevníky).
Fytoncidy jsou těkavé látky, které se vyskytují u vyšších aromatických rostlin (cibule, česnek, křen atd.) a mají antibakteriální, antimykotické a antivirové účinky. Např. v cibuli jsou obsaženy fytoncidy alliin a allicin. Velmi citlivými k fytoncidům jsou prvoci v senném nálevu a některý hmyz.
BUNĚČNÝ STRES je negativní působení vnějších faktorů na buňku.
STRESOVÉ FAKTORY (STRESORY) mohou být fyzikální, chemické nebo biologické, porušující životní procesy v buňkách.
Působení stresorů:
- specifické - ovlivnění pouze některé struktury či funkce buňky např. enzymové jedy blokují aktivitu některého enzymu, mikrotubulární toxiny zabrání vazbou na tubulin jeho polymerizaci v mikrotubuly atd.
- nespecifické - např. denaturace všech proteinů při teplotě nad 100 oC, účinkem těžkých kovů, kyselin, aldehydů a dalších chemických látek
Účinek stresorů:
- cytocidní – zánik buňky, tzv. nekróza
- cytostatický – zastavení buněčného cyklu
- mitoklastický – narušení průběhu mitózy
- genotoxický (mutagenní) – změna genetické informace
STRESOVÉ PROTEINY jsou proteiny syntetizované buňkou jako obranná reakce proti stresu. Některé proteiny tepelného šoku např. HSP60 (heat shock protein o velikost 60 kD) u Escherichia coli chrání buněčné proteiny před poškozením (denaturací) při zvýšené teplotě.
Kontrolní otázky – vlivy vnějšího prostředí
- Co patří mezi stresory?
- Jaký může být účinek stresorů?
- Co je to fotodynamie?
- Co patří mezi fotodynamická barviva a jaký je jejich účinek?
- Jaký je účinek ionizující záření na varle potkana?
- Co je to oligodynamie?
- Co jsou to fytoncidy a jaký je jejich účinek?
ÚKOLY - Fyzikální a chemické vlivy vnějšího prostředí (viz úkoly)
Fyzikální a chemické vlivy vnějšího prostředí
Úkol 1: Fotodynamie
NP: senný nálev, eosin
Připravte si 2 podložní sklíčka. Na jedno dejte kapku senného nálevu a k tomu přidejte kapku eosinu a preparát umístěte do tmy (první kontrola). Na druhé sklíčko dejte dvě kapky senného nálevu: jedna z nich bude bez eosinu (druhá kontrola), k druhé kapce přidejte eosin (vlastní pokus) a sklíčko umístěte na denní světlo. Preparáty prohlížejte zhruba každé 3 min. a porovnejte, co se děje s nálevníky ve vlastním pokusu a ve dvou kontrolách. V preparátu na světle je možno pozorovat nejdříve podráždění (excitaci), které se projevuje zrychlením pohybu nálevníků. Po excitaci dochází ke zpomalení pohybu, až k jeho zastavení a úhynům prvoků.
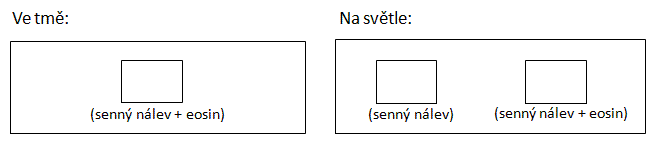
Úkol 2: Vliv ionizujícího záření na varle potkana
TP: varle potkana (normální tkáň a tkáň po ozáření dávkou 6,5 Gy = grayů), barvený hematoxylin-eosinem
Nejprve si prohlédněte a nakreslete normální tkáň a poté tkáň po ozáření při malém a pak i při větším zvětšení. Porovnejte hustotu semenotvorných kanálků, jejich strukturu, tvar buněk a barvitelnost jader.
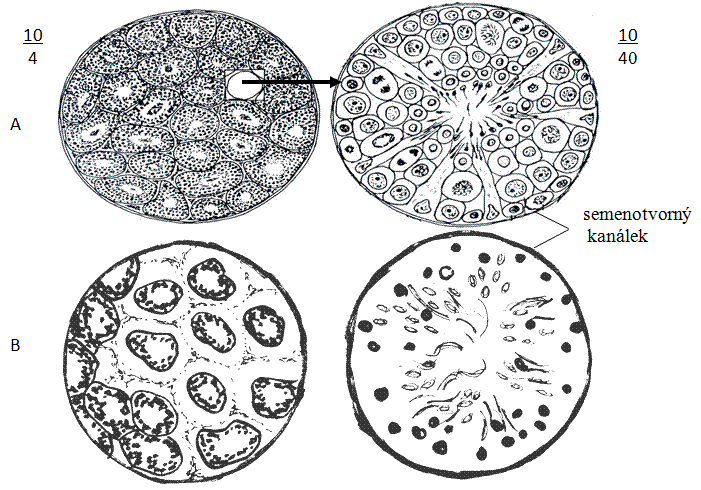
Obr.: Porovnání struktury varlete a semenotvorného kanálku potkana: A – před ozářením (při malém a větším zvětšení), B – po ozáření (při malém a větším zvětšení).
Úkol 3: Oligodynamie
NP: senný nálev, voda nad rtutí
Na podložní sklo naneste kapku vody, pod níž byla uchovávaná rtuť, a do ní přidejte kapku senného nálevu. Pozorujte preparát s nálevníky každé 3 min. a porovnejte s kontrolní skupinou prvoků v čisté vodě. Nejprve dojde k excitaci prvoků, pak k útlumu pohybu a nakonec k úhynu. Zaznamenejte výsledky pozorování.
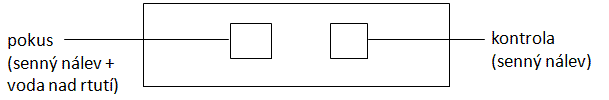
Úkol 4: Vliv CdCl2 na varle potkana
TP: varle potkana (normální tkáň a tkáň potkana, kterému byl aplikován CdCl2), barvený hematoxylin-eosinem
Prohlédněte si a porovnejte preparát varlete potkana po účinku CdCl2 s kontrolním preparátem. Všimněte si snížení počtu spermiotvorných buněk a zvýšení počtu doprovodných buněk (Sertoliho buňky) a zakreslete rozdíly.
Úkol 5: Vliv fytoncidů na nálevníky
NP: senný nálev, cibule
Nakrájejte cibuli na malé kousky a rozetřete v třecí misce s mořským pískem na jemnou kašovitou hmotu. Na podložní sklíčko kápněte senný nálev a zkontrolujte přítomnost nálevníků. Preparát umístěte na podložku do Petriho misky, na jejímž dně je přidaná rozdrcená cibule. Po 3-5 min kontrolujte pohyblivost nálevníků v Petriho misce i v paralelně připravené kontrole mimo Petriho misku. Zaznamenejte výsledky pozorování.
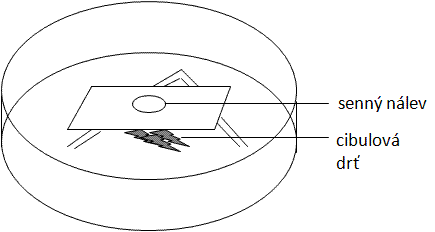
Tyto výukové materiály byly spolufinancovány Evropským sociálním fondem a státním rozpočtem ČR.

OPVK
Veterinární a farmaceutická univerzita BrnoPalackého tř. 1/3
tel.: +420 54156 1111
IČ 62157124
Obsah
- Na úvod aneb co vás čeká
- Metody získávání informací v biologických vědách
- Lupy a mikroskopy
- Mikroskopická technika
- Biologie
- Chemické složení bioplazmy
- Prokaryota, zastavení objektu pod imerzí
- Eukarya – živočišná buňka, protozoa
- Eukarya – rostlinná buňka
- Pohyb a taxe, nativní preparáty
- Vyšetření krve
- Buněčný cyklus, mitóza
- Rozmnožování a vývoj
- Modelový organismus
- Cytogenetika
- Metody molekulární biologie
- Buněčné a tkáňové kultury
- Nebuněčné formy života, elektronové mikroskopy
- Fyzikální a chemické vlivy vnějšího prostředí
- Genetika
- Mendelismus, monohybridismus
- Dihybridismus, polyhybridismus a rozvětvovací metoda
- Polymorfní geny
- Dědičnost a pohlaví
- Genové interakce
- Vazba genů
- Nemendelistická dědičnost
- Kvantitativní genetika
- Populační genetika


