Průkaz Salmonella spp. v potravinách
Princip metody:
Zkoušený vzorek se inokuluje do tekuté půdy pro neselektivní pomnožení – pufrovaná peptonová voda (PPV médium) a inkubuje se aerobně při 37 °C po dobu 16 – 20 hodin. Získaná kultura se přeočkuje do dvou tekutých selektivních půd – Rappaport Vassiliadis sója médium (RVS médium) a Mueller-Kauffman tetrationát novobiocin médium (MKTTn médium). RVS médium se inkubuje aerobně při 42 °C po dobu 24 hodin a MKTTn médium při 37 °C po dobu 24 hodin. Ze selektivního pomnožení se provádí vyočkování na dvě pevné selektivní půdy – agar s xylózou, lyzinem a deoxycholátem (XLD agar) a kteroukoli jinou selektivní půdu např. agar s fenolovou červení a brilantovou zelení (BR agar) nebo chromogenní agar pro stanovení salmonel (např. Rambach agar, IRIS Salmonella agar. Inokulované misky se inkubují aerobně při 37 °C po dobu 24 – 48 hodin a zjišťuje se přítomnost suspektních kolonií bakterií rodu Salmonella. Následně se provede biochemická a sérologická konfirmace vybraných suspektních kolonií. Výsledkem je průkaz přítomnosti či absence bakterií rodu Salmonella v navážce vyšetřovaného vzorku.
Postup metody:
Neselektivní pomnožení: odebereme zkušební vzorek (obvykle 25 g nebo 25 ml) a připravíme výchozí ředění, jako ředící roztok použijeme devítinásobné množství (tj. 225 ml) PPV média. Inkubujeme aerobně v termostatu při 37 °C po dobu 16 – 20 hodin.
Selektivní pomnožení: po ukončení inkubace přeneseme 0,1 ml výchozí suspenze do zkumavky s 10 ml RVS půdy a inkubujeme aerobně v termostatu při 42 °C po dobu 24 hodin. Souběžně přeneseme 1 ml výchozí suspenze do zkumavky s 10 ml MKTTn půdy a inkubujeme aerobně v termostatu při 37 °C po dobu 24 hodin.
Izolace: z obou půd pro selektivní pomnožení provedeme vyočkování sterilní bakteriologickou kličkou na dvě selektivní půdy. Povinnou půdou je XLD agar, druhá selektivní půda se volí dle zvyklostí laboratoře (např. BR agar). Inokulované Petriho misky obrátíme dnem vzhůru a inkubujeme aerobně v termostatu při 37 °C po dobu 24 – 48 hodin.
Při hodnocení sledujeme nárůst kolonií suspektních pro bakterie rodu Salmonella. Pro konfirmaci vybereme náhodně z každé plotny 5 suspektních kolonií.
Kolonie vybrané pro konfirmaci subkultivujeme vyočkováním na masopeptonový agar (MPA). Při biochemické konfirmaci standardně provedeme následující testy: růst na TSI agaru, průkaz štěpení močoviny, průkaz lyzindekarboxylázy, průkaz β-galaktozidázy, VP test a průkaz tvorby indolu. Pro biochemickou konfirmaci je dovoleno použít komerční identifikační soupravy. Po biochemické identifikaci následuje sérologická konfirmace a sérotypizace, která je zaměřena na průkaz O, H a Vi antigenů sklíčkovou aglutinací.
Na základě výsledků konfirmace potvrdíme nebo vyloučíme přítomnost bakterií rodu Salmonella v navážce vyšetřovaného vzorku.
Schéma – průkaz Salmonella spp. v potravinách:
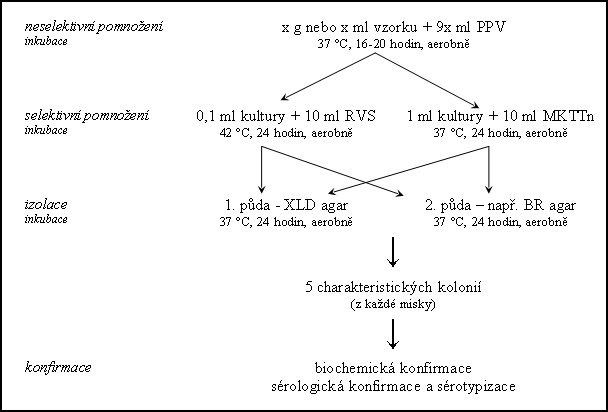
Morfologie charakteristických kolonií:
XLD agar – kolonie laktóza negativních bakterií (salmonely) jsou průsvitné s černým středem o průměru 2 mm a v jejich okolí dochází ke změně barvy půdy z oranžové do červena; Kolonie laktóza pozitivních bakterií (koliformní bakterie) jsou jasně žluté barvy někdy s černým středem o průměru 2 mm obklopené žlutou zónou.
BR agar – kolonie laktóza negativních bakterií (salmonely) jsou průsvitné o průměru 2 mm a v jejich okolí dochází ke změně barvy půdy do pivoňkově červena; Kolonie laktóza pozitivních bakterií (koliformní baktérie) jsou jasně žlutozelené barvy o průměru 2 mm, podobně se barví i půda v okolí kolonií.
Rambach agar – typické kolonie salmonel rostou jasně červeně, ostatní v odstínech od vínové až po modrou. Velikost kolonií je kolem 1,5 mm.
IRIS Salmonella agar – typické kolonie salmonel mají tmavě purpurovou barvu a velikost kolem 1,5 mm. E. coli roste v bezbarvých koloniích, Enterobacter spp. v modrých koloniích, růst pseudomonád je inhibován.