Nebuněčné formy života, elektronové mikroskopy
Nebuněčné formy života
Mezi nebuněčné formy života patří viry (nukleové kyselina a proteiny), viroidy, virusoidy (nukleové kyseliny) a priony (proteiny).
VIRY jsou submikroskopické částice, jejichž velikost se pohybuje v desítkách až stovkách nanometrů. Genom u nejmenších virů je tvořen 3 500 nukleotidy (RNA-bakteriofág R17) a 3 strukturními geny kódující protein kapsidy, protein pro absorpci viru na hostitelskou buňku a specifickou RNA-polymerázu. Největším nově objeveným virem je Mimivirus z čeledi Mimiviridae (virus "napodobuje" bakterie), který byl zjištěn uvnitř buněk měňavky, měří 400 nm, jeho genetický kód se skládá z 800 000 nukleotidů a obsahuje až 900 genů.
Virion je jednotlivá částice (partikule), schopná infikovat hostitelskou buňku a množit se v ní. Je složen z nukleokapsidu, tj. nukleové kyseliny (NK), a to buď deoxyribonukleové (DNA), nebo ribonukleové (RNA) a z kapsidy, což je proteinový obal složený z proteinových molekul (kapsomer).
Obalené viry při zrání (maturaci) získávají membránový obal, který je odvozen z plazmatické nebo jaderné membrány (nebo z obou) hostitelské buňky, která je virem modifikována. Na povrchu obalu mohou být z glykoproteinů vytvořeny ostré výčnělky, tzv. hroty (peplomery), které udílí viru antigenní vlastnosti a jsou pro určité viry specifické.
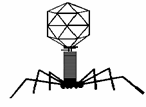
Bakteriofág (zkráceně fág, "požírač bakterií") je virus infikující bakterie. Proteinová kapsida je složená z hlavičky obsahující nukleovou kyselinu (DNA, RNA) a z bičíku, ze kterého vyrůstají bičíková vlákna, která slouží k přichycení. Tyto viry mohou lyzovat napadené bakterie a lze je tak využít k antibakteriální léčbě. Po infekci bakterie může bakteriofág přejít do latentního (lyzogenního) stavu, kdy se začlení do genetické informace buňky ve formě tzv. profága. Teprve při „stresu“ bakteriální buňky se virus aktivuje, začne se replikovat a buňku zlyzuje. Byly popsány i případy, kdy se kmeny bakterií se začleněnou virovou DNA stanou vysoce patogenními původci onemocnění.
Pro taxonomii a systematiku virů jsou důležité tyto znaky:
- rozměry a morfologie virionu
- přítomnost (nepřítomnost) povrchového obalu: obalené a neobalené viry
-
typ a molekulární stavba genomové NK:
- typ NK: RNA-viry, DNA-viry
- počet a tvar řetězců NK: ssRNA - jednořetězcová (z angl. single stranded), dsRNA -dvouřetězcová (z angl. double stranded), ssDNA, dsDNA, lineární (většinou) nebo kružnicová NK
- polarita řetězce NK: (+)RNA (plus RNA, pozitivní RNA, stejná polarita jako mRNA), (-)RNA (minus RNA, negativní RNA), (+)DNA, (-)DNA.
- znaky proteinů kapsidu: symetrie helikální (šroubovicová), ikozahedrální (dvacetistěnová), komplexní, binární (u bakteriofágů; hlavička obsahující NK má ikozahedrální symetrií, dutý bičík sloužící ke vstřikování NK do hostitelské buňky má symetrii helikální)
-
okruh hostitelů a afinita k jejich tkáním:
- okruh hostitelů: živočišné viry - viry obratlovců (včetně člověka) a viry bezobratlých (nejčastěji hmyzu), rostlinné viry, viry hub, řas a prvoků, viry bakterií (bakteriofágy, fágy) a viry fototrofních bakterií (cyanofágy)
- afinita k tkáním: viry respirační, enterální, sexuálně přenosné, hepatické
- Viry jsou zařazeny do řádů s koncovkou virales, čeledí s koncovkou viridae, podčeledí s koncovkou virinae a dále rozlišujeme rody, druhy a varianty.
Některá virová onemocnění:
Rostliny: mozaiková choroba tabáku, brambor, rajčat.
Zvířata: slintavka a kulhavka sudokopytníků, vzteklina, myxomatóza králíků, mor drůbeže.
Člověk: dětská obrna, lidská hepatitida A (Picornaviridae), neštovice (Poxviridae), opary, infekční mononukleóza (Herpesviridae), spalničky, příušnice (Paramyxoviridae), chřipka (Orthomyxoviridae), klíšťová encefalitida, lidská hepatitida C, žlutá zimnice (Flaviviridae, lat. flavus = žlutý), zarděnky (Togaviridae), AIDS (Retroviridae).
Reprodukce virů v hostitelských buňkách:
LYTICKÝ CYKLUS probíhá v 7 krocích:- vazba virionu na povrch buňky: pomocí specifického receptoru
- proniknutí (penetrace) do buňky: celý virion proniká do buňky pinocytózou (živočišné a rostlinné viry), nebo je do buňky vstříknuta pouze NK (u bakteriofágů), u obalených virů splývá jejich vnější obal s plazmatickou membránou buňky a do cytoplazmy se dostává nukleokapsid
- uvolnění NK z kapsidy: enzymatickým rozložením
-
replikace virové NK a genová exprese: liší se v závislosti na typu NK:
- ds(+/-)DNA (u bakteriofágů a živočišných virů) - DNA se replikuje a přepisuje do virové mRNA, podle které jsou syntetizovány proteiny
- ss(+)DNA - nejdříve se nasyntetizuje komplementární řetězec DNA, další průběh jako u dsDNA
- ds(+/-)RNA - k syntéze proteinů slouží jen jedno ze dvou vláken
- ss(+)RNA (u bakteriofágů, živočišných a rostlinných virů) - může přímo sloužit jako mRNA pro syntézu proteinů, jinak dochází k nasyntetizování komplementární (-)RNA, která je matricí pro replikaci (+)RNA, která slouží jako mRNA pro syntézu proteinů nových virionů
- ss(+)RNA se zpětnou transkripci (u živočišných virů - retrovirů), (+)RNA se přepisuje v komplementární ss(-)DNA, podle níž je dosyntetizována komplementární (+)DNA za vzniku ds(+/-)DNA. Oba procesy katalyzuje virová polymeráza reverzní transkriptáza. Dvouřetězcová DNA se začlení do genomu buňky jako provirus, odkud je přepisována do (+)RNA, která slouží k syntéze proteinů nových virionů.
- ss(-)RNA (u bakteriofágů) - nejdříve probíhá syntéza komplementární (+)RNA s následnou tvorbou proteinů, podle (+)RNA se nasyntetizuje (-)RNA, která je součástí nových virionů.
- syntéza virových proteinů: probíhá v cytoplazmě (na ribozomech) hostitelské buňky
- zrání (maturace) virionů: spojování NK s kapsidem
- uvolnění virionů z buňky: exocytózou nebo rozpadem (lýzou) buňky
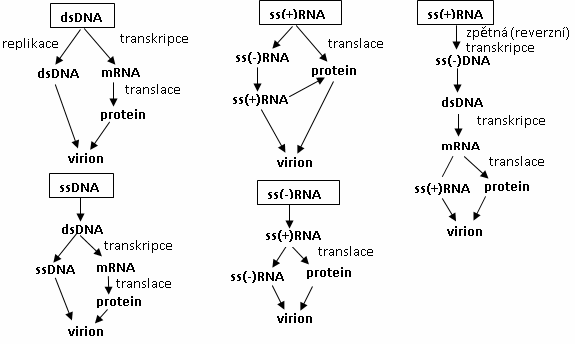
Obr.: Schéma rozdílů genové exprese u různých virů v závislosti na typu jejich nukleové kyseliny.
VIROGENNÍ CYKLUS u živočišných virů (zejména virů čeledi Retroviridae – např. virus HIV) spočívá v začlenění virové NK (DNA) do genomu hostitelské buňky jako tzv. provirus. Provirus může být přenášen z rodičů na potomky, aniž by se infekce projevila. Spontánně nebo účinkem indukčních činitelů (UV paprsky, peroxidy atd.) se provirus vyčlení z chromozomu, a tím je spuštěn lytický cyklus. Virogenní cyklus onkogenních virů může vést i k nádorové transformaci hostitelské buňky.
LYZOGENNÍ CYKLUS (např. u bakteriofágů) je obdobou virogenního cyklu. Do genomu bakterií je začleňována virová NK jako tzv. profág.
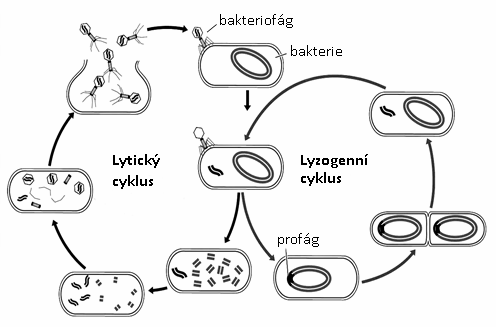
Obr.: Lytický a lyzogenní cyklus u bakteriofágů.
VIROIDY jsou malé infekční cirkulární molekuly RNA bez proteinového obalu. Předpokládá se, že vznikají cirkularizací intronů genů svých eukaryotických hostitelů uvolněných posttranskripčním sestřihem. Nekódují žádný protein, replikují se v jádře buňky pomocí jaderných RNA polymeráz. Vyvolávají onemocnění kulturních rostlin (např. vřetenovitost brambor, onemocnění kokosových palem), která jsou obvykle vázána na určitou lokalitu (první viroidová onemocnění byla objevena až ve 20. století).
SATELITY (VIRUSOIDY) jsou samostatné krátké molekuly nukleových kyselin (DNA či RNA), které vyvolávají onemocnění u rostlin. Byly objeveny teprve roku 1981. Nemohou se replikovat nezávisle, ale vyžadují pomocný virus, v jehož kapsomeře jsou uzavřeny (jsou tedy jakýmisi „parazity jiných virů“). Nekódují žádný protein, replikují se v cytoplazmě.
PRIONY jsou infekční proteiny (bez NK) kódované strukturními geny hostitelského organizmu. Vznikají konformační změnou prionového proteinu PrPC s prostorovou strukturou ?-helix (šroubovice) na PrPSc s ß-strukturou (složeného listu). Priony jsou původci přenosných spongiformních (houbovitý vzhled degenerované tkáně centrální nervové soustavy) encefalopatií. U lidí je to např. Creutzfeldtova-Jakobova choroba a kuru, u zvířat klusavka ovcí a koz (scrapie), bovinní spongiformní encefalopatie (BSE, "nemoc šílených krav") a felinní spongiformní encefalopatie (FSE).
Elektronové mikroskopy
Některé objekty jako např. viry jsou tak malé, že je nelze pozorovat ani nejvýkonnějším optickým mikroskopem s nejlepšími skleněnými čočkami, což zjistil již v 19. století německý fyzik Ernst Abbe. Rozlišovací schopnost optického mikroskopu je totiž omezena vlnovou délkou viditelného světla (400-700 nm). A protože vlnovou délku pro nás viditelného světla neumíme zkrátit, bylo třeba pro posunutí hranice rozlišovací schopnosti mikroskopu najít jiné "světlo" s výrazně kratší vlnovou délkou. A tady začíná příběh elektronového mikroskopu, který byl zkonstruován ve 20. století a umožnil odhalit do té doby skrytá tajemství hmoty. Cesta k jeho sestrojení byla podmíněna technologickým pokrokem a sestávala z postupného propojování objevů mnoha badatelů. Důležitý byl objev elektronu anglickým fyzikem J. J. Thompsonem v roce 1897. Dalším krokem vedoucím k použití elektronů k zobrazení mikrosvěta byl poznatek, který v roce 1925 publikoval Louis de Broglie, že rychle letící elektrony se chovají nejen jako částice, ale mají i vlnový charakter podobně jako viditelné světlo. Protože elektron jako záporně nabitá částice ochotně přispěchá k čemukoliv kladně nabitému, je možné mu tímto způsobem udělit určitou rychlost, které odpovídá konkrétní vlnová délka. Navíc je možné dráhu letícího elektronu ovlivnit silným magnetickým polem podobným způsobem, jako je tomu při průchodu světla optickými čočkami. Tím byla nalezena cesta k novému "světlu" vhodnému pro zkoumání mikrosvěta. Postupně byly sestrojeny dva typy elektronových mikroskopů (transmisní a rastrovací), které využívají urychlené elektrony, a které posunuly hranici rozlišovací schopnosti do rozměru desetin nanometru, tj. na úroveň velikosti atomů. První transmisní elektronový mikroskop sestrojili v roce 1931 němečtí vědci Max Knoll a Ernst Ruska. Teprve v roce 1986 dostal Ernst Ruska za konstrukci transmisního elektronového mikroskopu Nobelovu cenu. Rastrovací elektronový mikroskop se na trhu objevil až v roce 1965.
O rozvoj elektronové mikroskopie se zasloužil i český vědec Armin Delong (brněnský profesor, rodák z Bartovic u Ostravy), který uvedl první elektronový mikroskop do výroby už v roce 1949. V roce 2005 mu byla udělena Národní cena vlády České republiky Česká hlava.
Elektronové mikroskopy mohou dosahovat až 1 000 000× násobného zvětšení a jejich rozlišovací schopnost se pohybuje na hranici 2 – 20 nm, čímž umožňují pozorovat např. viry, které mají průměrnou velikost kolem 50 nm (do tečky za touto větou by se vešly stovky tisíc virů). V elektronovém mikroskopu se místo světelných paprsků pohybují elektrony (od toho název elektronový mikroskop), jejichž průchod mikroskopem je ovlivňován ne skleněnými, ale ektromagnetickými čočkami.
TRANSMISNÍ (PROZAŘOVACÍ) ELEKTRONOVÝ MIKROSKOP (TEM) je zařízení, které se vejde do menší místnosti. Jeho nejnápadnější částí je tubus (asi metr dlouhá svislá dutá trubice), kterým procházejí elektrony. Ty jsou v horní části tubusu uvolňovány elektronovým dělem (nejčastěji rozžhavené wolframové vlákno - katoda), jehož pracovní teplota je okolo 2500 °C. Aby vlákno neshořelo, musí být prostor elektronového děla zbaven vzduchu. Stejně tak musí být vzduch vyčerpán i z ostatních prostorů, kterými elektrony na své pouti tubusem procházejí. Uvolněné elektrony jsou urychleny působením kladně nabité anody a získají rychlost (až polovinu rychlosti světla), která je nezbytná k prolétnutí celým tubusem. Zhruba v jeho polovině jim stojí v cestě vzorek, jímž musí proniknout. Elektrony, které jsou vzorkem zachyceny, nedopadnou a nerozzáří stínítko na dně tubusu, čímž vzniknou stíny vytvářející mnohonásobně zvětšený obraz vzorku. Průchod elektronového paprsku tubusem je ovlivňován elektromagnetickými čočkami. V horní části tubusu se nachází kondenzorové čočky, řídící sílu a průměr elektronového svazku. Pod vzorkem je umístěn objektiv (nejvýkonnější čočka), který zaostřuje svazek elektronů na vzorek a zvětšuje obraz asi 50×. O zvětšování obrazu na požadovanou hodnotu se postarají další čočky (projektor resp. projektiv) umístěné pod objektivem. Ke zviditelnění obrazu neseného elektrony slouží stínítko na dně tubusu. Je tvořeno fluorescenční látkou, která se po dopadu elektronů rozzáří v závislosti na množství a energii dopadajících elektronů. Obraz, který na něm elektrony vytvoří, je možné pozorovat mikroskopem, zaznamenat na fotografický materiál uložený pod stínítkem nebo pomocí speciální CCD kamery (Charge Coupled Device – nábojově vázaný prvek) jej přenést do počítače v digitalizované podobě.
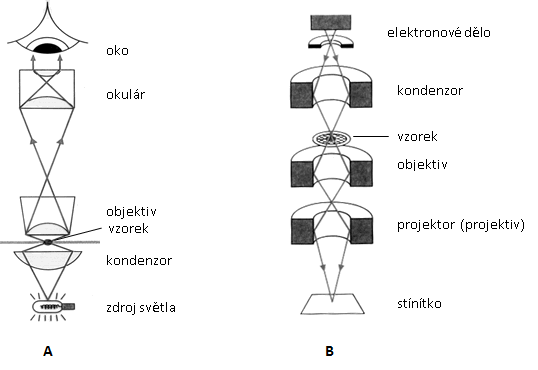
Obr.: A - Směr pohybu světelných paprsků ve světelném mikroskopu; B - Směr pohybu elektronů v elektronovém mikroskopu (TEM).
Velké požadavky jsou kladeny na vzorek, který nesmí obsahovat vodu, protože by se v prostoru zbaveném vzduchu vypařovala. Tloušťka vzorku by se měla pohybovat do 100 nanometrů, tak aby jím mohly elektrony procházet. Vzorek o velikosti 1 × 1 mm se zaleje do speciální pryskyřice a po vytvrzení se ze vzniklého bločku na ultramikrotonu odkrajují ultratenké řezy, které se pak pokrývají tenkou vrstvou těžkého kovu nebo jeho oxidu. Obraz pořízený v elektronovém mikroskopu je černobílý, ale pomocí počítačového programu je možné získat i barevný obraz dle vlastního výběru.
RASTROVACÍ (SKENOVACÍ) ELEKTRONOVÝ MIKROSKOP (SEM) získal své jméno na základě skutečnosti, že elektronový svazek jako velmi jemný hrot přejíždí po povrchu vzorku a skenuje ho. Svazek se pohybuje v řádcích podobně jako při zapisování signálu na televizní obrazovce. Při dopadu elektronů jsou z povrchu vzorku vyraženy sekundární elektrony, které jsou zachyceny detektorem. Povrch vzorku je nutné upravit podobně jako u transmisního mikroskopu. Tento typ mikroskopu je oblíbeným nástrojem pro pozorování mikrosvěta díky schopnosti poskytnout velmi plastický obraz s vysokou hloubkou ostrosti (trojrozměrný obraz) i z tak členitých objektů, jakými je např. hmyz.
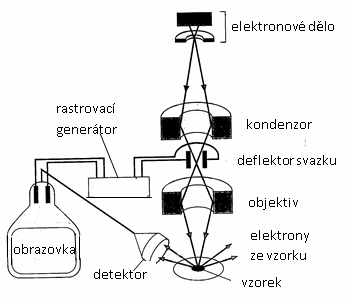
Obr.: Směr pohybu elektronů v elektronovém mikroskopu (SEM).
Mezi světelnými a elektronovými mikroskopy jsou určité analogie a určité rozdíly:
Světelné mikroskopy – využívají jako zdroj zobrazení světlo, světelný paprsek se pohybuje optickou soustavou mikroskopu, kterou tvoří skleněné čočky, rozlišovací schopnost je 0,2 µm, zvětšení max. 1000×, výhodou je, že lze pozorovat i nativní preparáty bez složité úpravy nebo fixace, pozorovaný obraz může být barevný.
Elektronové mikroskopy – využívají jako zdroj zobrazení elektrony, jejichž proud je usměrňován elektromagnety, rozlišovací schopnost je 2 – 20 nm, zvětšení max. 1 000 000×, nevýhodou je vysoká cena elektronových mikroskopů, složitá úprava vzorků, nutnost fixace a nemožnost pozorovat živé objekty, obraz pořízený z mikroskopu je černobílý, výhodou je možnost pořízení trojrozměrného obrazu (pomoci SEM).
Kontrolní otázky – metody molekulární biologie
- Co patří mezi nebuněčné formy života?
- Jaké je chemické složení virů, prionů, viroidů a virusoidů?
- Znáš příklady virového a prionového onemocnění?
- Jaká je velikost virů?
- Jak probíhá reprodukce virů v buňce?
- Jaký je rozdíl mezi lytickým a lyzogenním cyklem?
- Jak probíhá genová exprese u virů v závislosti na typu nukleové kyseliny?
- Jaké jsou dva typy elektronových mikroskopů?
- Jaký je rozdíl mezi světelným a elektronovým mikroskopem?
- Jaký je rozdíl mezi transmisním a rastrovacím elektronovým mikroskopem?
- Jaké je zvětšení a rozlišovací schopnost elektronových mikroskopů?
- Jak je třeba upravit vzorek před pozorováním v el. mikroskopu?
ÚKOLY - Nebuněčné formy života (viz úkoly)
Tyto výukové materiály byly spolufinancovány Evropským sociálním fondem a státním rozpočtem ČR.

OPVK
Veterinární a farmaceutická univerzita BrnoPalackého tř. 1/3
tel.: +420 54156 1111
IČ 62157124
Obsah
- Na úvod aneb co vás čeká
- Metody získávání informací v biologických vědách
- Lupy a mikroskopy
- Mikroskopická technika
- Biologie
- Chemické složení bioplazmy
- Prokaryota, zastavení objektu pod imerzí
- Eukarya – živočišná buňka, protozoa
- Eukarya – rostlinná buňka
- Pohyb a taxe, nativní preparáty
- Vyšetření krve
- Buněčný cyklus, mitóza
- Rozmnožování a vývoj
- Modelový organismus
- Cytogenetika
- Metody molekulární biologie
- Buněčné a tkáňové kultury
- Nebuněčné formy života, elektronové mikroskopy
- Fyzikální a chemické vlivy vnějšího prostředí
- Genetika
- Mendelismus, monohybridismus
- Dihybridismus, polyhybridismus a rozvětvovací metoda
- Polymorfní geny
- Dědičnost a pohlaví
- Genové interakce
- Vazba genů
- Nemendelistická dědičnost
- Kvantitativní genetika
- Populační genetika


