Teorie - Biologie - kompletní přehled (úkoly)
Chemické složení bioplazmy
Úkol 1: Průkaz škrobu
brambor, Lugolův roztok
Rozkrojte bramborovou hlízu a skalpelem setřete tekutinu z řezné plochy a naneste na podložní sklo. Pozorujte tvar excentrických škrobových zrn a zakreslete. Poté přidejte k preparátu Lugolův roztok (2KI + I2 + H2O), přikryjte krycím sklíčkem a znovu pozorujte. Jak se změnila barva škrobových zrn?

Obr.: Škrobová zrna – zásobní rostlinné inkluze.
Úkol 2: Průkaz tuků v bioplazmě
TP: jaterní tkáň s tukovou infiltrací barvená na tuky (Sudan III, olejová červeň)
Zakreslete si jaterní buňku s oranžově zbarveným tukem, který se v buňce nachází v podobě tukových kapének nebo vyplňuje celý obsah buňky.
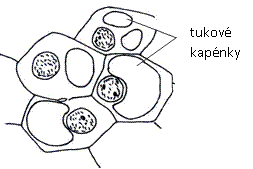
Obr.: Tukové kapénky v jaterních buňkách.
Úkol 3: Průkaz proteinů (Hellerova zkouška – srážecí reakce s koncentrovanou kyselinou dusičnou)
bílek, kys. dusičná
Do zkumavky nalijte asi 2 ml koncentrované kyseliny dusičné a po stěně zkumavky opatrně navrstvěte suspenzi vaječného bílku, tak aby nedošlo k promíchání tekutin. Na styčné ploše obou vrstev se vytvoří bílý prstenec vysrážených (denaturovaných) proteinů.
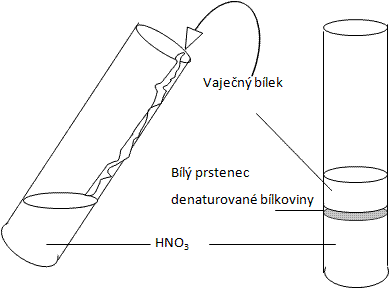
Obr.: Průkaz bílkovin (Hellerova zkouška)
Prokaryota, zastavení objektu pod imerzí
Úkol 1: Příprava trvalého preparátu suchou cestou – roztěr bakterií
bakterie G+ a G-, krystalová violeť, Lugolův roztok, etanol, karbolfuchsin
Nejdříve si vyžíhejte bakteriologickou kličku v plameni a poté proveďte kličkou stěr z povrchu agarové půdy porostlé koloniemi bakterií (zástupci Gram-pozitivních a Gram-negativních bakterií). Obsah kličky homogenizujte v co nejmenší kapce vody na podložním sklíčku, po usušení na vzduchu fixujte nad plamenem (stačí 3x protáhnout nad plamenem roztěrem nahoru) a proveďte barvení preparátu.
Postup barvení dle Grama:
- na sklíčko s roztěrem bakterií kápněte barvivo krystalová violeť (nechat barvit 3 min)
- slijte, opláchněte destilovanou vodou a převrstvěte preparát Lugolovým roztokem (KI + I + H2O) (2 min)
- slijte, opláchněte destilovanou vodou a přidávejte etanol tak dlouho dokud se bude barvivo vyplavovat
- opláchněte destilovanou vodou a převrstvěte karbolfuchsinem (1,5 min)
- opláchněte destilovanou vodou a osušte
Pomůcka pro zapamatování postupu barvení: VLAK (violeť, Lugol, alkohol, karbolfuchsin)
Preparát s obarvenými bakteriemi pozorujte pod imerzním objektivem. Do protokolu si zakreslete a zapište, jak se oba typy bakterií navzájem liší, a to tvarem a zbarvením.
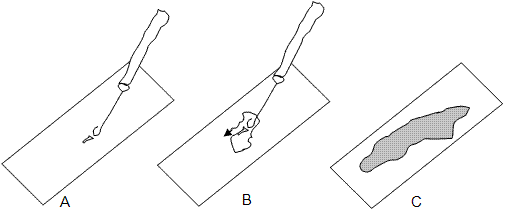
Obr.: Postup zhotovení roztěru bakterií: A – přenos bakterií do kapky vody bakteriologickou kličkou, B – homogenizace, C – hotový roztěr bakterií.
Úkol 2: Pozorování bakterií pod imerzí
TP, NP: zástupci G+ a G- bakterií
Imerzní objektiv slouží k pozorování větších detailů, které již nejsou patrné pod suchými objektivy. Nejdříve je potřeba najít vhodné místo v preparátu při menším zvětšení a umístit objekt do středu zorného pole mikroskopu. Následně je třeba pootočit revolverový měnič do poloviny (mezi objektivy), na krycí sklo nanést kapku imerzního oleje (dostatečně velkou) a dotočit objektiv do optické osy mikroskopu. Tím se spojí čelní čočka objektivu s kapkou imerzního oleje. Další postup: pomocí makroposuvu posunout stolek mikroskopu až do nejvyšší polohy (pozor, ať nepraskne preparát), kontrolovat pohledem ze strany, následně točit makrošroubem opačným směrem, tj. oddalovat stolek s preparátem až se v zorném poli mikroskopu objeví objekt, doostřit mikroposuvem a upravit osvětlení.
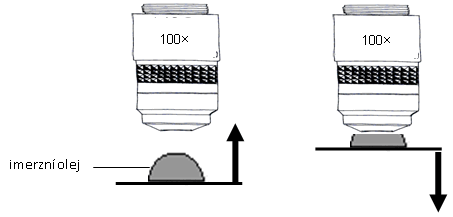
Obr.: Dva způsoby zastavení objektu pod imerzí.
Zásady:
- Mezi objektivem a preparátem musí být imerzní olej, proto je potřeba nanést dostatečně velkou kapku oleje.
- Po skončení práce s imerzním objektivem je nutné očistit čočku objektivu a sklíčko trvalého preparátu alkoholem.
- Nepodaří-li se zastavit pozorovaný objekt pod imerzním objektivem, je třeba olej odstranit a celý postup zopakovat.
Eukarya (eukaryota) – živočišná buňka, protozoa
Úkol 1: Tvar buněk – nervová buňka
TP: mícha
Ve ventrálních rozích šedé hmoty míšní vyhledejte neurony, pozorujte a zakreslete tvar nervové buňky (neuron).
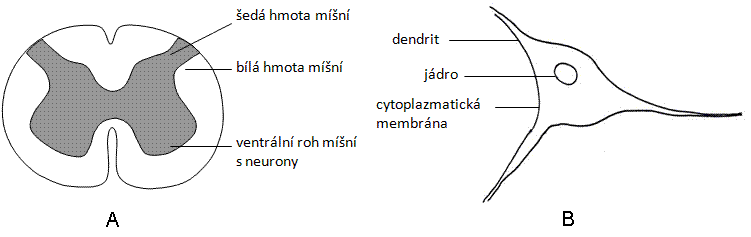
Obr.: A – průřez míchou, B – složení neuronu.
Úkol 2: Tvar a počet jader
TP: jaterní tkáň, leukocyty, nálevníci - trepka (Paramecium sp.), plazivenka (Spirostomum sp.), opalinka žabí (Opalina ranarum)
Pozorujte a zakreslete počet a tvar jader v jednotlivých buňkách. Jádra leukocytů (bílé krvinky) mohou mít tvar kulovitý, bobovitý (ledvinovitý), podkovovitý (tyčinkovitý), segmentovaný (esovitý nebo laločnatý); erytrocyt (červená krvinka) u savčích buněk je bez jádra, u ptáků má jádro oválný tvar. U trepky jsou v cytoplazmě dva typy morfologicky i funkčně odlišných jader: makronukleus (velké jádro vegetativní) a mikronukleus (malé jádro generativní); během procesu konjugace dvou trepek dochází k vzájemné výměně a vývoji těchto jader. Plazivenka má jádro růžencovité/korálkovité (připomíná růženec, korálky na šňůrce), v cytoplazmě opalinky můžeme pozorovat velký počet drobných stejných jader (mnohojaderná buňka).
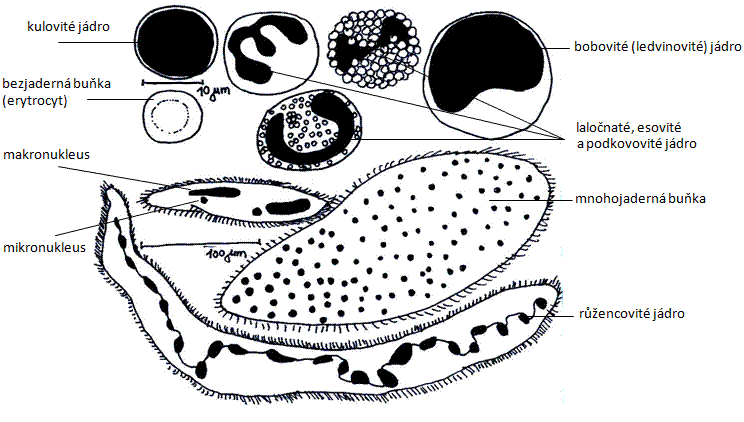
Obr.: Typy buněčných jader.
Úkol 3: Buněčné organely – Golgiho aparát, mitochondrie
TP: tenké střevo (stříbřené a dobarvené hematoxylin-eosinem), játra obarvená na mitochondrie (podle Heidenheina)
Do středu zorného pole zastavte klky střevní sliznice a při větším zvětšení prohlédněte jejich povrchové buňky (enterocyty). V apikální (horní) části buňky nad fialově zbarveným jádrem můžete nalézt Golgiho aparát v podobě hnědočerného klubkovitého útvaru nebo nepravidelné sítě. V jaterních buňkách jsou vidět mitochondrie (drobné tmavě zbarvené čárkovité až oválné útvary) a světlé šedé jádro (případně růžové) s tmavými jadérky. Nakreslete Golgiho aparát a mitochondrie.
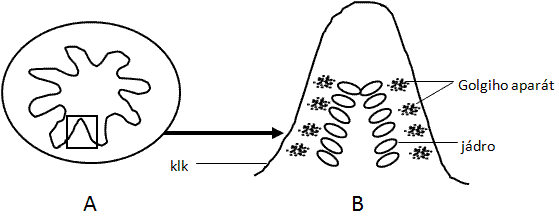
Obr.: A – průřez tenkým střevem, B – střevní klk s enterocyty s Golgiho aparátem a jádrem.
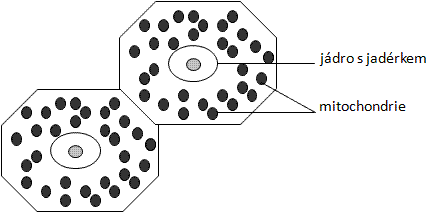
Obr.: Mitochondrie v jaterních buňkách.
Úkol 4: Pigmentové inkluze
TP: kůže žáby
Pod mikroskopem pozorujte buňky epidermis žáby (tzv. chromatofory resp. melanofory) obsahující inkluze pigmentu melaninu. Buněčné inkluze v podobě drobných hnědých zrnek se v cytoplazmě shlukují do hvězdicovitých útvarů s různě dlouhými výběžky, realizuje se tím barvoměna.
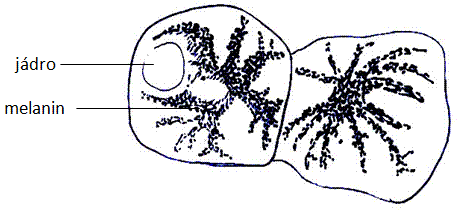
Obr.: Melanofory žáby obsahující melanin.
Eukarya (eukaryota) – rostlinná buňka
Úkol 1: Vakuoly, chloroplasty
NP: bobule ptačího zobu (Ligustrum vulgare), voda, NaOH, kys. octová
Rozřízněte bobuli ptačího zobu a obtiskněte na podložní sklíčko. Přidejte vodu, přikryjte krycím sklíčkem a pozorujte. Jaké je zbarvení vakuol (neutrální prostředí)? Pozorujte, jak se změní zbarvení vakuol po přidání kys. octové (kyselé prostředí) a NaOH (zásadité prostředí) a vaše pozorování zapište. Kromě vakuol lze uvnitř buněk pozorovat i drobné zelené chloroplasty.
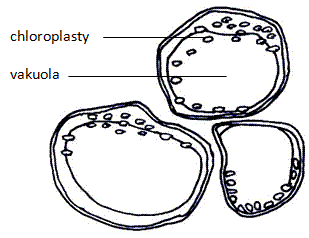
Obr.: Buňky bobule ptačího zobu s centrální vakuolou a chloroplasty.
Úkol 2: RZvýšení turgoru
pyl, voda
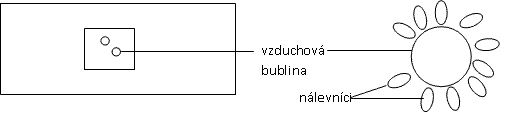
Na podložní sklíčko naneste špejlí pylová zrna, pozorujte a zakreslete jejich tvar. Pylová zrna se někdy v preparátu hůře hledají. Nejdříve se snažte zaostřit na vnitřní hranu krycího skla a poté prohledávejte okraje preparátu meandrovitým způsobem při zvětšení 10× (nezapomeňte clonit a proostřovat). Poté přikápněte k pylu kapku destilované vody, přikryjte krycím sklíčkem a znovu pozorujte a zakreslete. Pronikáním vody do pylových zrn, dojde ke změně jejich tvaru (zvětší se a zakulatí), u některých pylových zrn může docházet k praskání - výronům žlutě zbarvené cytoplazmy. Nezaměňujte ale se vzduchovými bublinami, které mají černé kontury.
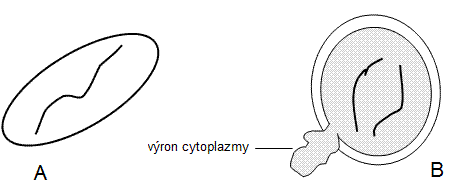
Obr.: Osmotické jevy: A – pylové zrno v izotonickém prostředí, B – pylové zrno v hypotonickém prostředí.
Úkol 3: Plazmolýza (prostá a křečová)
cibule, KNO3
Z cibule sloupněte vnitřní epidermis (protáhlé buňky) a dejte na podložní sklíčko (vyrovnejte epidermis preparační jehlou), přikápněte 1 % neutrální červeň a přikryjte krycím sklíčkem. Po obarvení vakuol do červena přikápněte k hraně krycího skla kapku 1M KNO3 (hypertonické prostředí) a z protilehlé hrany krycího skla odsajte filtračním papírem tekutinu pod krycím sklem. V mikroskopu pozorujte plazmolýzu - oddělování cytoplazmy od buněčné stěny z důvodu úniku vody z buňky do hypertonického prostředí. V jednom preparátu můžete pozorovat zároveň prostou plazmolýzu (oddělování cytoplazmatické membrány od buněčné stěny na protilehlých stranách buňky) a křečovou plazmolýzu (nestejnoměrné oddělování cytoplazmatické membrány od buněčné stěny, centrální vakuola je křečovitě stažená). Plazmolýza může být vratný proces. Nakreslete a napište závěr.
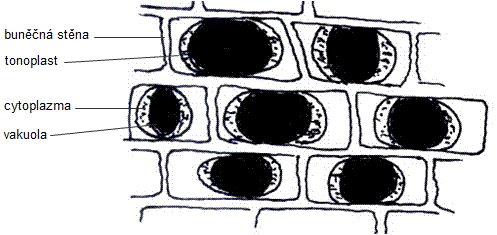
Obr.: Osmotické jevy v buňkách epidermis cibule - prostá plazmolýza
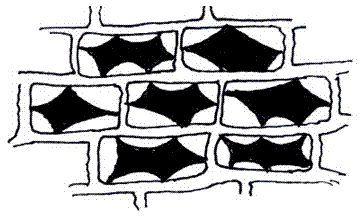
Obr.: Osmotické jevy v buňkách epidermis cibule - křečová plazmolýza
Pohyb a taxe, nativní preparáty
Úkol 1: Brownův molekulární pohyb
NP: suspenze oxidu železitého
Kápněte na podložní sklo suspenzi oxidu železitého a přikryjte krycím sklem a pozorujte jednu malou částici a zakreslete trajektorii jejího pohybu.
Jaký je princip pohybu částice?
Úkol 2: Buňky s řasinkami
TP: buňky s řasinkovým epitelem obarvené hematoxylin-eosinem
Pozorujte a zakreslete buňky cylindrického nebo kónického tvaru s viditelným jádrem a řasinkami na širší základně.
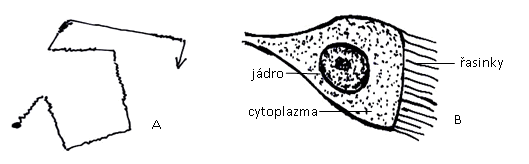
Obr.: A – Brownův molekulární pohyb, B – buňka s řasinkami
Úkol 3: Řasinkový pohyb
NP: senný nálev, detrit z akvária/ video
Z povrchové blanky senného nálevu (nebo detritu z akvária) naberte opatrně kapátkem kapku nálevu, přeneste na podložní sklíčko a pod úhlem 45o přikryjte krycím sklíčkem (rovnoběžně s podložním) tak, aby pod sklíčkem nevznikly vzduchové bubliny. Pozor na chyby: nadbytek vody (vibrace, unášení objektů proudem vody mimo zorné pole, únik ze zaostřené optické roviny, voda na stolku, kondenzoru), nedostatek vody (bubliny, rychlé vyschnutí preparátu). V preparátu pozorujte rychle se pohybující buňky jednobuněčných eukaryot, především nálevníky různých velikostí, drobné bičíkovce, a také velké množství prokaryot (bakterií).
Pohyb řasinek lze pozorovat na obrvených buňkách nálevníků, ale i na povrchu mikroskopických živočichů z akvária (ploštěnky, vířníci). U nálevníků pozorujte i potravní a pulzující vakuoly. Pro lepší pozorování lze použít fázový kontrast.
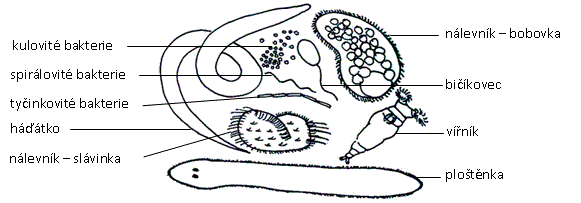
Obr.: Zástupci mikrofauny
Úkol 4: Améboidní pohyb
NP: senný nálev/video
Připravte NP z povrchové blanky senného nálevu a pozorujte améby. Zpočátku jsou améby podrážděné a zakulacené, po několika desítkách sekund se přemění v plošší formy a začnou vysílat panožky (pseudopodie) ve směru pohybu. Panožky jsou homogenní, cytoplazma je granulovaná. Pozorujte, nakreslete a popište princip améboidního pohybu.
Úkol 5: Bičíkový pohyb
NP: spermie, senný nálev/video
Kápněte spermie z inseminační dávky (v médiu androhep) na nahřáté podložní sklíčko a pozorujte pohyb spermií a to směrem dopředu a rotaci kolem osy (mění se šířka hlavičky, bičík je na zadním konci buňky, buňku tlačí před sebou). Obdobně lze pozorovat bičíkový pohyb u bičíkovců v NP zhotoveném ze senného nálevu (většina volně žijících bičíkovců má bičík na přední části buňky, bičík táhne buňku za sebou). Pro zpomalení nálevníků odsajte část vody pod sklíčkem pomocí filtračního papíru.
Úkol 6: Struktura příčně pruhovaného svalu
TP: příčně pruhovaný sval z končetiny hmyzu obarvený Heidenheinovým hematoxylinem a příčně pruhovaný sval potkana obarvený haematoxylin-eosinem
Pozorujte oba typy preparátů a zakreslete příčné pruhování svaloviny, které je způsobené rozdílnou barvitelností svalových vláken. Vysvětlete princip svalového pohybu.
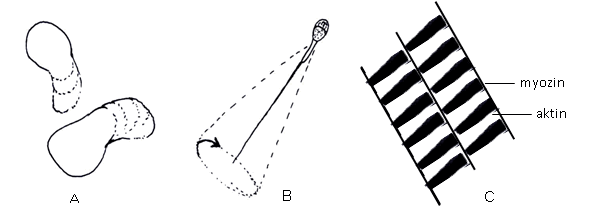
A – améboidní pohyb, B – bičíkový pohyb, C – příčně pruhovaný sval hmyzu.
Úkol 7: Oxygenotaxe u nálevníků
NP: senný nálev
Připravte nativní preparát ze senného nálevu a přikryjte krycím sklíčkem tak, aby pod sklíčkem vznikly vzduchové bubliny. Nálevníci vyhledávají prostředí s optimální tenzí kyslíku a začnou se shromažďovat v okolí bublin. Stejný jev je možné pozorovat při okrajích krycího sklíčka. O jakou oxygenotaxi se jedná? (pozitivní nebo negativní)
Vyšetření krve
Úkol 1: Příprava trvalého preparátu suchou cestou – krevní nátěr
krev
K jedné straně odmaštěného podložního skla kápněte malou kapku nesrážlivé krve. Před kapku krve přiložte pod úhlem 45o podložní sklo se zabroušenými rohy a nechejte krev roztéct podél hrany sklíčka a poté plynulým tahem rozetřete kapku po podložním skle (kapka krve se táhne za sklíčkem). Krevní nátěr musí být tenký, rovnoměrný, asi do 2/3 podložního sklíčka. Několikrát postup opakujte, až se vám podaří zhotovit kvalitní krevní nátěr, který nechte zaschnout a prohlédněte pod mikroskopem.
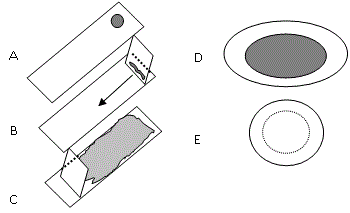
Obr.: Postup zhotovení krevního nátěru: A – kápnutí kapky krve na podložní sklo, B – přiložení krycího skla před kapku krve pod úhlem 45°, C – zhotovení krevního nátěru, D – ptačí erytrocyt (oválný, s jádrem, větší), E – savčí erytrocyt (kulatý, bikonkávní, bez jádra, menší)
Úkol 2: Barvení krevního nátěru (panoptické barvení dle Pappenheima)
krev, May-Grünwald, Giemsa-Romanowski
Zhotovte krevní nátěr (viz předchozí úkol). Po zaschnutí převrstvěte preparát barvivem May-Grünwald a nechejte působit 5 min., poté přidejte destilovanou vodu a opět nechejte 5 min. působit. Slijte a převrstvěte barvivem Giemsa-Romanowski. Po 10 min. slijte, opláchněte destilovanou vodou a k preparátu opatrně přiložte filtrační papír k odsátí zbytků vody. Po odstranění filtračního papíru nechte nátěr zaschnout. Prohlédněte si obarvený krevní nátěr, v kterém můžete kromě erytrocytů pozorovat i leukocyty s modře obarvenými jádry.
Úkol 3: Měření velikosti mikroskopických objektů
TP: ptačí erytrocyty, NP: savčí erytrocyty
Měření velikosti objektů se provádí pomocí okulárového mikrometru (měřítka), který je umístěn v jednom z okulárů. Při měření velikosti objektu je třeba zjistit, kolika dílkům okulárového mikrometru odpovídá měřený objekt. Tento počet dílků se vynásobí mikrometrickým koeficientem pro daný objektiv (každý objektiv má svůj koeficient) a výsledek se vyjádří v µm. Změřte velikost ptačích a savčích erytrocytů. Jaký je rozdíl mezi ptačím a savčím erytrocytem (velikost, tvar a přítomnost jádra)?
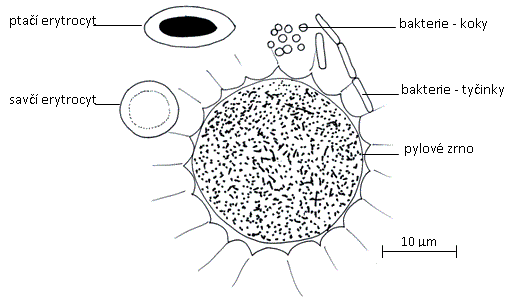
Obr.: Porovnání velikostí různých buněk.
Úkol 4: Hemolýza osmotická (makroskopicky)
krev, fyziol. roztok, voda
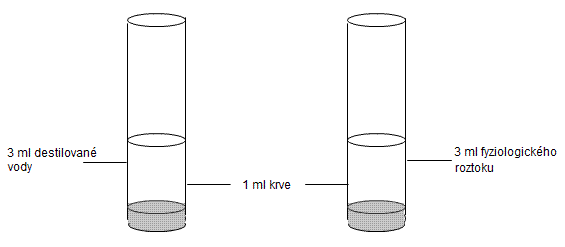
Do dvou zkumavek nalijte po 1 ml savčí krve. Do jedné ze zkumavek přidejte 3 ml fyziologického roztoku a do druhé stejné množství destilované vody. Mírně protřepejte a porovnejte obě zkumavky. Vysvětlete, k čemu v jednotlivých zkumavkách došlo a proč. Proveďte tzv. „čtecí zkoušku“ a výsledky zaznamenejte.
Úkol 5: Hemolýza osmotická (mikroskopicky)
krev, voda
Na podložní sklíčko naneste malou kapku krve a přikryjte krycím sklíčkem. K okraji sklíčka přikápněte kapku destilované vody. Pozorujte postupné ubývání erytrocytů způsobené jejich praskáním (prasklé erytrocyty jsou málo viditelné).
Úkol 6: Plazmorhiza
krev, 1M KNO3
Na podložní sklo naneste kapku krve a přikápněte k ní kapku 1M KNO3. Po přiložení krycího skla pozorujte a zakreslete krvinky svraštělé do hvězdicovitých útvarů, tzv. echinocyty (k této deformaci krvinek může dojít také např. v silných nátěrech, které pomalu vysychaly). Nakreslete a zapište závěr.
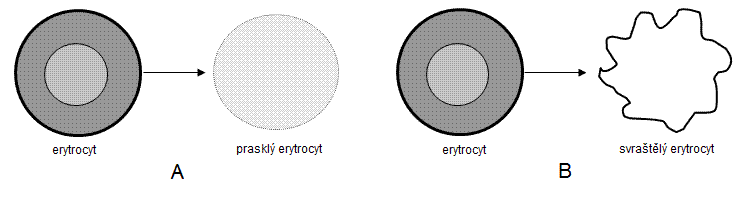
Obr.: Osmotické jevy u savčích erytrocytů: A – hemolýza, B – plazmorhiza.
Úkol 7: Fagocytóza
TP: fagocytující bílé krvinky, barvené Pappenheimovou metodou.
Prohlédněte si preparát, najděte a zakreslete bílé krvinky s fagocytovanými partikulemi. Spočítejte fagocytární aktivitu (FA): FA = počet fagocytujících buněk/počet počítaných buněk.
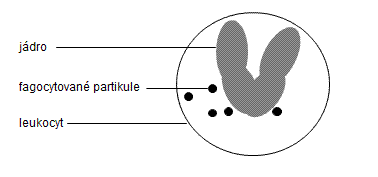
Obr.: Leukocyt s fagocytovanými partikulemi.
Úkol 8: Určování krevních skupin
Pomocí diagnostické soupravy pro určování krevních skupin systému ABO (monoklonální) si určete svoji krevní skupinu a zaznamenejte do protokolu.
Buněčný cyklus, mitóza
Úkol 1: Mitóza v buňkách kořínku cibule
TP: kořínek cibule obarvený v acetorceinu
Mitóza u rostlinných buněk je mnohem výraznější než u buněk živočišných, jednotlivé chromozomy jsou po obarvení acetorceinem patrné a jsou vidět i mikrotubuly dělicího vřeténka. V preparátu najděte a zakreslete jednotlivé fáze mitózy a rovněž buňku v interfázi.

Obr.: Mitóza v buňkách kořínku cibule.
Úkol 2: Mitóza v tkáňové kultuře a mitotický index
TP: preparát z tkáňové kultury z ledvin králíka.
V preparátu najděte a zakreslete jednotlivé fáze mitózy, buňku v interfázi a tzv. monaster (buňka v metafázi při pohledu shora). V preparátu jsou patrné i poruchy mitózy jako je anafázový most.
V 5 zorných polích mikroskopu spočítejte buňky v mitóze a buňky v klidu a dosaďte do vzorce pro MI.
MITOTICKÝ INDEX udává frekvenci mitóz v živočišné tkáni nebo v rostlinném pletivu. Vyjadřuje podíl počtu buněk ve stádiu mitózy k celkovému počtu buněk.
MI (%) = M/N x 100 kde, M = počet buněk v mitóze, N = celkový počet buněk
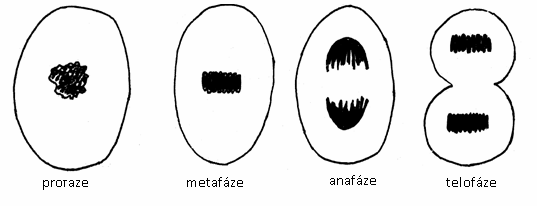
Obr.: Mitóza v živočišné buňce.
Úkol 3: Mitotické buňky v histologickém řezu tenkého střeva
TP: střevo laboratorního potkana barvené hematoxylin-eosinem
Preparát střeva prohlédněte nejdříve při malém zvětšení a zakreslete průřez střeva s vyznačením místa, kde budete hledat mitotické buňky. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy. Buňky v mitóze jsou větší se zaoblenými okraji, světlejší a místo jádra je možné pozorovat některou z mitotických figur.
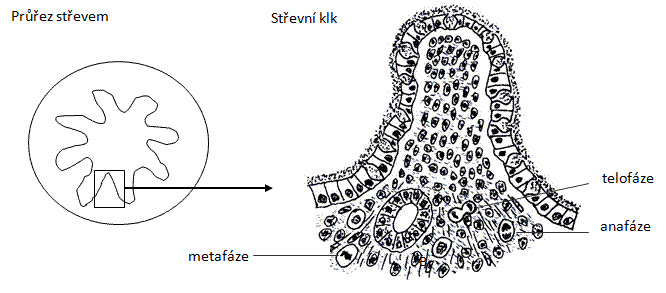
Obr.: Mitóza v epitelu tenkého střeva.
Úkol 4: Mitotické buňky v histologickém řezu dělohy
TP: děloha laboratorního potkana barvená hematoxylin-eosinem
Preparát prohlédněte nejdříve při malém zvětšení a zakreslete průřez dělohou s kubickým epitelem děložní sliznice, kde je možné najít buňky v mitóze. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy.
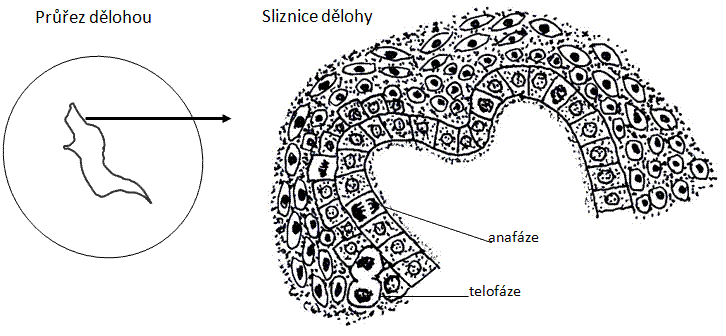
Obr.: Mitóza ve sliznici dělohy.
Úkol 5: Mitotické buňky v histologickém řezu varlat
TP: varle laboratorního potkana barvené hematoxylin-eosinem
Preparát prohlédněte a nakreslete nejdříve při malém zvětšení s vyznačením místa, kde budete hledat mitotické buňky, tj. na obvodu semenotvorných kanálků. Při větším zvětšení se pokuste najít jednotlivé fáze mitózy.
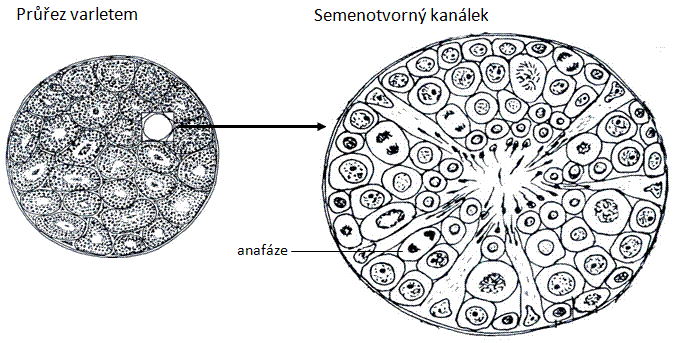
Obr.: Mitóza v semenotvorném kanálku varlete.
Rozmnožování a vývoj
Úkol 1: Spermiogeneze
TP: varle potkana barvené hematoxylin-eosinem.
Spermiogeneze probíhá v semenotvorných kanálcích varlat. Na příčném řezu semenotvorného kanálku jsou patrná jednotlivá vývojová stádia spermiogeneze. Prohlížejte kanálek směrem od periferie do středu kanálku a zakreslete jednotlivé typy buněk. Na periferii semenotvorného kanálku se nachází spermatogonie, menší buňky s jádrem bohatým na chromatin, směrem do středu kanálku se vyskytují spermatocyty I. řádu a spermatocyty II. řádu, které se liší velikostí buněk i typem jader. Blíže ke středu jsou spermatidy s malým množstvím chromatinu v jádrech, v centru kanálku jsou dozrávající spermie. V některých kanálcích převládá pouze určitý typ buněk, proto je důležité prohlédnout větší počet kanálků a zakreslit jednotlivá vývojová stádia buněk.
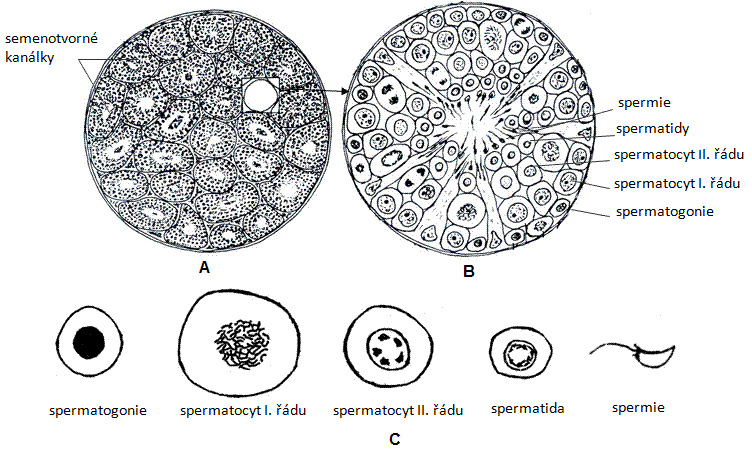
Obr.: Spermiogeneze ve varleti potkana: A – příčný řez varletem potkana, B – semenotvorný kanálek s jednotlivými buňkami spermiogeneze, C – vývojová řada spermiogeneze.
Úkol 2: Pozorování tvaru a velikosti spermií různých druhů zvířat
TP: spermie potkana, králíka, prasete a býka. Fotografie spermií dalších druhů živočichů.
Pozorujte a zakreslete v poměrných velikostech jednotlivé typy spermií lišících se počtem a délkou bičíků, tvarem hlavičky a velikostí akrozomu (struktura ve tvaru čepičky, která obklopuje přední polovinu hlavičky, obsahuje důležité enzymy, které umožňují pronikání hlavičky spermie do vajíčka).
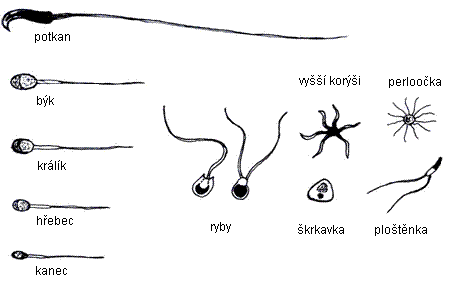
Obr.: Ukázky spermií různých živočichů v poměrných velikostech.
Úkol 3: Meióza
TP: obarvené podélné řezy varlat brouka smrtníka obecného (Blaps mortisaga).
Prohlédněte si v TP několik řezů varlat a hledejte jednotlivé fáze meiózy. Do protokolu zakreslete charakteristickou strukturu jader meiotické profáze I v chronologicky správném pořadí.
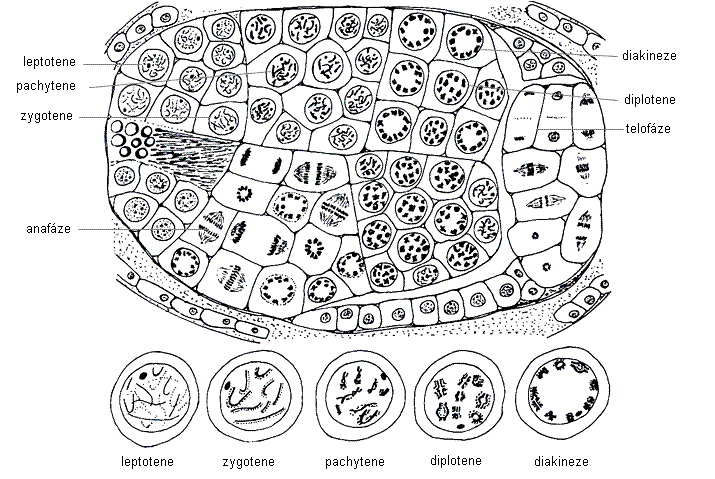
Obr.: Meióza v podélném řezu varlete brouka smrtníka obecného.
Úkol 4: Oogeneze
TP: ovarium potkana
Prohlédněte si preparát ovaria potkana. Najděte a zakreslete oocyt s několika folikulárními buňkami (tzv. primární folikul, tj. nezralý) a Graafův folikul, tj. zralý folikul obsahující zralý oocyt se zmnoženými folikulárními buňkami a dutinkami vyplněnými tekutinou.
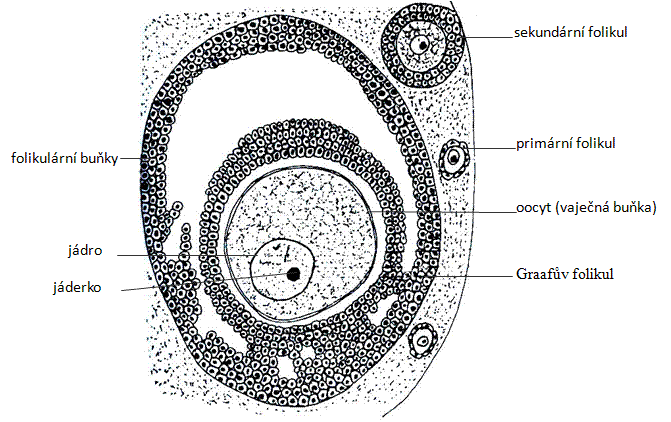
Obr.: Oogeneze ve vaječníku potkana.
Úkol 5: Cytologické změny vaginální sliznice v průběhu estrálního cyklu
TP: obarvené vaginální výtěry potkana v různých fázích estrálního cyklu
V každé fázi estrálního cyklu převládá charakteristický typ buněk. Pozorujte a zakreslete nálezy typické pro jednotlivé fáze estrálního cyklu.
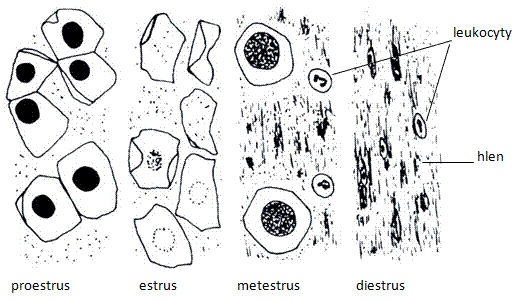
Obr.: Jednotlivé fáze estrálního cyklu s typickým nálezem ze stěru z poševní sliznice.
Úkol 6: Rýhování vajíčka králíka
TP: vajíčko obklopené folikulárními buňkami a vajíčko se 2 blastomerami. Fotografie vajíčka se 2 pólovými tělísky a vajíčka s 8 blastomerami.
Prohlédněte si trvalé preparáty a fotografie a zakreslete zralé vajíčko a jednotlivá stádia rýhování.
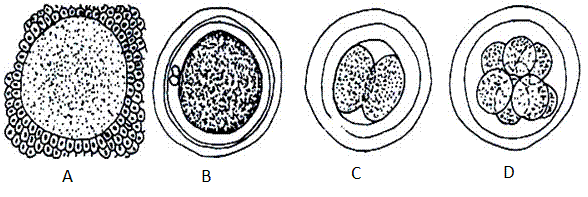
Obr.: Vajíčko králíka: A – neoplozené vajíčko, B – vajíčko po oplození, C – 2 blastomery, D – 8 blastomer.
Úkol 7: Pučení kvasinek
NP: suspenze kvasinek v kultuře
Zhotovte nativní preparát ze suspenze kvasinek. Pozorujte a zakreslete pučení, tj. vznik pupenu na pólu některých buněk, který se postupně zvětšuje a nakonec se odloučí od mateřské buňky.
Obr.: Pučení kvasinky.
Úkol 8: Vývoj jednotlivých druhů živočichů
TP: Hmyz s proměnou nedokonalou – (luptouš Menacanthus currucae nebo péřovka Degeeriela rufa). Kyvety s vývojovými stadii hmyzu s proměnou dokonalou (motýl bekyně velkohlavá Lymantria dispar), ryby (pstruh obecný Salmo trutta), obojživelníka (skokan hnědý Rana temporaria), ptáka (kur domácí Gallus gallus) a savců (potkan Rattus norvegicus, plod člověka Homo sapiens).
Prohlédněte si vývojová stádia hmyzu s proměnou nedokonalou (vajíčko, larva, nymfa II. a III. instaru, imago), hmyzu s proměnou dokonalou (vajíčko, larva, kukla, imago), ryby (jikra, zárodek, vykulený plůdek se žloutkovým vakem), obojživelníků (vajíčko, pulec, žába s pulčím ocáskem, žába), ptáků (vejce, embryo vyjmuté z vejce, kuře po vylíhnutí) a savců (děloha v raném a pozdním období gravidity, plod potkana).
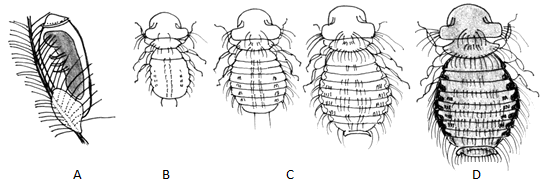
Obr.: Vývoj hmyzu s proměnou nedokonalou (všenka): A – vajíčko, B – larva, C – nymfa II. a III. instaru, D – imago (dospělec).
Modelový organizmus
Úkol 1: Křížení drozofil s různě zbarvenýma očima
Drosophila melanogaster – samec a samice s různou barvou očí
Křížení původní (divoké) formy drozofily s červenýma očima a mutantní linie drozofily s bílýma očima. Jedná se o pokus, který bude probíhat během 3 cvičení:
1. cvičení - zahájení pokusu
Na cvičeních budete pracovat ve skupinách. Každá skupina dostane Erlenmeyerovu baňku s čerstvým živným médiem a 2 zkumavky s drozofilami vytříděnými podle pohlaví. Prohlédněte si obě zkumavky (někdo bude mít červenooké samečky a bělooké samičky, jiní zase červenooké samičky a bělooké samečky), všimněte si a zaznamenejte rozdíly mezi oběma pohlavími a různě zbarvených očí. Poté opatrně přesypte drozofily (samečky i samičky) do Erlenmeyerovy baňky, kterou si důkladně popište.
2. cvičení - odstranění dospělých drozofil z pokusu
Na vatu připevněnou zespodu uzávěru uspávací nádobky kápněte trochu éteru a nádobku uzavřete. Za chvíli nádobku otevřete a vytřepejte do ní mouchy z kultivační nádoby. Mouchy jsou během několika sekund znehybněny a můžete je přesypat do zkumavky.
3. cvičení - hodnocení výsledku pokusu
Pomocí éteru uspěte mouchy (potomky křížení) a roztřiďte je podle pohlaví a barvy očí a odvoďte, jak se tento znak dědí.
Úkol 2: Mutantní linie
Mutantní linie drozofil (white, yellow, ebony, curly, vestigial) - živé, v lihu a na obrázku.
Prohlédněte si jednotlivé mutantní linie drozofil a zakreslete.
Cytogenetika
Úkol 1: Struktura polytenních chromozomů
TP: slinné žlázy larev pakomárů (Chironomus sp.) s obrovskými chromozomy.
Pozorujte buňky s polytenním chromozomem v buněčném jádru označovaném jako pentlicovité jádro. Pod větším zvětšením jsou na chromozomu patrné různě široké, odlišně se barvící okrsky, tzv. chromomery, které připomínají „čárový kód“. Dále jsou na chromozomu patrné zduřeniny, tzv. pufy. Zakreslete buňku slinných žláz s polytenním chromozomem.
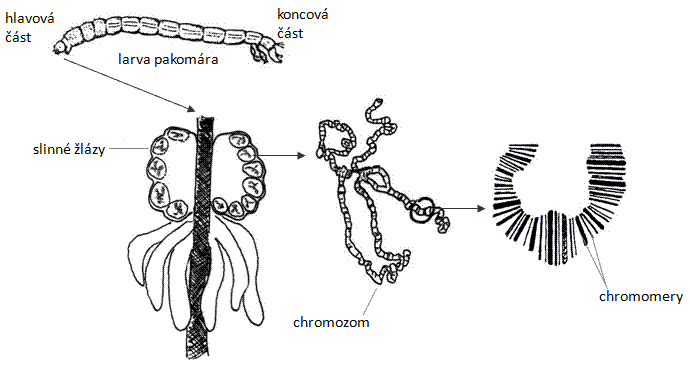
Obr.: Polytenní chromozom v buňkách slinných žláz z larev pakomára.
Úkol 2: Karyotypy savců
TP: karyotypy králíka (44), prasete (38), ovce (54), koně (64), skotu (60) a člověka (46) obarvené metodou podle Giemsy po předchozí kultivaci s kolchicinem.
V TP z krve jednotlivých zástupců savců hledejte chromozomy. Porovnejte počty a tvary chromozomů jednotlivých druhů savců na základě mikroskopického pozorování. Zakreslete alespoň jeden karyotyp. V čem je zvláštní karyotyp skotu?
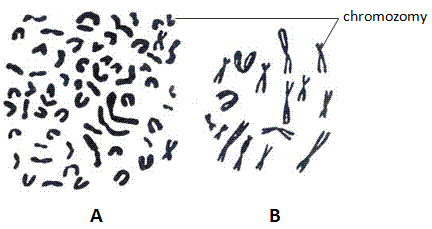
Obr.: Ukázka karyogramu: A – tur domácí (Bos taurus), B – cibule kuchyňská (Allium cepa).
Úkol 3: Zápis karyotypů
Pokuste se správně zapsat následující karyotypy:
- karyotyp zdravého muže a ženy
- karyotyp býka, klisny, berana
- karyotyp muže s Downovým syndromem a muže s Klinefelterovým syndromem
- karyotyp ženy s Edwardsovým syndromem a ženy s Turnerovým syndromem
Metody molekulární biologie
Cvičení z molekulární biologie jsou sestavena tak, aby se studenti prakticky seznámili se základními metodami, které se využívají k analýze DNA. Studenti si sami vyzkouší izolaci DNA, amplifikaci DNA pomocí PCR, restrikční štěpení PCR produktu, elektroforézu, vizualizaci DNA a hodnocení výsledku. Tyto metody budou využity při řešení jednoho komplexního úkolu. Bude se jednat o určení pohlaví ptačího jedince z biologického materiálu pomocí restrikční analýzy PCR produktu specifického genu. Každý student bude pracovat samostatně. Materiál k vyšetření bude zajištěn, ale lze si zajistit svůj vlastní materiál.
Instrukce k zajištění vlastního materiálu: K vyšetření lze použít jakékoliv ptačí buňky obsahující DNA. Lze odebrat krev od ptačího jedince zaživa, krev nebo orgány během porážky (kur, husa, kachna....), případně odebrat tkáň z drůbežího masa koupeného v tržní síti.
Ptačí krev:
- odběr do zkumavky s anti-koagulans EDTA (zkumavky budou k vyzvednutí u laborantky)
- požadovaný objem je minimálně 200 µl
- po odběru je třeba vzorek uložit do mrazáku při teplotě pod -15 °C
Ptačí tkáň (svalovina či vnitřní orgán):
- odběr do igelitového sáčku nebo mikrozkumavky
- o velikosti minimálně dvou špendlíkových hlaviček
- po odběru je třeba vzorek uložit do mrazáku při teplotě pod -15 °C
Vzorek je třeba označit (jméno studenta, číslo skupiny) a předat laborantce k evidenci a uložení do mrazáku ve cvičebně. Vzorky je potřeba přinést nejpozději do cvičení, kdy bude probíhat příprava tkáně k izolaci DNA.
Úkol 1 a 2: Příprava tkáně k izolaci DNA a vlastní izolace DNA
Izolace DNA se provádí pomocí izolační soupravy založené na principu adsorpce DNA na silikát. Vyšetřovaný materiál (ptačí krev či tkáň) je nejdříve lyzován pomocí lyzačního pufru (obsahuje detergenty, které rozpouští membrány a denaturuje proteiny) a enzymu proteinázy K (štěpí proteiny včetně histonů vázajících se na DNA). Buněčný lyzát se přenese na izolační kolonku, jejíž součásti je silikátový povrch (SiO2 – sklo). V přítomnosti chaotropních solí (součást lyzačního pufru) adheruje DNA na silikát. Kolonka s DNA vázanou na silikát je promyta promývacími roztoky a následně uvolněna pomocí elučního pufru. Vzhledem k tomu, že různé izolační soupravy od jednotlivých výrobců se poněkud liší, pokud jde o jednotlivé komponenty (zejména použité roztoky a jejich pipetované objemy), není možné uvést vždy platný konkrétní sled kroků a je třeba se vždy řídit předepsaným postupem od příslušného výrobce, který vám bude k dispozici na cvičení.
Zásady práce:
- Každý student zpracovává vlastní vzorek a pracuje v pracovní skupině, která má k dispozici sadu automatických pipet.
- U pipet lze nastavit požadovaný objem - pozor na přetočení pipety mimo dané rozmezí.
- K zabránění kontaminace vzorku a chemikálií se pro jednotlivé kroky používá vždy nová špička.
- K zabránění kontaminace pipet se pro práci s DNA používá špička s filtrem.
- K zajištění přesného objemu je třeba důkladně nasadit špičku na pipetu.
- Požadovaný objem se získá stlačením pipety do první polohy a ponořením špičky pipety do nasávané tekutiny, povolením stlačení, přenesením požadovaného objemu a stlačením pipety do druhé polohy.
- Homogenizace vzorku se provádí ve zkumavce tzv. propipetováním tj. po přidání určité chemikálie do zkumavky třikrát opakovaně nasát směs do špičky a vytlačit.
- Mikrozkumavky je třeba označit číslem skupiny a pořadovým číslem studenta ve skupině.
Úkol 3: PCR
Příprava PCR:
-
Každá pracovní skupina si do mikrozkumavky (1,5 ml) připraví společnou PCR směs dle počtu vzorků (n) s rezervou (n+1):
Směs pro jeden vzorek:
- 10 µl - PCR master mix (směs nukleotidů dNTP, DNA polymerázy a Mg2+ iontů)
- 0,2 µl - primer PP (pořadí nukleotidů: TCTGGATCGCTAAATCCTTT)
- 0,2 µl - primer P8 (CTCCCAAGGATGAGRAAYTG) (R a Y - degenerované nukleotidy)
- 7,6 µl - voda pro PCR
- Napipetujte (novou špičkou) 18 µl PCR směsi do PCR mikrozkumavky (0,2 ml) označené fixem.
- Napipetujte (špičkou s filtrem) 2 µl izolované DNA.
- Uzavřete důkladně PCR mikrozkumavku, vložte ji do termocykleru a spusťte program.
-
Po dokončení programu bude PCR produkt uchován v lednici.
Program PCR amplifikace (trvá asi 1 hod 55 min):

Úkol 4: Restrikční reakce s PCR produktem, elektroforéza, vizualizace a hodnocení
K určení pohlaví u ptáků se využívá gen CHD (Chromo-Helicase-DNA binding gene), který kóduje protein, jež reguluje aktivaci transkripce na úrovni chromatinu. Tento gen je u ptáků lokalizován na pohlavních chromozomech.
- Samčí pohlaví je u ptáků homogametické s pohlavními chromozomy ZZ.
- Samičí pohlaví je heterogametické s pohlavními chromozomy ZW.
Pomocí PCR je namnožena DNA odpovídající části genu na chromozomu W (CHD-W) a na chromozomu Z (CHD-Z). PCR produkt je štěpen pomocí restrikční endonukleázy (restriktázy) Hae III (izolované z bakterie Haemophilus aegyptius) v restrikčním místě:
PCR produkt genu CHD-Z toto místo obsahuje, proto dojde působením enzymu k odštěpení fragmentu DNA, zatímco PCR produkt genu CHD-W se enzymem neštěpí. Fragmenty jsou separovány pomocí gelové elektroforézy, vizualizovány pod UV zářením a vyhodnoceny.
Restrikční reakce:
- Napipetujte 1,2 µl směsi restriktázy Hae III a aktivačního pufru do nové označené PCR zkumavky (0,5 ml).
- Napipetujte (novou špičkou s filtrem) 10 µl PCR produktu.
- Vložte do termocykleru při teplotě 37 °C na 45 min.
Příprava 1,2 % agarózového gelu:
Připraví se jeden gel pro všechny studenty ve cvičebně.
- Do baňky typu Erlen dejte 1,2 g agarózy.
- Skleněným válcem odměřte 100 ml TBE pufru, přidejte do baňky a kroužením promíchejte.
- Dejte baňku do mikrovlnné trouby a vařte při teplotě nastavené na maximální ohřev po dobu 2 minut (jakmile začne obsah kádinky bublat, přerušte ohřev a promíchejte obsah kádinky v ruce s nasazenou rukavicí).
- Po 2 minutách ohřevu vyjměte baňku z mikrovlnné trouby a opatrně ji ochlaďte pod tekoucí vodou na teplotu přibližně 60 °C (teplota, kdy několik sekund udržíme kádinku přiloženou ke hřbetu ruky).
- Do rozehřátého roztoku agarózy napipetujte (novou špičkou) 3 µl Midori Green (10 tis. krát koncentrovaný roztok) a v ruce promíchejte.
- Připravte si nalévací vanu a přelijte do ní rozehřátý roztok agarózy z baňky do výšky minimálně 8 mm.
- Do vany vložte hřebínek a pipetovací špičkou odstraňte případné bubliny v gelu.
- Gel ztuhne asi po 30 minutách.
Horizontální agarová gelová elektroforéza a vizualizace DNA
- Po ztuhnutí gelu vyjměte hřebínek, otočte gel v elektroforetické vaně a zalijte TBE pufrem, tak aby byl celý gel ponořený.
- Do jedné z jamek v gelu (nejlépe do prostřední) naneste 3 µl velikostního markeru.
- Do sousední jamky naneste 10 µl směsného vzorku PCR produktu (směsný vzorek PCR produktu připravíte smícháním všech vzorků ve cvičebně).
- Do dalších jamek nanáší (novou špičkou) každý student svůj vzorek, tj. 10 µl PCR produktu po restrikční analýze. S pipetou je třeba manipulovat opatrně, ať neprotrhnete gel.
- Zapojte elektroforetickou vanu do zdroje a pusťte elektrický proud při konstantním napětí 160 V po dobu 15-20 minut.
- Po ukončení elektroforézy přemístěte gel na UV-transiluminátor a pod UV zářením odečtěte výsledek. V rámci bezpečnosti je třeba pozorovat gel přes plastový kryt.
U samičího pohlaví: (ZW) se na gelu objeví 2 pruhy (bandy). Jeden větší, který odpovídá neštěpenému CHD-W (o stejné velikosti jako neštěpený PCR produkt) a druhý menší asi o 50 bp (párů bází).
U samčího pohlaví: dojde ke štěpení CHD-Z a na gelu se objeví jeden pruh o menší velikosti.
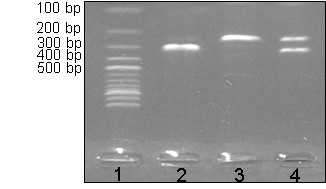
Obr.: Výsledek gelové elektroforézy: 1 – velikostní standard, 2 – neštěpený PCR produkt, 3 – samec, 4 – samice.
Úkol 5: Sekvenátor a sekvenování DNA
Než proběhne restrikční reakce nebo gelová elektroforéza navštivte Laboratoř sekvenční analýzy na Ústavu biologie a chorob volně žijících zvířat, kde se seznámíte s osmikapilárovým automatickým sekvenátorem (Beckman Coulter CEQ 8000), který slouží ke stanovení sekvence DNA na principu separace fragmentů DNA syntetizovaných terminační enzymovou Sangerovou metodou.
Buněčné a tkáňové kultury
Úkol 1: Pozorování buněk v buněčné kultuře
TP: ledvinné buňky králíka z buněčné kultury
Pozorujte a zakreslete si ledvinné buňky králíka z buněčné kultury.
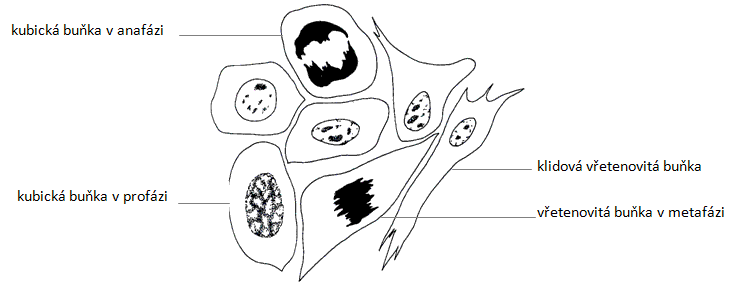
Obr.: Buňky rozdílné morfologie z buněčné kultury v klidové fázi a v mitóze.
Úkol 2: Práce s inverzním mikroskopem a buněčnou kulturou
NP: adherentní buňky z buněčné kultury
V inverzním mikroskopu si prohlédněte kultivační láhev s buněčnou kulturou (všímejte si tvaru buněk pokrývajících celé dno láhve). Slijte médium z láhve, propláchněte roztokem PBS (phosphate buffered saline, fosfátem pufrovaný fyziologický roztok) a do láhve přidejte 2 ml trypsinu. Účinkem trypsinu dojde k uvolnění buněk ze dna láhve, což se projeví zakalením obsahu láhve (uvolňování buněk lze urychlit umístěním láhví do termostatu na 37 oC nebo mechanicky klepáním láhve o dlaň ruky). Pod inverzním mikroskopem pozorujte uvolněné buňky, které jsou zakulacené a volně plavou. Do kultivační láhve přidejte médium obsahující sérum, které inhibuje účinek trypsinu, tak aby se zabránilo natrávení buněk. Poté slijte obsah láhve do kádinky, připravte si nativní preparát a pozorujte pod svým mikroskopem. Zakreslete si tvar buněk a porovnejte s tvarem, který měly buňky přisedlé.
Nebuněčné formy života
Úkol 1: Viry
Nakreslete si do sešitu alespoň 3 zástupce různých druhů virů. Můžete si vybrat virus známého onemocnění nebo virus, kde je patrný vztah mezi vzhledem a názvem - např. filovirus (filum = vlákno), kalicivirus (calyx = kalich), coronavirus (corona = koruna, věnec), parvovirus (parvus = malý), toga (toga = plášť, obal).
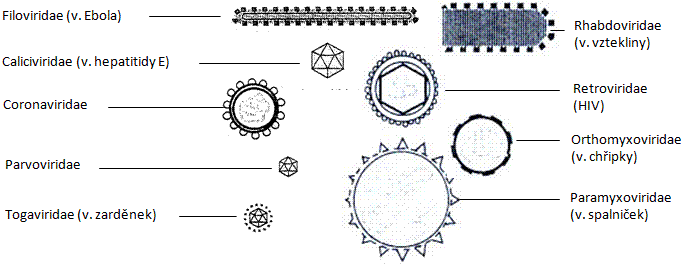
Obr.: Někteří zástupci virů.
Fyzikální a chemické vlivy vnějšího prostředí
Úkol 1: Fotodynamie
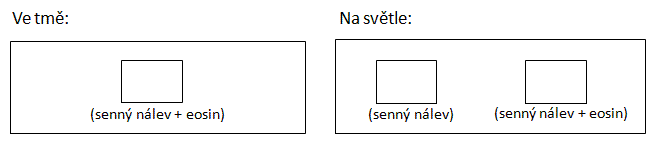
NP: senný nálev, eosin
Připravte si 2 podložní sklíčka. Na jedno dejte kapku senného nálevu a k tomu přidejte kapku eosinu a preparát umístěte do tmy (první kontrola). Na druhé sklíčko dejte dvě kapky senného nálevu: jedna z nich bude bez eosinu (druhá kontrola), k druhé kapce přidejte eosin (vlastní pokus) a sklíčko umístěte na denní světlo. Preparáty prohlížejte zhruba každé 3 min. a porovnejte, co se děje s nálevníky ve vlastním pokusu a ve dvou kontrolách. V preparátu na světle je možno pozorovat nejdříve podráždění (excitaci), které se projevuje zrychlením pohybu nálevníků. Po excitaci dochází ke zpomalení pohybu, až k jeho zastavení a úhynům prvoků.
Úkol 2: Vliv ionizujícího záření na varle potkana
TP: varle potkana (normální tkáň a tkáň po ozáření dávkou 6,5 Gy = grayů), barvený hematoxylin-eosinem
Nejprve si prohlédněte a nakreslete normální tkáň a poté tkáň po ozáření při malém a pak i při větším zvětšení. Porovnejte hustotu semenotvorných kanálků, jejich strukturu, tvar buněk a barvitelnost jader.
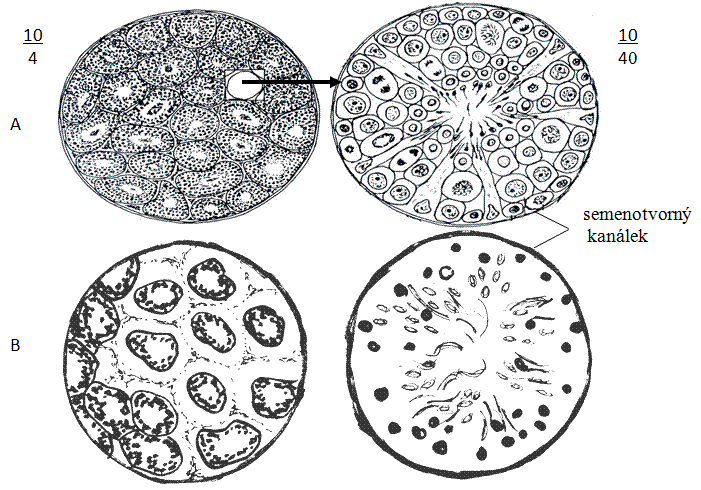
Obr.: Porovnání struktury varlete a semenotvorného kanálku potkana: A – před ozářením (při malém a větším zvětšení), B – po ozáření (při malém a větším zvětšení).
Úkol 3: Oligodynamie
NP: senný nálev, voda nad rtutí
Na podložní sklo naneste kapku vody, pod níž byla uchovávaná rtuť, a do ní přidejte kapku senného nálevu. Pozorujte preparát s nálevníky každé 3 min. a porovnejte s kontrolní skupinou prvoků v čisté vodě. Nejprve dojde k excitaci prvoků, pak k útlumu pohybu a nakonec k úhynu. Zaznamenejte výsledky pozorování.
Úkol 4: Vliv CdCl2 na varle potkana
TP: varle potkana (normální tkáň a tkáň potkana, kterému byl aplikován CdCl2), barvený hematoxylin-eosinem
Prohlédněte si a porovnejte preparát varlete potkana po účinku CdCl2 s kontrolním preparátem. Všimněte si snížení počtu spermiotvorných buněk a zvýšení počtu doprovodných buněk (Sertoliho buňky) a zakreslete rozdíly.
Úkol 5: Vliv fytoncidů na nálevníky
NP: senný nálev, cibule
Nakrájejte cibuli na malé kousky a rozetřete v třecí misce s mořským pískem na jemnou kašovitou hmotu. Na podložní sklíčko kápněte senný nálev a zkontrolujte přítomnost nálevníků. Preparát umístěte na podložku do Petriho misky, na jejímž dně je přidaná rozdrcená cibule. Po 3-5 min kontrolujte pohyblivost nálevníků v Petriho misce i v paralelně připravené kontrole mimo Petriho misku. Zaznamenejte výsledky pozorování.
Tyto výukové materiály byly spolufinancovány Evropským sociálním fondem a státním rozpočtem ČR.

OPVK
Veterinární a farmaceutická univerzita BrnoPalackého tř. 1/3
tel.: +420 54156 1111
IČ 62157124
Obsah
- Na úvod aneb co vás čeká
- Metody získávání informací v biologických vědách
- Lupy a mikroskopy
- Mikroskopická technika
- Biologie
- Chemické složení bioplazmy
- Prokaryota, zastavení objektu pod imerzí
- Eukarya – živočišná buňka, protozoa
- Eukarya – rostlinná buňka
- Pohyb a taxe, nativní preparáty
- Vyšetření krve
- Buněčný cyklus, mitóza
- Rozmnožování a vývoj
- Modelový organismus
- Cytogenetika
- Metody molekulární biologie
- Buněčné a tkáňové kultury
- Nebuněčné formy života, elektronové mikroskopy
- Fyzikální a chemické vlivy vnějšího prostředí
- Genetika
- Mendelismus, monohybridismus
- Dihybridismus, polyhybridismus a rozvětvovací metoda
- Polymorfní geny
- Dědičnost a pohlaví
- Genové interakce
- Vazba genů
- Nemendelistická dědičnost
- Kvantitativní genetika
- Populační genetika


